 研发追踪
研发追踪
 佰傲谷BioValley
佰傲谷BioValley
 2022.12.30
2022.12.30
 2618
2618
近日(2022年12月28日),TG Therapeutics公司宣布,其CD20单抗ublituximab获FDA批准上市,用于治疗复发型多发性硬化症(MS)。
此次批准主要基于ULTIMATE I和ULTIMATE II的两项III期临床数据。两项临床试验均达到临床终点。试验结果结果显示,治疗96周后,与对照组相比,ublituximab显著降低了RMS患者的年化复发率(ARR)。在ULTIMATE I试验中,ublituximab组(n=271)的ARR为0.076,对照组(n=274)则为0.188。在ULTIMATE II试验中,ublituximab组患者(n=272)的ARR为0.091,对照组(n=272)为0.178。
ublituximab为TG Therapeutics开发的一种靶向CD20shagn独特表位的糖化工程单克隆抗体,作用机制与已获批的抗CD20单抗相似。ublituximab通过岩藻糖修饰,大幅度提高了ADCC活性,增加了ublituximab效力。
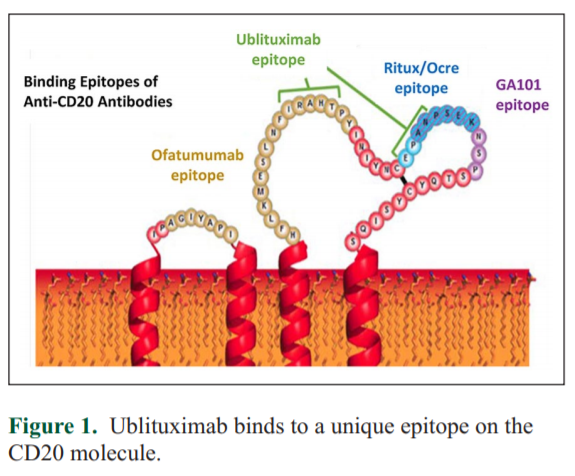
1997年第一款药品批准上市至今,抗CD20单抗已经发展到了第三代,药物活性和免疫原性都有了很大改善。第一代以人鼠嵌合单抗——利妥昔单抗为代表;第二代以人源化单抗——奥法木单抗为代表;第三代以单抗Fc段被修饰的阿妥珠单抗为代表,随着人源化程度的提高,新一代抗CD20单抗显示出越来越高的活性和越来越低的耐药性及副作用;同时新的适应症也不断被发掘。

作为治疗B细胞淋巴瘤的理想靶点,除了CD20 单抗以外,越来越多的靶向疗法选择CD20,包括双抗、ADC、CAR-T等等。
英文原文:https://www.tgtherapeutics.com/our-pipeline/ublituximab/

 新浪医药
新浪医药
 2018.07.12
2018.07.12
 34356
34356

 医药地理
医药地理
 2018.10.22
2018.10.22
 18824
18824

 医谷
医谷
 2019.03.18
2019.03.18
 18772
18772