 产业资讯
产业资讯
 Insight数据库
Insight数据库
 2023.03.22
2023.03.22
 1363
1363
3 月 20 日,第一三共更新了 HER3 ADC 新药 Patritumab Deruxtecan(HER3-DXd,U3-1402)的两项临床结果,分别针对非小细胞肺癌和乳腺癌。这些数据发表在日本肿瘤内科学会(JSMO)年会上。
最新临床结果再次佐证了 Patritumab Deruxtecan 对两个癌种中特定患者群体令人鼓舞的疗效:EGFR 突变 NSCLC、HER3 表达转移性乳腺癌。其中,EGFR 突变 NSCLC 也是 Patritumab Deruxtecan 的首发适应症,注册 II 期临床 HERTHENA–Lung01 今年即将释放数据,III 期临床试验 HERTHENA–Lung02 也在进行中。

在 EGFR 突变 NSCLC 中绽放光芒
据 Insight 数据库显示,第一三共针对 NSCLC 共登记开展了 4 项 HER3 ADC 临床试验。
这 4 项临床试验包括两项 I 期临床,分别评估 Patritumab Deruxtecan 单药治疗重度预处理的 EGFR 突变 NSCLC 患者、或联用三代 EGFR-TKI 奥希替尼一线或二线治疗 EGFR 敏感突变 NSCLC 患者;II 期注册临床 HERTHENA–Lung01 研究,和 III 期临床试验 HERTHENA–Lung02 研究。
HER3 ADC 肺癌临床试验登记

数据来自 Insight 数据库
本次更新结果的是第一项开放标签、全球多中心 1 期临床(ClinicalTrials.gov: NCT03260491),在亚洲、欧洲和北美共入组 264 名患者。试验包括剂量递增和剂量扩展阶段,剂量递增部分针对经奥希替尼治疗后进展的、或厄洛替尼/吉非替尼/阿法替尼治疗后进展的 T790M 阴性 EGFR 突变 NSCLC 患者;
剂量扩展阶段在推荐剂量下(RDE,5.6mg/kg Q3W)分为 4 个队列,队列 1 纳入既往接受过 1 种及以上 EGFR-TKIs 和 1 种及以上铂类化疗的局部晚期或转移性 EGFR 突变 NSCLC 患者;队列 2 纳入了既往接受过铂类化疗和抗 PD-(L)1 治疗的不具备 EGFR 激活突变的鳞状和非鳞状 NSCLC 患者;队列 3 纳入 EGFR 激活突变 NSCLC 患者,1:1 分配分别接受 5.6mg/kg HER3 ADC 治疗(3a)和剂量递增 HER3 ADC 治疗(3b);队列 4 包括除混合小细胞之外的任意组织学类型 NSCLC 患者。
队列 1-3 的主要终点均为 BICR 评估的确认 ORR(cORR),次要终点包括研究者评估的 ORR、DCR、DOR、PFS、OS、安全性和药代动力学性质。
试验设计

截图来自:JSMO
Insight 数据库此前已收录这项临床试验的两条临床结果。第一三共近日发布的是队列 3a 数据,也是该队列数据的首次披露,在中位随访 23 个月(范围,11.8-36.0 个月)表现出不错的临床疗效。患者们接受前线转移性疾病系统治疗的中位治疗线数为 4(范围,1-14),中位治疗持续时间为 5.5 个月(范围,0.7-27.5 个月)。
先来一览临床结果表:
HER3 ADC 非小细胞肺癌数据
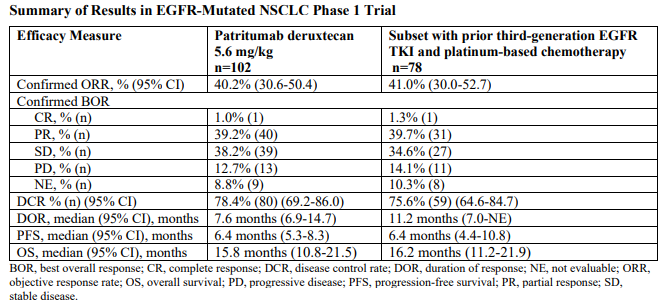
截图来自:第一三共新闻稿
具体而言,在 102 例 EGFR 突变 NSCLC 中,BICR 评估的 ORR 为 40.2%(95% CI:30.6-50.4),其中包括了 1 例完全缓解(CR)、40 例部分缓解(PR)、39 例疾病稳定(SD),疾病控制率(DCR)为 78.4%(95% CI:69.2-86.0),中位缓解持续时间(DOR)为 7.6 个月(95%CI:6.9-14.7)。中位无进展生存期(PFS)为 6.4 个月(95% CI:5.3-8.3),中位总生存(OS)为 15.8 个月(95% CI:10.8-21.5)。在亚组既往接受过三代 EGFR-TKI 和铂类化疗的 78 例患者中,疗效结果是一致的。
PFS 和 OS 数据

截图来自:JSMO
Patritumab Deruxtecan 的响应在 HER3 表达和多种 EGFR-TKI 耐药的不同机制中均有观察到,详见下图:
HER3 ADC 在不同 HER3 表达水平和 EGFR TKI 耐药机制中的响应
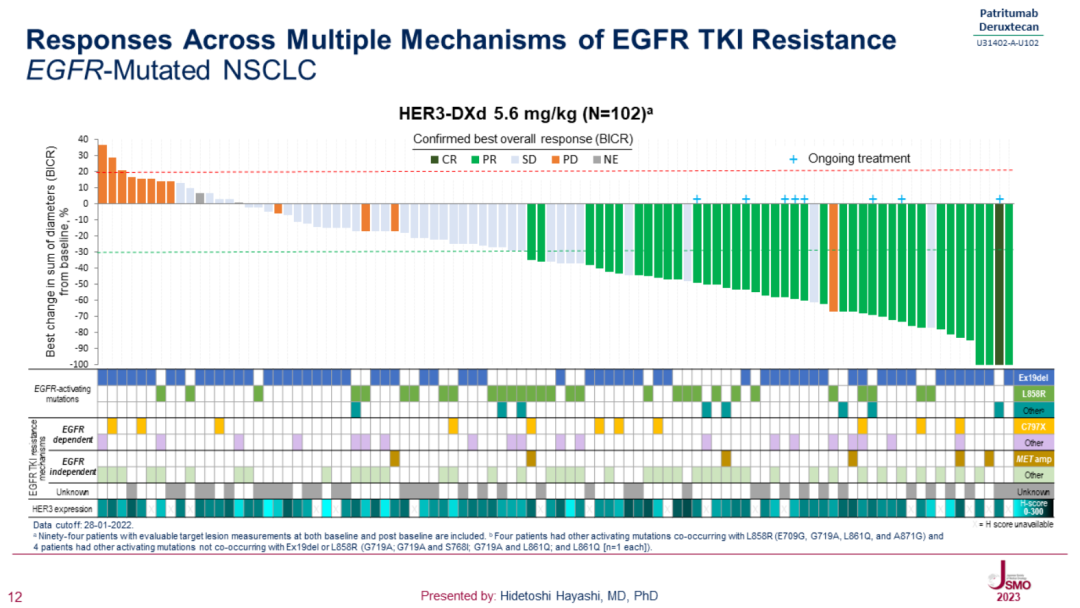
截图来自:JSMO
此外,在有或无 CNS 突变的患者中,确认的 ORR 分别为 36.4%(95%CI:23.8-50.4)和 44.7%(95%CI:30.2-59.9)。
CNS 转移患者中的响应
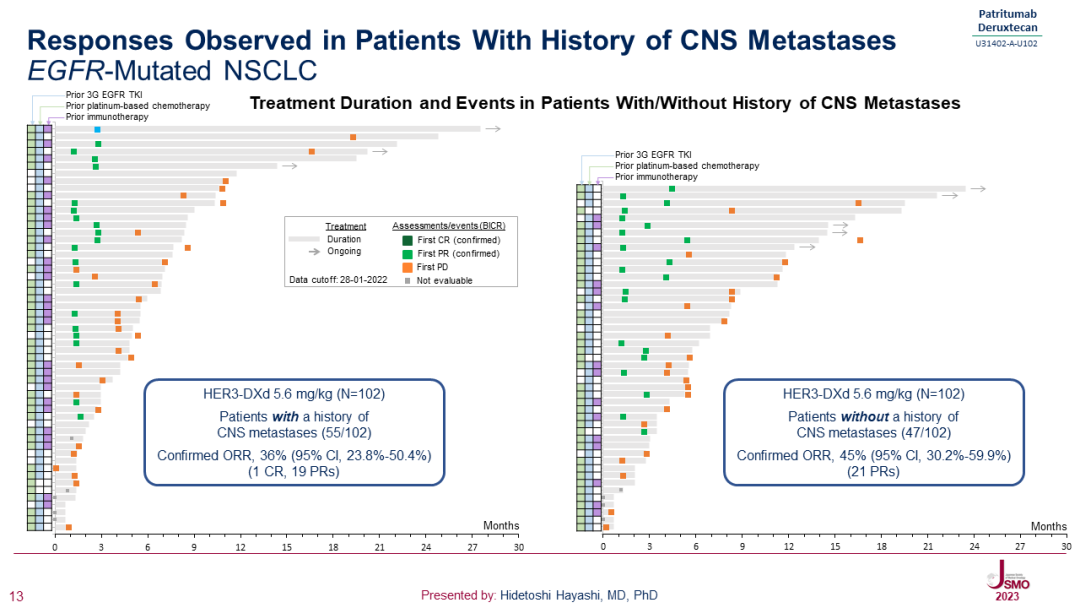
截图来自:JSMO
同一项临床试验的队列 1 和队列 2 数据分别在 2021 ASCO 和 2022 ASCO 中已经披露,这些数据也详细展现出 Patritumab Deruxtecan 对不同 EGFR-TKI 耐药机制的疗效。
曾经在 2021 年度的 ASCO 中,第一三共公布了队列 1 数据,覆盖的 EGFR-TKI 耐药患者详细突变类型涉及到 EGFR C797S 突变、MET 基因扩增、HER2 突变、BRAF 融合等。对于耐药机制为 EGFR 通路依赖性的患者和非 EGFR/MET 通路的患者,均有良好缓解,这也使该药成为了应对三代 EGFR-TKI 耐药 NSCLC 患者的潜力新星,引起广泛关注和期待。
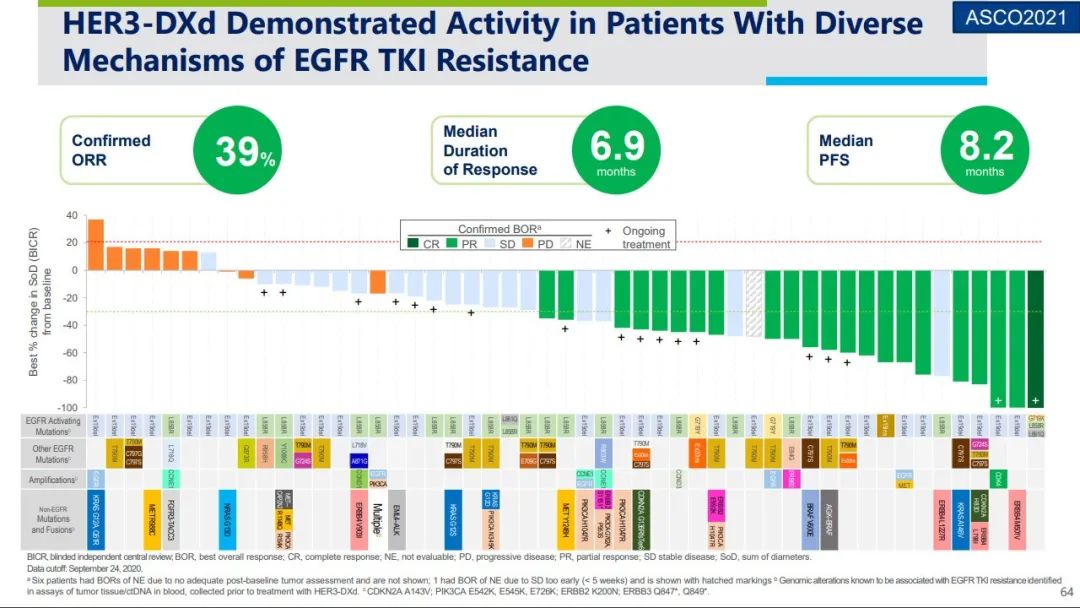
来自:2021 ASCO
在 2022 年的 ASCO 会议上,第一三共又公布了队列 2 的临床数据,这一队列在 NSCLC 患者中广泛评估了不同类型基因突变的疗效,包括 KRAS G12C/G12D 突变、EGFR 外显子 20 插入突变、RET 融合等等,U3-1402 也表现出了值得期待的疗效和可控的安全性。
U3-1402 @2022ASCO
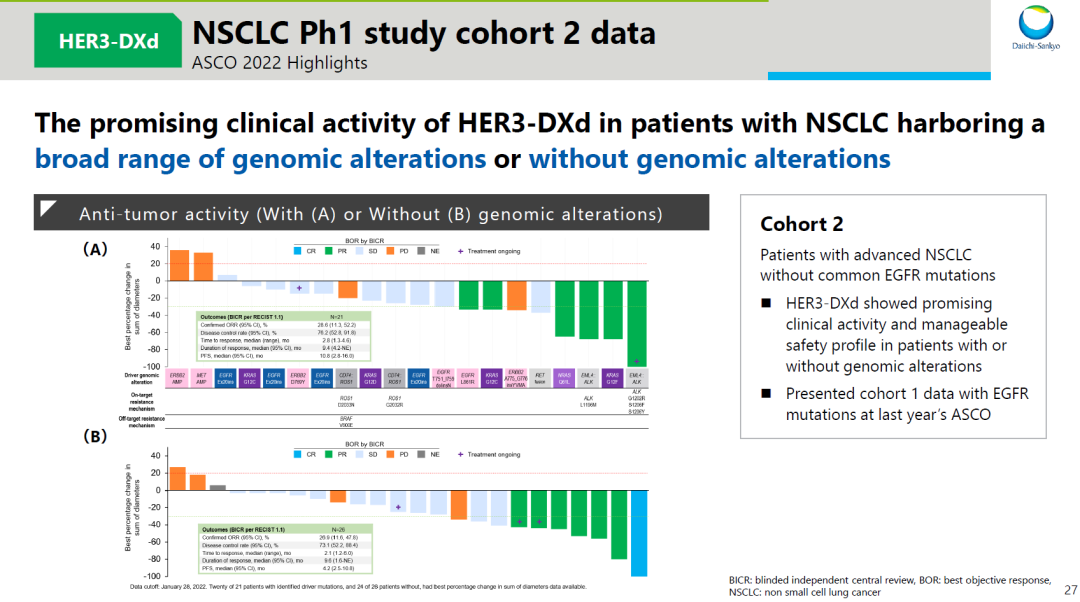
来自:2022 ASCO
潜力新星,再续辉煌
HER3 是 HER 受体酪氨酸激酶家族的成员之一,在多种类型的癌症中均有表达,包括结直肠癌、胃癌、头颈鳞癌、乳腺癌、肺癌等,其中在 NSCLC 中占 83% 之高。不光表达 HER3 的比例高,HER3 过表达与 NSCLC 癌细胞的转移及患者存活率降低有关,因此有望成为晚期、转移性 NSCLC 的新治疗手段。
U3-1402 的抗体部分为 HER3 单抗 patritumab(U3-1287),通过 linker 共价偶联拓扑异构酶 I 抑制剂依喜替康(exatecan,MAAA-1181a),每个抗体连接有 8 个依喜替康。通过与癌细胞表面的 HER3 结合,U3-1402 被内吞入细胞内释放出依喜替康,进而发挥细胞毒作用,杀灭癌细胞。
U3-1402 结构及作用机制
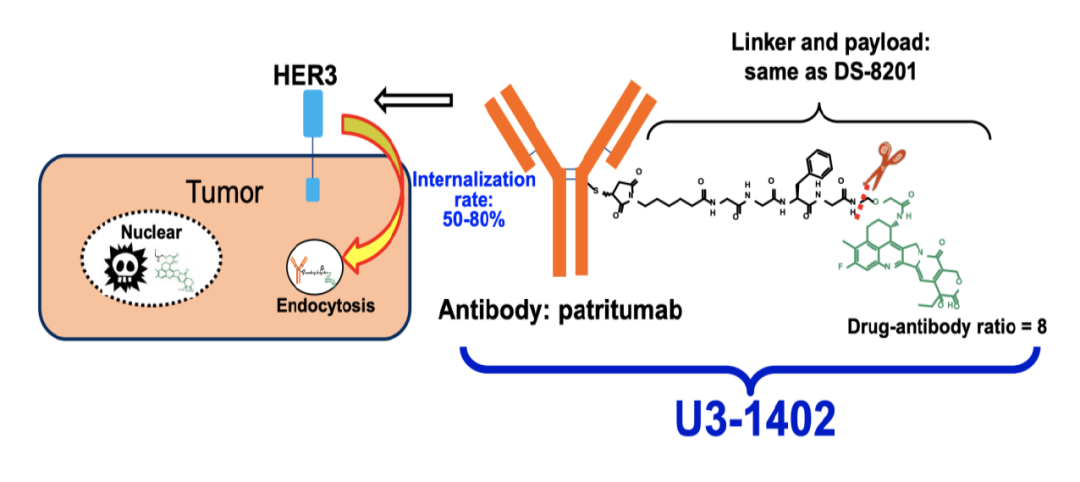
来自:第一三共官网
该药的抗体部分来自第一三共在 2008 年度收购的 U3 pharma。U3 pharma 与安进共同开发了靶向 HER3 的单抗 Patritumab,然而在收购 U3 之后,2016 年第一三共由于临床数据不佳终止了 Patritumab 项目针对 NSCLC 的研发。
不过,第一三共的 ADC 技术无疑使这个单抗重新焕发了新的生机,以 U3-1402 的形式在治疗 NSCLC 的征程上继续前行。2021 年度,U3-1402 还赢得了「最值得期待的 ADC 临床候选药」奖项。
第一三共的 HER2 ADC 德曲妥珠单抗(Enhertu)、TROP-2 ADC 德达博妥单抗(Dato-DXd)和 U3-1402(HER3-DXd)连续包揽 3 年这一 ADC 奖项,现在这 3 款 ADC 新药也是第一三共「3 and Alpha Strategy」的重要组成部分,将承托起第一三共未来在肿瘤领域的宏图。

截图来自:第一三共研发日
Insight 数据库显示,在 2016 年第一三共针对 HER3 ADC 开展的第一项临床试验并非针对 NSCLC,而是乳腺癌,次年才登记 NSCLC 临床试验。不过这款药物很快就在 NSCLC 领域展现出颇具想象力的前景,第一三共立刻加注研发,在肺癌上高速推进,如今也将成为该药率先开花结果的首发癌种。
不过,在肺癌领域的高歌猛进并不代表 HER3 ADC 放弃了乳腺癌,相应临床试验仍在扎实推进,本次 JSMO 年会上更新的数据也包括了对 HER3 阳性乳腺癌中不同 HR 和 HER2 表达状态亚组的缓解率数据。与 Enhertu 和 Dato-DXd 一起,第一三共的 ADC 管线正在广泛而细致地覆盖以 NSCLC 和乳腺癌为首癌种的各线治疗,而这两者正是全球发病和死亡 TOP2 的两个癌种,需要新治疗方案的不断涌现,满足临床需求的同时为药企带来高速增长。
HER3 ADC 开发计划

截图来自:第一三共研发日
第一三共 HER3 ADC 在乳腺癌领域迄今登记了 5 项临床试验,包括 1 项 I 期临床、1 项 I/II 期临床、3 项 II 期临床。近日更新临床试验结果的是 I/II 期临床(NCT02980341)的一项亚组数据,同登记号临床结果最早亮相于 2018 ASCO,后又在 2021 AACR 和 2022 ASCO 持续公布新数据。
在 HR 阳性亚组中,患者既往接受过中位为 7 的前线系统治疗方案;在 HR 阴性、HER2 低表达亚组中,患者既往接受中位为 4 的前线系统治疗方案;在 HR 阴性、HER2 阴性亚组中,患者的前线治疗方案中位数为 3。
试验结果清晰图表数据,可点击以下图片放大一览:
HER3 ADC 乳腺癌数据 @Insight 数据库
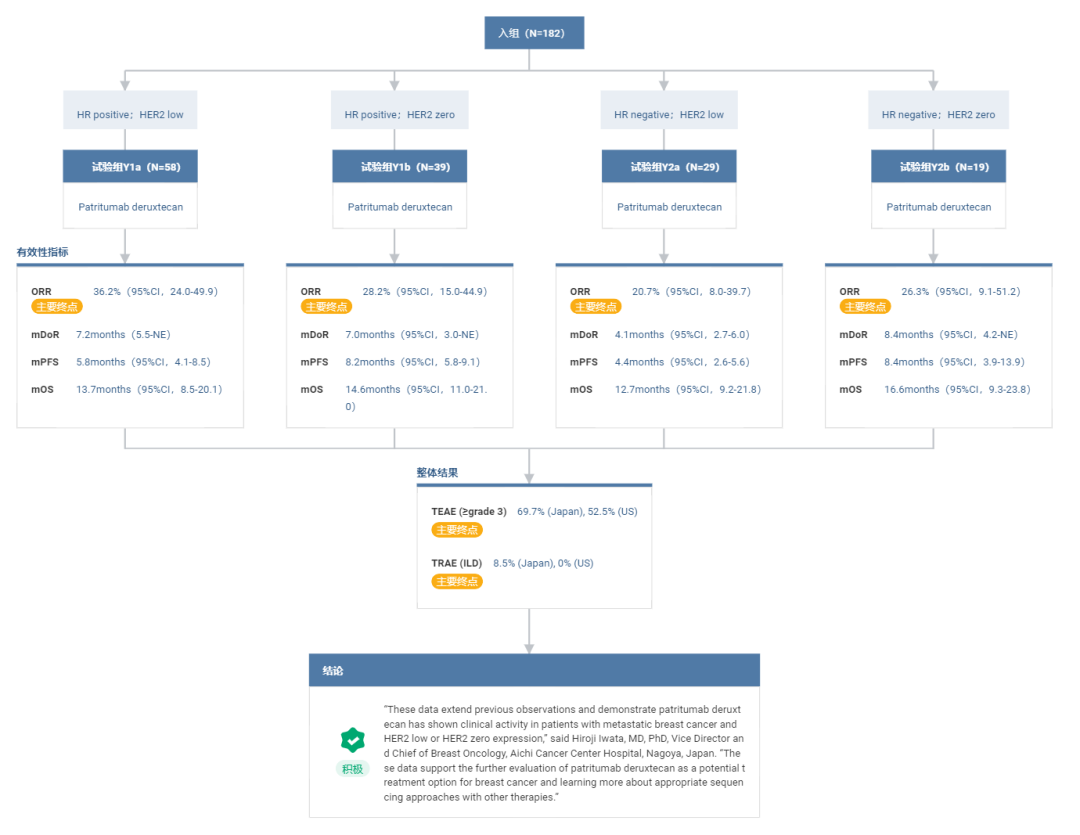
截图来自:Insight 数据库临床试验结果模块(http://db.dxy.cn/v5/home/)
在 HR 阳性乳腺癌患者中,HER2 低表达患者(n=58)的 cORR 为 36.2%(95% CI:24.0-49.9),HER2 阴性患者(n=39)的 cORR 为 28.2%(95%CI:15.0-44.9);中位缓解持续时间分别为 7.2 个月(95% CI:5.5-NE)和 7.0 个月(95% CI:3.0-NE),中位 PFS 分别为 5.8 个月 (95% CI: 4.1-8.5) 和 8.2 个月 (95% CI: 5.8-9.1),中位 OS 分别为 13.7 个月 (95% CI: 8.5- 20.1) 和 14.6 个月 (95% CI: 11.0-21.0)。
在三阴乳腺癌(即 HR 阴性亚组)患者中,HER2 低表达患者(n=29)的 cORR 为 20.7% (95% CI: 8.0-39.7),HER2 阴性患者(n=19)的 cORR 为 26.3% (95%, CI: 9.1-51.2) ;中位缓解持续时间分别为 4.1 个月(95% CI:2.7-6.0)和 8.4 个月(95% CI:4.2-NE),中位 PFS 分别为 4.4 个月 (95% CI: 2.6-5.6) 和 8.4 个月 (95% CI: 3.9-13.9),中位 OS 分别为 12.7 个月 (95% CI: 9.2-21.8) 和 16.6 个月 (95% CI: 9.3-23.8)。

 CPhI制药在线
CPhI制药在线
 2018.07.24
2018.07.24
 49675
49675

 艾美仕
艾美仕
 2018.07.09
2018.07.09
 34704
34704


 2014.03.11
2014.03.11
 31117
31117