来源:医药魔方 2016-7-7
药品审评中心(CDE)7月6日公布了新一批拟纳入优先审评的药品清单,此次共有9个受理号(涉及9个药品)上榜,全部来自外资药企。
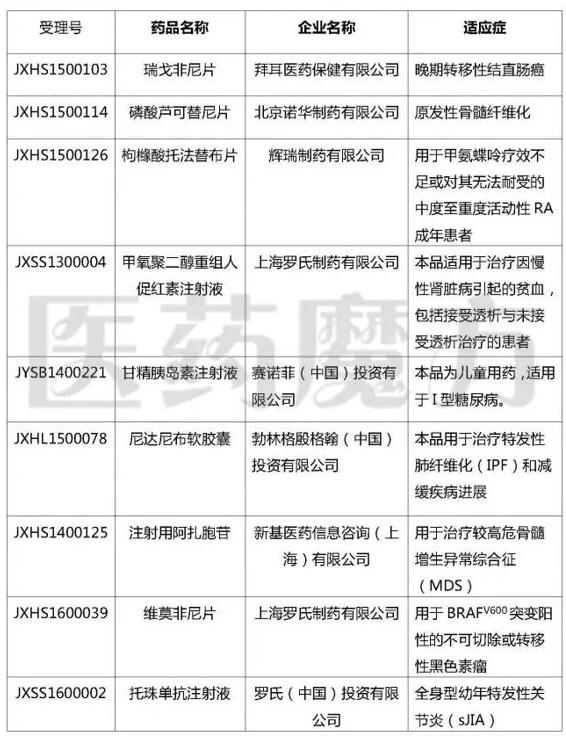
此次获得优先审评的9个注册申请中,除了勃林格殷格翰的尼达尼布软胶囊和赛诺菲的甘精胰岛素注射液之外,其他7个均为上市申请,具体信息如下:

根据总局《关于解决药品注册申请积压实行优先审评审批的意见》([2016]19号),我中心组织专家,对申请优先审评程序的药品注册申请进行了审核论证,现将拟优先审评的药物品种与申请人予以公示,公示期5日。公示期间如有异议,可按要求填写附件《药品注册申请优先审评审批品种异议表》,并反馈给我中心:wuq@cde.org.cn。
在此之前,CDE已公布过6批纳入优先审评的品种清单,具体品种及厂家信息如下:
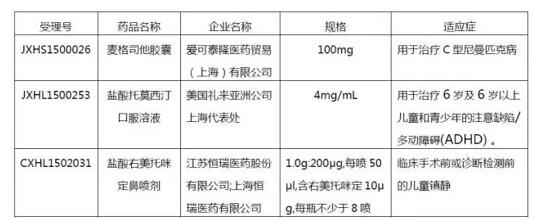
2016/1/29,CDE发布《关于临床急需儿童用药申请优先审评审批品种评定基本原则及首批优先审评品种的公告》,共有5个儿童药品种入选。
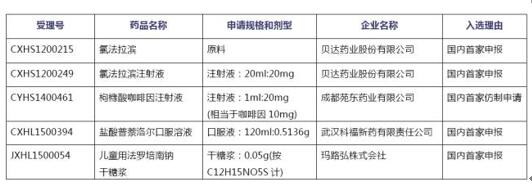
2016/3/5,CDE发布《关于首批优先审评专利到期品种和申请人的公示》,共有5个专利已到期或接近到期的具有显著临床价值的重磅品种入选。
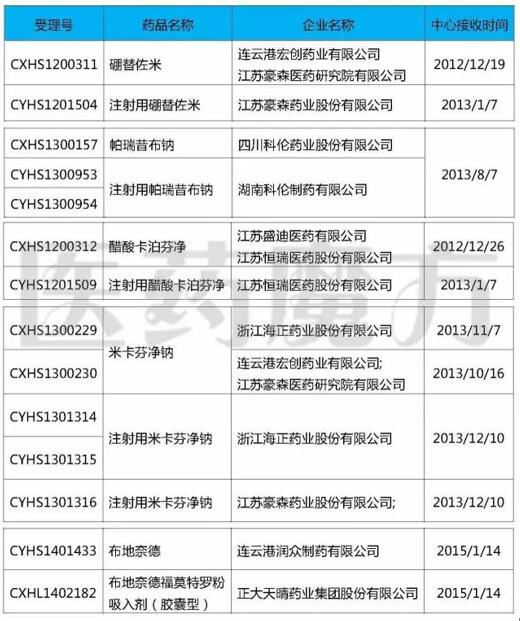
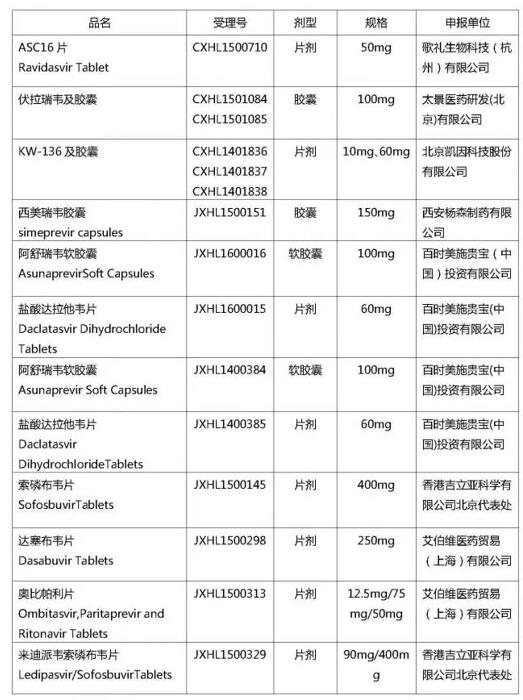
2016/4/18,CDE发布《拟纳入优先审评程序HCV药物注册申请的公示》,共有12个丙肝药物入选。
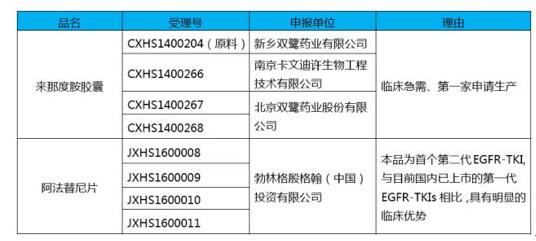
2016/4/24日,CDE发布《拟纳入优先审评程序抗肿瘤药物注册申请的公示》,此次共有2个肿瘤药入选,均为上市申请,万众瞩目的来那度胺也被列入其中。
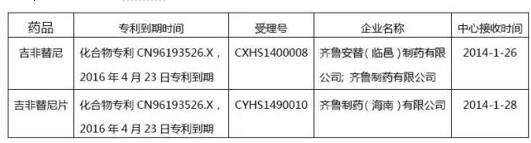
2016/4/28日,CDE发布《拟纳入优先审评程序药品注册申请的公示》,此次主要针对齐鲁首家申报的吉非替尼片的注册申请。
2016/6/12日,CDE发布新一批《拟纳入优先审评程序药品注册申请的公示》,又将3个儿童用药纳入优先审评。