来源:新康界 2016-06-17
优先审评政策推进快
据了解,去年就有4次关于重大新药创制科技重大专项拟推荐优先审评药物品种的共识,共有67个药品被推荐为优先审评品种。
创新是一个行业持续发展的根本动力。对于中国医药行业来说,无论是推动行业发展,还是满足不断提高的公众用药安全及质量需求,都必须依靠创制新药。为了鼓励新药创制,2009年初,当时的SFDA开始实施《药品注册特殊审批管理规定》,对四种类别新药实行特殊审批。
这四种情形包括,一是没有在国内上市销售的从植物、动物、矿物质中提取的有效成分及其制剂,以及新发现的药材及其制剂;二是没有在国内外获准上市的化学原料药和制剂以及生物制品,三是治疗艾滋病、恶性肿瘤、罕见病等疾病,并具有明显临床疗效优势的新药;四是目前尚没有治疗手段的新药。
而为解决药品注册申请积压的问题,国务院以及CFDA高度重视,近两年陆续发布了不少文件,于2015年11月13日发布有关优先审评审批的征求意见稿,而在随后的2016年2月,国家食品药品监管总局就发布了《总局关于解决药品注册申请积压实行优先审评审批的意见》(以下简称“意见”),目的为加强药品注册管理,加快具有临床价值的新药和临床急需仿制药的研发上市,解决药品注册申请积压的矛盾。
同时,在3月11日,CFDA公布了《首批优先审评专利到期品种和申请人名单》,其中涉及5个专利到期品种,值得业界关注。入选的优先审评企业都是国内的研发大户,其中包括恒瑞、豪森、正大天晴、科伦等,凸显出强者恒强的态势。
对于国内制药而言,纳入优先审评审批意义非凡,不仅能够获得政策的支持,先人一步上市。另一方面,对市场开发,有国家背书其疗效好于市场,便于更好地开发市场。据了解,优先审评的审评时间为6个月,而标准审评时间是11个月,随着国家在解决审评积压方面的力度加大,未来必然会走向一个快速审评的阶段,而时间更短的优先审评品种,必然会更早拿到市场的红利。
已纳入名单有何玄机
而在今年,到目前为止,CFDA已经公布拟纳入和已经纳入优先审批品种就有6次,其中已经纳入的2批次,拟纳入的4批次。在已经纳入的两批次中,儿童用药有5个品种,专利到期6个品种。
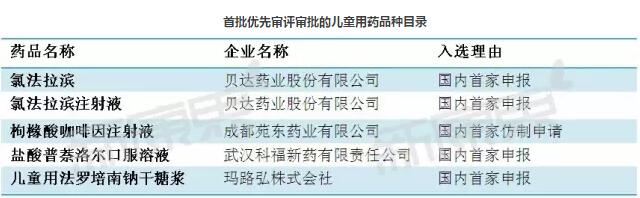
首批优先审评审批的儿童用药品种目录
首批优先审评审批的儿童用药品种目录是今年1月29日公布的,除了一家是外资以外,其余都是本土企业品种。与去年年底公布的申请名单相比,正式公布的少了5个品种。例如扬州市三药制药有限公司的左乙拉西坦口服溶液和广州一品红制药有限公司盐酸克林霉素棕榈酸酯颗粒已经不在正式公布名单,均属于儿童专用剂型。
根据2016年《关于临床急需儿童用药申请优先审评审批品种评定基本原则》,临床急需儿童专用药品有3种可优先审评审批:一是新增用于儿童人群品种,即创新型新药或新3类仿制药;二是改剂型或新增规格品种;三是市场短缺的仿制品种。而实际操作层面,一和三获批的可能性更高。
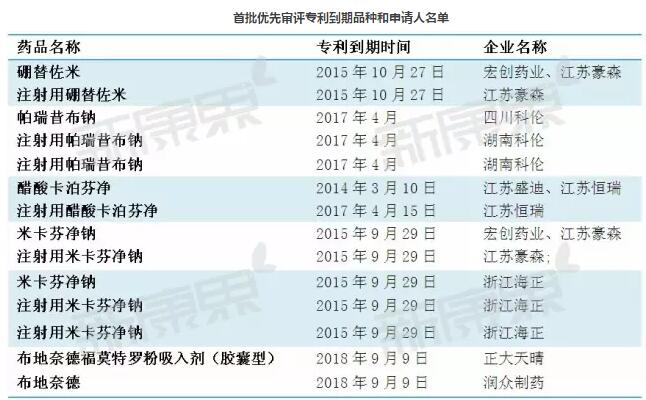
首批优先审评专利到期品种和申请人名单
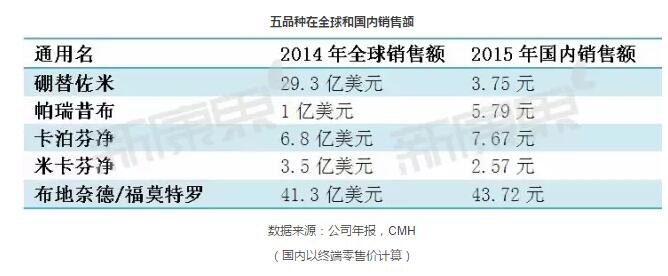
从专利过期品种来看,3月5日公布的优先审评品种多为具有显著临床价值的重磅品种。据全球畅销药销售数据统计,5个品种2014年全球销售额分别是:阿斯利康/安斯泰来的布地奈德/福莫特罗41.3亿美元,强生/武田公司硼替佐米29.3亿美元,默沙东卡泊芬净6.8亿美元,日本藤泽米卡芬净3.5亿美元,帕瑞昔布销售额为1亿美元。其中,布地奈德/福莫特罗、硼替佐米两个产品近五年市场增速较快,卡泊芬净、米卡芬净市场发展较为平稳。 而从国内来看,上述品种销售额均过亿,其中布地奈德/福莫特罗的销售额高达43.72亿元。
五品种在全球和国内销售额
拟纳入名单强调 临床优势和急需品种
在从今年拟纳入的优先审评名单来看,今年以来公布的四个批次总共有19个品种,其中仅有6个为本土品种,其余均为外资申报品种。而从治疗领域来看,涉及的领域包括丙肝、肿瘤和部分儿童疾病。基本上遵循了优先审评审批原则:创新药、短缺药、肝炎、恶性肿瘤、罕见病等享有绿色通道。
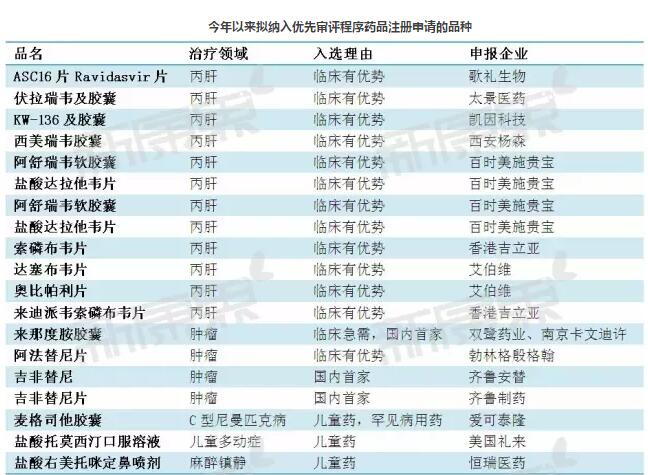
今年以来拟纳入优先审评程序药品注册申请的品种
对比上面的专利到期优先审评审批,显然在拟纳入的优先审评品种中,外资占据了绝对优势,这也从侧面反映出我国的创新药物开发与外资的差距十分明显。当然,我们看到部分国内企业,如哥礼生物、恒瑞医药、齐鲁制药等企业正在迎头赶上。
对于上述拟纳入品种,由于都是临床急需或者与现有药物相比有明显优势,例如丙肝新药一次性就有12个企业申报,得益于国际上丙肝治疗领域的重大突破,市场一片火热,而国内又缺乏疗效确切的药物,这些丙肝新药一旦纳入优先审评,将会加快我国丙肝治疗用药领域的极大发展。不过,由于申报企业众多,竞争在所难免,大家只能拼速度,谁先抢先上市,谁就能取得市场先机。
儿童用药一直是国内制药企业的软肋,多年来由于成本和收益不对等,国内企业研发兴趣淡薄,自从去年以来国家发布多项鼓励政策,企业申报的积极性明显提高,相信在未来,儿童用药市场将会更加红火。当然,由于儿童用药试验要求比较高,门槛自然也高,目前国内更多心思还是局限于在首仿国外的品种上面。