11月20日,上海复星医药(集团)股份有限公司发布公告,称其控股子公司重庆药友制药有限责任公司(以下简称“重庆药友”)近日收到国家药品监督管理局颁发的关于盐酸克林霉素胶囊(以下简称“该药品”)的《药品补充申请批件》(批件号:2018B04085、2018B04086),该药品通过仿制药一致性评价。复星集团对该药一致性评价投入研发费用人民币约655万元(未经审计)。
该药品的基本情况
药品名称:盐酸克林霉素胶囊
剂型:胶囊剂
规格:按C18H33ClN2O5S计75mg、150mg
注册分类:化学药品
药品生产企业:重庆药友
原批准文号:国药准字H50020508、H50020507审批结论:通过仿制药质量和疗效一致性评价
规格0.15g的盐酸克林霉素胶囊为289目录品种,据药智数据,目前该药按照一致性评价申报的受理号有7个,涉及5家企业,重庆药友率先审批完毕,成为首家过一致性评价企业。
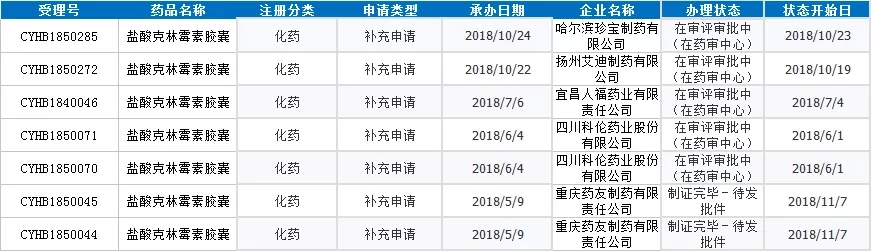
数据来源:药智药品注册与受理数据库
据药智一致性评价进度数据库,除了申报的5家企业,还有山东方明药业集团、石药集团欧意药业2家完成了BE,5家企业正在开展BE。
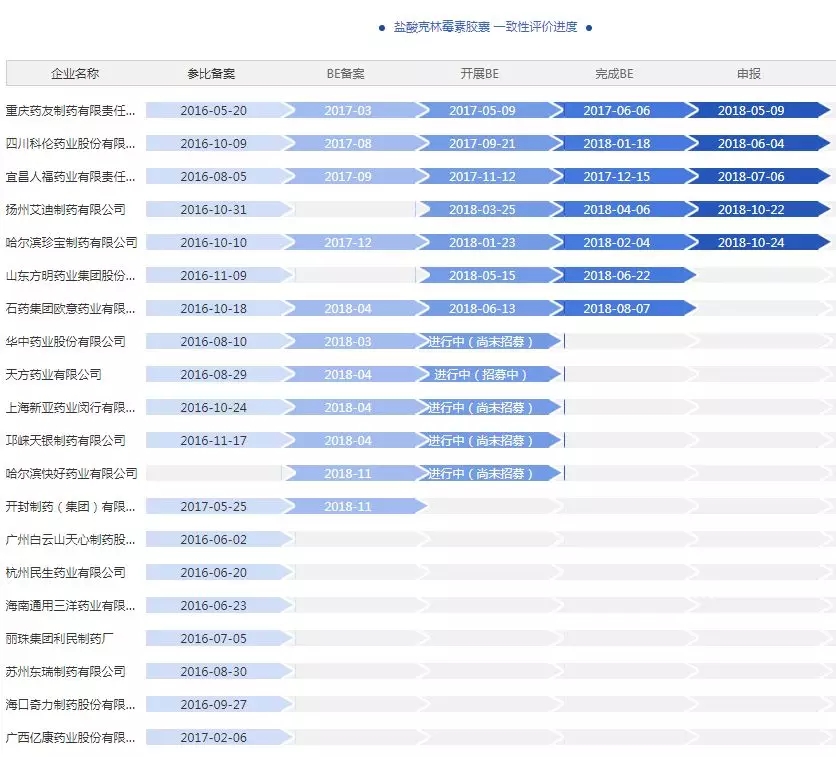
数据来源:药智一致性评价进度数据库
盐酸克林霉素胶囊为抗感染药物,主要适用于由链球菌属、葡萄球菌属及厌氧菌等敏感菌株所致的感染。根据IQVIACHPA最新数据,2017年度,克林霉素制剂于中国境内销售额约为人民币11.3亿元。