来源:丁香园 2015-12-07
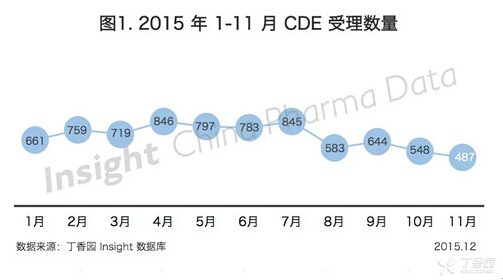
根据丁香园 Insight -China Pharma Data 数据库最新统计, 2015 年 11 月 CDE 共承办新的药品注册申请有 487 个(以受理号计,下同)。
受到 11 月 11 日发布的 230 号公告和临床自查核查结果影响,11 月份申请数量持续降低,再创 2015 年最低申报纪录。
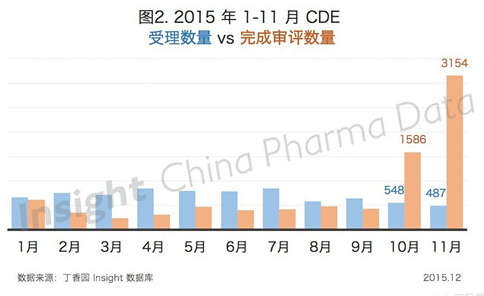
从审评进度来看,11 月 CDE 效率大增,共完成了 3154 个受理的审评。
以下,分别来分析 11 月化药、中药、生物制品的申报受理及审评审批情况。
一、化药
化药申报受理情况
11 月份 CDE 共承办新的化药注册申请以受理号计 403 个,与 10 月份相比降低了 15%,其中各个申请类型的具体数据如下所示:
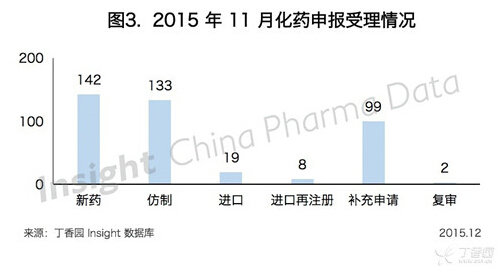
1、新药
1.1 类新药
百济神州申报 1.1 类 PARP 抑制剂 BGB-290
根据 Insight 数据库统计,11 月份 CDE 共承办化药 1.1 类新药申请以受理号计有 24 个,涉及 9 个品种,均为临床申请。具体数据如下所示:
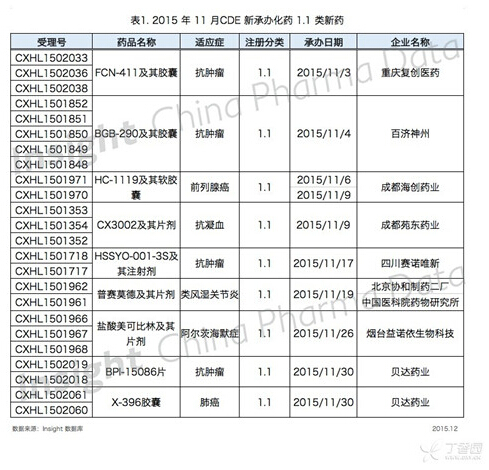
FCN-411 胶囊由复星医药子公司重庆复创医药申报,该药主要通过抑制肿瘤细胞表面受体酪氨酸激酶活性,阻断下游信号通路,抑制肿瘤细胞生长存活,从而达到肿瘤治疗的效果。
刚于 10 月提交了 IPO 申请的百济神州, 11 月申报了 1.1 类新药 PARP 抑制剂 BGB-290。BGB-290 百济神州与默克雪兰诺合作的抗肿瘤药物之一,百济神州已获得 900 万美元的里程碑款,目前该药正在美国进行 Ⅰ 期临床试验。
成都海创药业自主研发的 1.1 类新药 HC-1119 适应症为前列腺癌,该项目有成都市科技计划项目的支持。
成都苑东药业的 CX3002 是一种 Xa 因子抑制剂,适应症为抗凝血。CX3002 入选了 2016 年重大专项立项课题,但最终结果还未揭晓。
四川恒康发展集团子公司四川赛诺唯新申报了 1.1 类新药 HSSYO-001-3S,该药是喜树碱类半合成药物。最初 HSSYO-001-3S 由美国 Threshold 公司研发,其前期研发数据显示 HSSYO-001 有良好的抗肿瘤活性和安全性,2013 年四川赛诺唯新引进后继续开发。
中国医科院药物研究所和北京协和制药二厂联合申报了 1.1 类新药普赛莫德,用于治疗类风湿关节炎,11 月该药被国家卫计委拟推荐为优先审评药品。
盐酸美可比林是烟台益诺依生物科技与江苏先声药业有限公司、江苏欧威医药有限公司联合申报 1.1 类新药,用于治疗阿尔茨海默症,该药通过抑制乙酰胆碱酯酶活性及 tau 蛋白过度磷酸化来延缓疾病进程。
除了拥有埃克替尼以外,贝达药业也在积极开拓其他新产品。11 月贝达药业又申报了两个新药 BPI-15086 和 X-396。BPI-15086 是针对 EGFR T790M 突变的抑制剂,X-396 是 ALK 抑制剂,适应症为肺癌。其中,X-396 为美国 Xcovery 公司的研发项目,贝达药业投资 2000 万美元股权后,获得了 X-396 在中国的开发权。
3.1 类新药
北京康立、徐州万邦分别抢仿依匹哌唑和硫酸沃拉帕沙
11 月份 CDE 共承办新的化药 3.1 类新药申请以受理号计有 97 个。 其中,临床申请有 90 个,涉及 39 个品种;上市申请 7 个,涉及 4 个品种。
根据 Insight 数据库的潜力品种筛选系统,筛选出 2 个在国内首次申报 3.1 类新药的品种,它们未来或有可能成为国内首仿。具体数据如下所示:
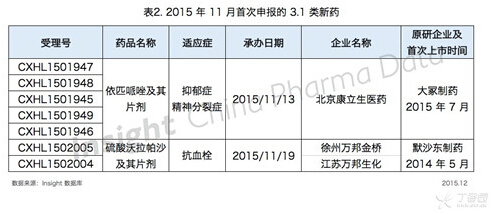
2、仿制药
11 月份,CDE 共承办化药仿制药新申请以受理号计有 133 个,涉及 81 个品种,申报数量稍有下降。
3、进口化药
拜耳国内首次申报 Vilaprisan 临床
11 月份 CDE 共承办新的化药进口注册申请以受理号计有 19 个,仅为 10 月进口化药申报量的一半,也是 2015 年进口化药申报量最少的一个月。
其中,临床申请有 14 个,上市申请有 5 个,所有申请共涉及 16 个品种。
其中,首次在中国申报的进口化药数据如下所示:
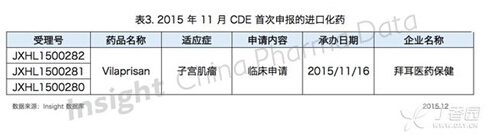
化药审批情况
1、总体审批情况
CDE 完成审评 3154 个,不批准 322 个,撤回 178 个
Insight 数据库显示,11 月 CDE 完成审评共 3154 个,加上 11 月 26 日公布的 164 个主动撤回的受理号,共 3371 个受理号完成审评。
其中,化药占了 94.17%,化药的审评结论分布如下:
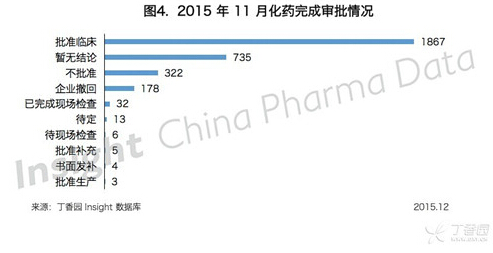
不批准的受理涉及诺华、西安杨森、辉瑞等多家外企的临床申请,也涉及江苏恒瑞、北京福瑞康正、齐鲁制药等多家企业。
撤回的受理中,浙江华海撤回了 8 个品种,损失 3800 万美元。其他撤回的企业还包括苏州二叶、陕西量子高科药业、海南双成药业等共 50 家企业。
2、1.1 类新药审批
郑州大学获得布罗佐喷钠临床批件,4500 万元转让给浙江奥翔药业
根据 Insight 数据库统计,获批临床的 1.1 类新药共有 5 个,涉及 11 个受理号。
从 11 月获批临床的审评时限来看,郑州大学的注射用布罗佐喷钠用时最短,仅 8 个月获批临床。与此同时,郑州大学以 4500 万元的价格转让给了浙江奥翔药业有限公司。
具体数据如下所示:
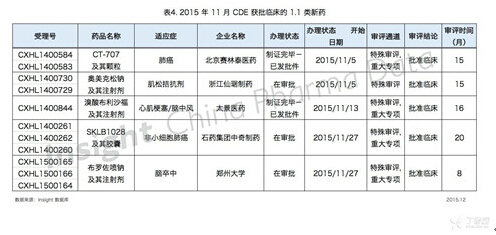
3、3.1 类新药审批
3.1 类新药中,批准临床占 78.50%,不批准占 7.20%
根据 Insight 数据库统计,11 月份 CDE 完成 3.1 类新药审评以受理号计有 805 个,其中,批准临床占了 78.5%,不批准占了 7.2%。
三、生物制品
百济神州提交 PD-1 药物 BGB-A317 临床申请
11 月份 CDE 共承办生物制品新申请以受理号计有 53 个,具体申报情况如下所示:
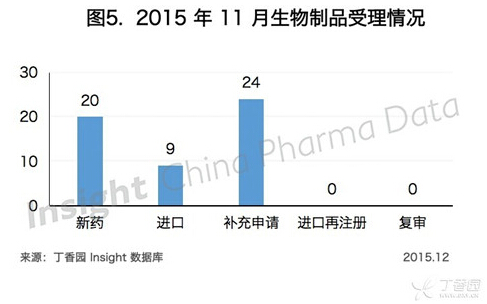
除了 1.1 类化药以外,百济神州 11 月还申报了 PD-1 抑制剂 BGB-A317。目前 BGB-A317 在美国进行一期临床试验,6 月份入组了第一位患者。Insight 数据库显示,BGB-A317 是第 7 个在中国申报临床的抗 PD-1 / PD-L1 药物。