 产业资讯
产业资讯
 药渡Daily
药渡Daily  2022-12-13
2022-12-13
 2176
2176
1 全球新药研发进展
2022.11.26-12.02这一周,全球新药研发各个领域均有新的突破,包括:肿瘤、精神、神经、消化系统、心血管、感染、免疫、皮肤和结缔组织疾病、内分泌系统等多个领域。其中,肿瘤等热门领域依旧同时涵盖了化学药、生物药、细胞疗法的最新研究进展。
Menarini在圣安东尼奥乳腺癌研讨会(SABCS)上公布有关Elacestrant的III期临床积极结果
2022年11月30日,Menarini和子公司Stemline在12月6日至10日举行的圣安东尼奥乳腺癌研讨会(SABCS)上公布了关于口服SERD elacestrant的III期EMERALD研究 (NCT03778931) 的积极数据。
EMERALD是一项III期注册试验,证明elacestrant与SOC内分泌单药治疗(氟维司群、来曲唑、阿那曲唑、依西美坦)相比,在所有ER+、HER2-晚期或转移性乳腺癌患者中达到主要终点,这些患者均携带ESR1突变(ESR1-mut)并且先前已经接受过CDK4/6抑制剂的系统治疗。基于先前使用CDK4/6抑制剂持续时间的EMERALD试验中对PFS结果的事后分析显示,在总患者群体和ESR1-mut患者中,elacestrant的单药疗法具有临床意义。转移性患者既往CDK4/6抑制剂持续时间增加与elacestrant组的PFS延长呈正相关,但与SOC无正相关。
Elacestrant是一种研究性选择性雌激素受体降解剂(SERD)。2018年,elacestrant获得了FDA的快速通道指定。在EMERALD之前完成的临床前研究表明,该化合物有可能用作单一药物或与其他疗法联合用于治疗乳腺癌。EMERALD III期试验是一项随机、开放标签、主动对照研究,旨在评估elacestrant作为ER+、HER2-晚期/转移性乳腺癌患者的二线或三线单药治疗的有效性。本项研究招募了478名先前接受过一线或两线内分泌治疗的患者,包括CDK4/6抑制剂。研究中的患者被随机分配接受elacestrant或研究者选择的批准的激素药物。该研究的主要终点是总体患者群体和雌激素受体1基因(ESR1)突变患者的无进展生存期(PFS)。次要终点包括对总生存期(OS)、客观缓解率(ORR)和缓解持续时间(DOR)和安全性的评估。

来源:Menarini官网
Atea宣布Bemnifosbuvir的III期SUNRISE-3临床研究已完成首例受试者入组给药
2022年11月29日,Atea宣布,Bemnifosbuvir(TA-527)III期SUNRISE-3临床演技已完成首例受试者入组给药。Bennifobuvir是基于Atea的嘌呤核苷酸前药平台开发的一种研究性口服核苷酸聚合酶抑制剂,靶向SARS-CoV-2 RNA聚合酶(nsp12)。SARS-CoV-2 RNA聚合酶(nsp12)是一种高度稳定不易突变的基因,负责SARS-CoV-2的复制和转录。Bennifobuvir具有独特的作用机制,具有由链终止(RdRp)和核苷酸转移酶(NiRAN)抑制组成的双靶点,有可能产生高抗性屏障。 体外数据证实,Bennifobuvir对已测试的变异株(包括奥密克戎亚变异株BA.4和BA.5)具有相似功效。SUNRISE-3是一项随机、双盲、安慰剂对照的全球III期试验,旨在评估Bennifobuvir和安慰剂与当地可用的标准护理(SOC)同时给药。该研究旨在招募至少1,500名轻度或中度COVID-19高风险、非住院患者,在美国、欧洲、日本和世界其他地区拥有约300个临床试验中心。患者将按1:1随机接受Bennifobuvir 550毫克,每日两次 (BID)加当地可用的SOC或安慰剂BID加当地可用的SOC,持续五天。该研究的主要终点是评估至少1,300名经Bennifobuvir单药进行支持性治疗的人群中,直到第29天的全因住院或死亡。支持性治疗和联合抗病毒人群的次要终点包括:COVID-19并发症、就诊、症状反弹/复发和病毒载量反弹。住院和死亡一直是包括美国食品和药物管理局在内的监管机构高度青睐的终点。

来源:Atea官网
2022.11.26-12.02全球新药研发进展(部分)
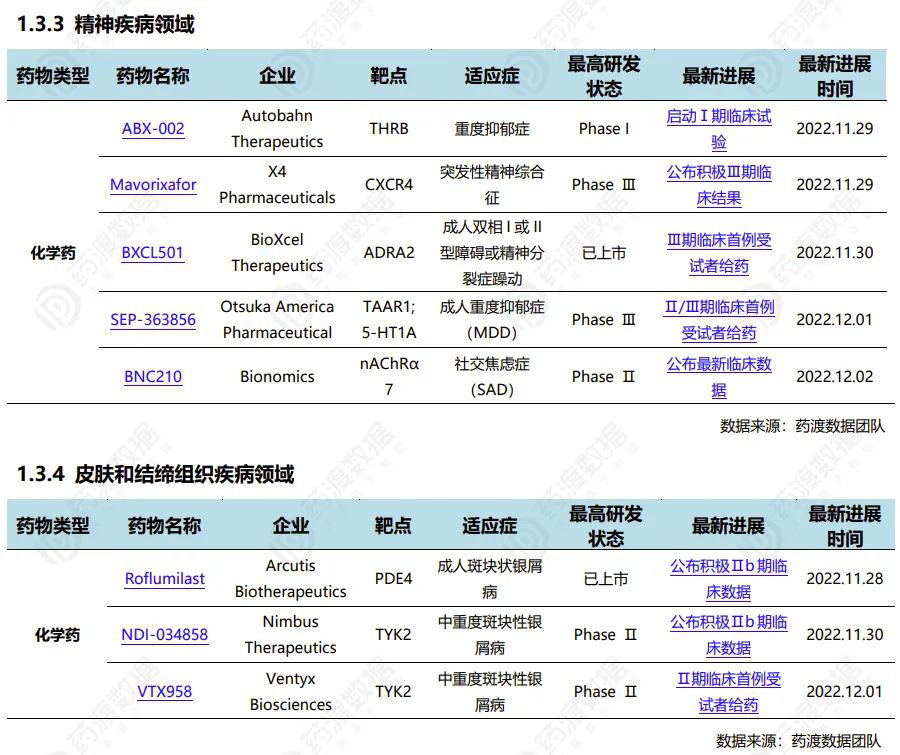
2 国内新药研发进展
2022年11月26日-12月2日,国内新药研发同样突飞猛进,治疗肿瘤的生物药进展迅速。
先声药业/南京宁丹新药宣布先必新舌下片治疗急性缺血性脑卒中III期临床达预期疗效终点
2022年12月1日,先声药业宣布,与南京宁丹新药技术有限公司合作开发的先必新舌下片治疗急性缺血性脑卒中的多中心、随机、双盲、平行、安慰剂对照的III期临床研究于近日完成数据库锁定(DBL)。先必新舌下片(前称Y-2舌下片)是一种口服固体制剂,所含依达拉奉和右莰醇两种活性成分可在舌下迅速崩解,通过舌下静脉丛吸收,进入中枢发挥抗炎、抗自由基和保护血脑屏障等药效,从而降低脑卒中引发的神经元损伤。独特的剂型有望增加卒中治疗方式的灵活性,提高用药依从性。先必新舌下片未来有望与本公司已上市的先必新®(依达拉奉右莰醇注射用浓溶液)组成序贯疗法,利于患者获得完整疗程。这项先必新舌下片注册III期临床研究由北京大学第三医院任组长单位,于全国近40家研究中心纳入发病时间≤48小时的AIS患者超900例, 旨在评价先必新舌下片治疗急性缺血性卒中患者的有效性和安全性。初步分析显示:相对于安慰剂, 先必新舌下片显著改善AIS患者治疗后神经功能恢复及独立生活能力,达到预期疗效终点, 安全性良好。本研究结果未来预计在学术期刊或医学会议上予以公布。2021年6月28日, 本研究达成首例患者入组(FPI)。其后用时仅约10个月,于2022年5月4日完成所有计划入组, 并于2022年8月完成所有患者治疗及访视。本研究的成功证实了先必新舌下片在AIS治疗中的临床价值, 有望为广大AIS患者带来新的治疗选择。
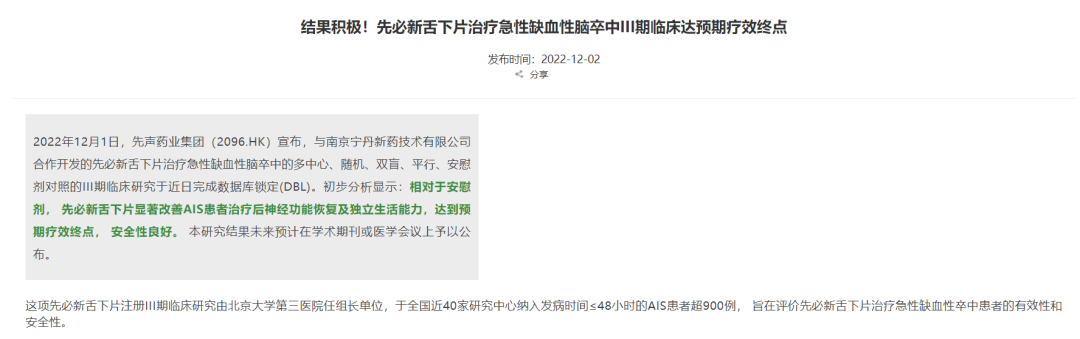
来源:先声药业官网
迈威生物在 Theranostics 发表 CD47/PD-L1 双抗临床前研究成果
2022年12月1日,迈威生物宣布,近日公司在国际期刊杂志《Theranostics》在线发表了 CD47/PD-L1 双抗 (6MW3211) 的临床前研究结果,论文题目为 “Blockade of dual immune checkpoint inhibitory signals with a CD47/PD-L1 bispecific antibody for cancer treatment”。
6MW3211是共轻链结构,采用差异化的亲和力设计,以确保优先结合到表达PD-L1的肿瘤细胞,并在此基础上发挥CD47抗体臂的阻断作用,同时活化T细胞及Macrophage的抗肿瘤作用。临床前研究显示,6MW3211完全不结合人及恒河猴的红细胞。进一步的晶体结构数据显示,CD47上的两个N-糖基化位点参与了与6MW3211的结合,提示了6MW3211对肿瘤细胞表面CD47特异性结合的结构基础。
6MW3211在Raji/NCG及hCD47/hSIRPα/hPD-L1三转基因小鼠模型上展示了很好的治疗效果,显著抑制肿瘤生长,延长小鼠生存期。体内外的功能研究结果表明,肿瘤细胞上PD-L1的表达能很大程度上提高6MW3211中CD47抗体臂的抗肿瘤效果。
恒河猴的毒理试验中,6MW3211显示了很好的安全性,在200mg/kg剂量下,未观察到任何红细胞毒性。6MW3211作用机制明确,具有很好的安全性,在动物模型上展示了显著的抗肿瘤效果,当前已推进到II期临床阶段。

来源:迈威生物官网
2022.11.26-12.02国内新药研发进展(部分)
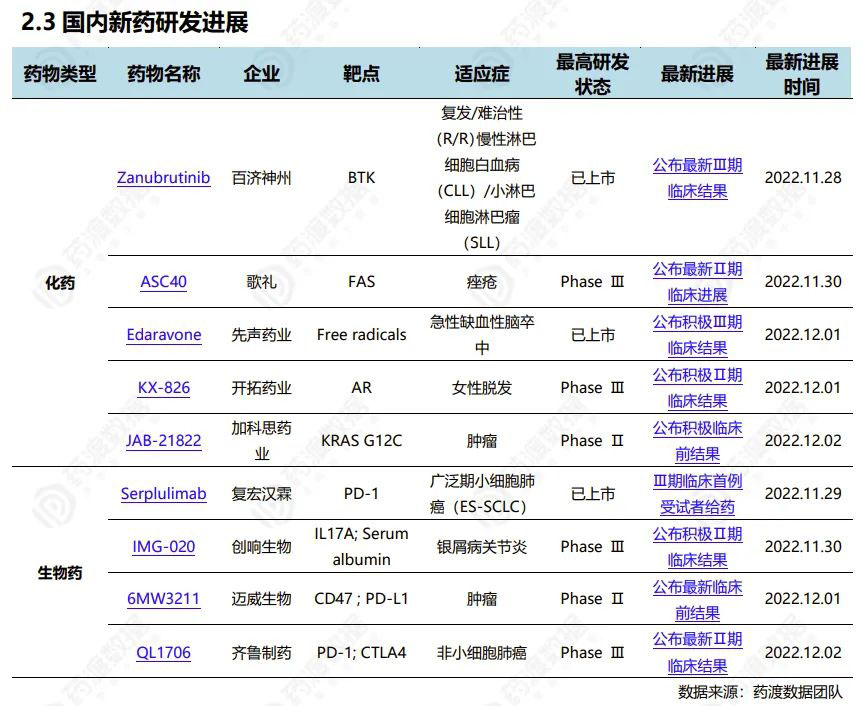
3 国内临床默示许可进展
2022.11.26-12.02临床默示许可进展(部分)
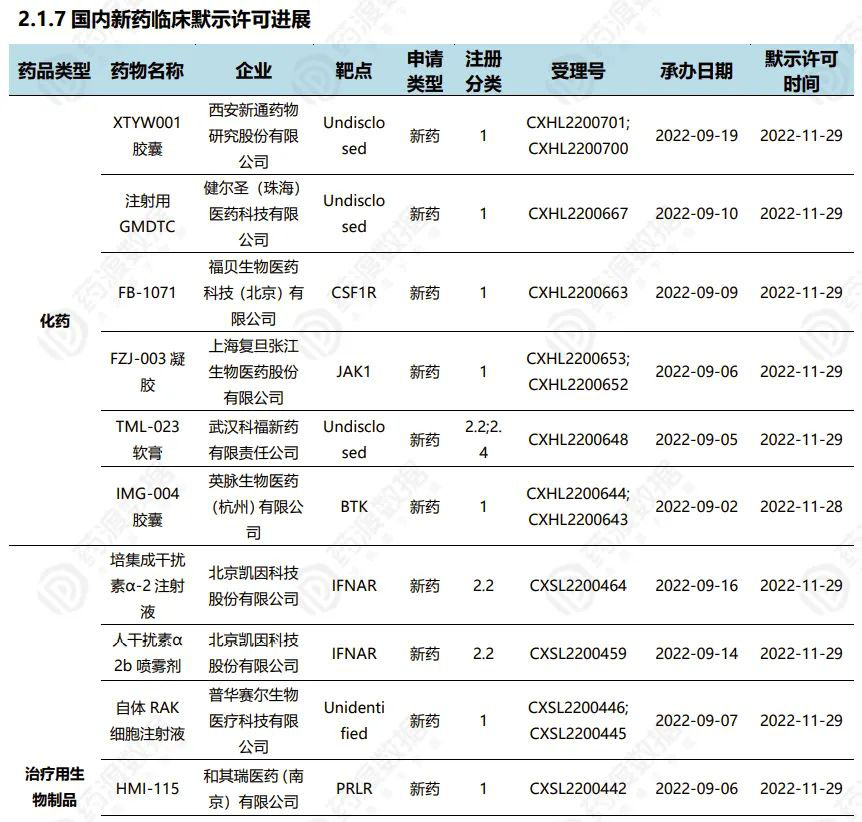
4 全球医药交易事件
Roivant和辉瑞成立合资公司Vant,专注于开发用于炎症和纤维化疾病的TL1A抗体药物
2022年12月1日,辉瑞与Roivant Sciences宣布成立一家名为Vant的新公司,专注于TL1A单抗RVT-3101(即PF-06480605)的开发和商业化,目前处于溃疡性结肠炎的IIb期开发阶段。根据协议条款,Vant拥有RVT-3101在美国和日本的商业权利。而辉瑞拥有Vant25%的股权,在美国和日本以外地区享有其商业权利,并在公司董事会中拥有代表权。此外,Vant还拥有与辉瑞合作开发下一代TL1A定向抗体的独家选择权,该抗体最近已进入第I阶段。Vant有权在第II阶段(预计在2025年)之前与辉瑞签订全球开发协议,费用平摊,共享商业化权益。RVT-3101是一种潜在的first-in-class药物,通过抑制肿瘤坏死因子样配体1A(TL1A)来阻遏炎症和纤维化途径,进而发挥疗效。

来源:辉瑞制药官网
百奥赛图与ADC Therapeutics签署抗体协议
2022年11月28日,百奥赛图宣布与总部位于瑞士的ADC Therapeutics签署具有选择权的抗体药物分子评估与授权协议。百奥赛图授权ADC Therapeutics针对百奥赛图具有自主知识产权的3个肿瘤靶点的抗体分子进行评估。在完成评估后ADC Therapeutics有权获得其所选定的抗体分子授权,在全球范围内用于ADC药物开发和商业化;百奥赛图将保留这些抗体分子用于除ADC药物以外的所有全球权益。百奥赛图将获得首付款。并且针对每个许可分子,百奥赛图将获得选择权执行费、不同阶段开发和商业化里程碑付款,累计可达数千万美元;以及个位数净销售额分成。
根据协议,百奥赛图将为ADC Therapeutics提供由百奥赛图“千鼠万抗”项目产生的针对3个肿瘤靶点的单抗或双抗分子。ADC Therapeutics将对这些抗体分子进行可行性测试;并在行使选择权后,负责进一步开发和商业化ADC产品。

来源:百奥赛图官网
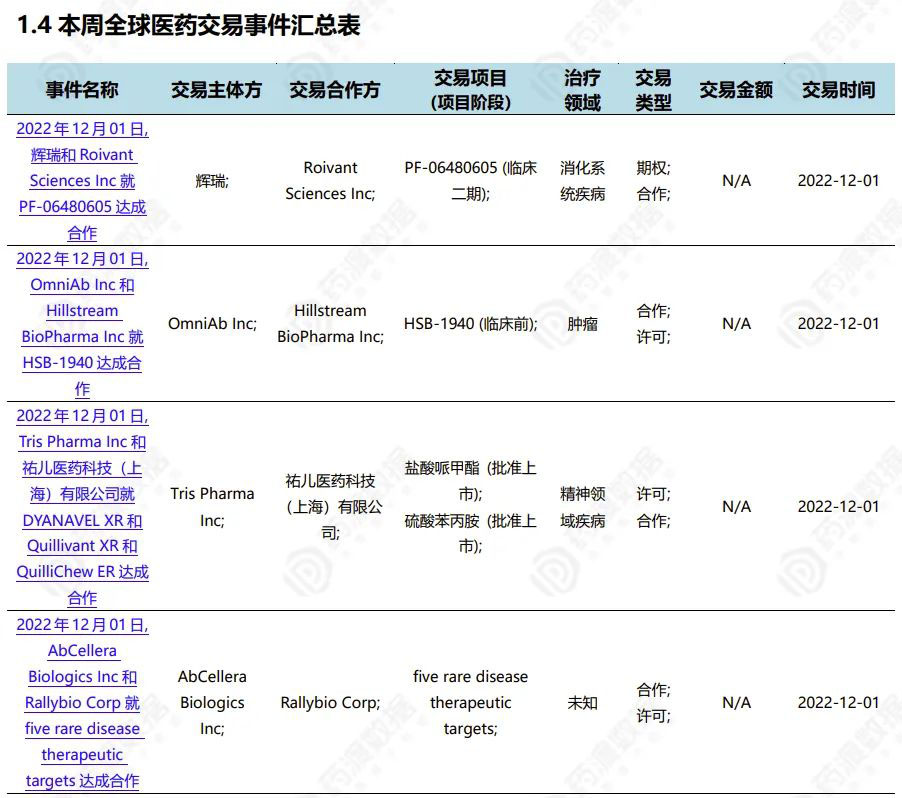
2022.11.26-12.02全球医药交易(部分)

 产业资讯
产业资讯
 医药投资部落
医药投资部落  2025-05-02
2025-05-02
 53
53

 产业资讯
产业资讯
 赛柏蓝
赛柏蓝  2025-05-02
2025-05-02
 53
53

 产业资讯
产业资讯
 瞪羚社
瞪羚社  2025-05-01
2025-05-01
 134
134