 产业资讯
产业资讯
 医药魔方
医药魔方  2023-04-11
2023-04-11
 4105
4105
自身免疫疾病是由于机体免疫系统异常而对自身抗原产生免疫反应进而导致自身机体损伤的一类疾病的总称,包括类风湿关节炎、银屑病、系统性红斑狼疮、强直性脊柱炎、溃疡性结肠炎等合计100余种细分病种[1]。据统计,自身免疫疾病影响全球约10%的人口[2],并且患病人数还以每年3%-9%的速度持续增加[3]。
庞大的患者群体和临床治疗需求推动自免疾病发展成为全球仅次于肿瘤的第二大药品市场,当前的市场规模已超过1200亿美元[4]。不过,相比肿瘤市场在全球范围内因受到众多创新药企业高度关注而形成白热化竞争的局面,自免市场当前仍算是一片蓝海。一方面,仍有诸多自免疾病亟待药物治疗手段的突破或更新,市场空间尚未打开;另一方面,自免疾病市场的全球格局极不均衡,高度集中在欧美日发达国家,包括中国在内的诸多新兴市场国家的市场潜力仍待挖掘。对于中国的创新药企业而言,自免市场毫无疑问也是一块诱人的蛋糕,但由于自免新药的研究和临床开发壁垒较高,真正全方位进军自免领域的企业较少,在这个赛道前瞻性布局的玩家更是凤毛麟角。本文简要介绍自免疾病市场的格局与现状,供业内参考。
无止境:自免疾病治疗药物持续迭代
由于人体免疫系统的复杂性,自免疾病的发病机制通常不明确,因此尚未能开发出能够彻底治愈某种自免疾病的药物。截至目前,临床上使用的自免疾病药物还是以缓解症状、延缓疾病进展、减少疾病复发和改善远期结局为主要治疗目标。
临床应用的自免疾病治疗药物
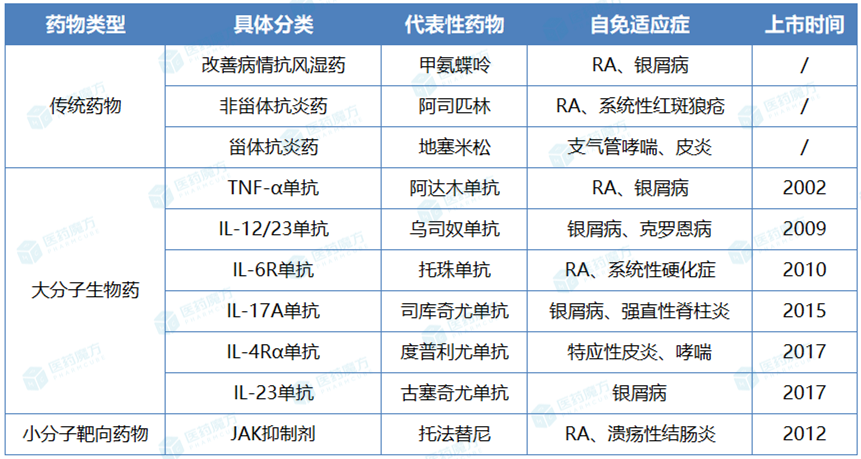
注:图中所注上市时间为药物的自免适应症在美国获批时间
在相当长的时间内,临床上治疗自免疾病的药物主要包括改善病情抗风湿药(DMARDs)、非甾体抗炎药(NSAIDs)和甾体抗炎药(SAIDs)这三类传统小分子药物。不过他们往往有各种缺陷,以至于不能满足患者需求。比如,传统DMARDs一般起效较慢,治疗类风湿关节炎(RA)的金标准药物甲氨蝶呤需使用6个月才能达到疗效峰值;非甾体抗炎药是最早用于RA的药物,可以缓解症状却不能延缓疾病进展;糖皮质激素可以快速起效,但伴随多种不良反应,停药后常会复发。显而易见,传统的自免疾病药物能给患者带来的获益比较有限。大量尚未满足的临床需求促使业界对自免病理和生物学机制进行深入探索,先后验证了TNF-α、IL-12/23、IL-17和JAK等可成药靶点,催生了多款靶向性大分子生物制剂与小分子选择性抑制剂,也培育出多款超级重磅炸弹药物。1998年,强生推出全球首款TNF-α抑制剂英夫利西单抗,起效速度秒杀传统DMARDs[5],生物制剂治疗自身免疫疾病的变革序幕由此拉开。2002年,全人源TNF-α单抗阿达木单抗(即修美乐)横空出世,以自免领域的大适应症RA为起点踏上征伐之路,凭借更小免疫原性的优势称霸市场。
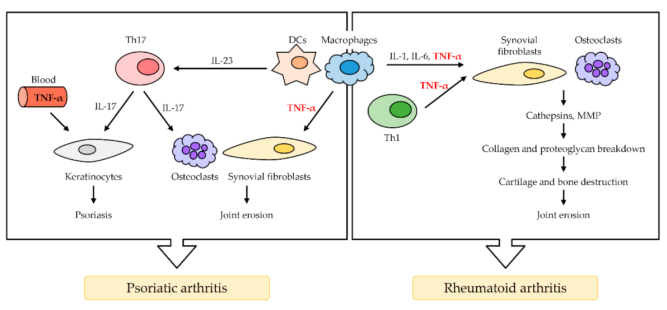
TNF-α在RA和银屑病关节炎的作用[6]
在TNF-α抑制剂席卷自免疾病领域之后,靶向白介素(IL)类促炎细胞因子及其受体的生物制剂打破了既往自免药物的疗效天花板而强势崛起,引领自免领域新一轮药物迭代浪潮。IL及其受体参与调节包括T细胞在内的各种免疫细胞的生长、分化及激活,在炎症和免疫反应过程中发挥着关键作用。强生旗下乌司奴单抗于2009年登陆美国市场,它可同时遏制银屑病核心发病机制IL-12/Th1与IL-23/Th17两条信号通路的上游信号,开创了白介素单抗用于治疗银屑病的先河。
仅1年后,罗氏开发的托珠单抗成为全球首个靶向IL-6受体的单抗药物,斩获RA适应症。对于新确诊的类风湿关节炎患者,托珠单抗展现出优于甲氨蝶呤的持续缓解效果[7]。
全球首款IL-17A单抗司库奇尤单抗则出自诺华,该产品在2015年拿到FDA的上市通行证。与IL-23相比,IL-17在IL-23/Th17信号轴中处于更下游的位置,使得司库奇尤单抗治疗银屑病起效更快[8,9]。
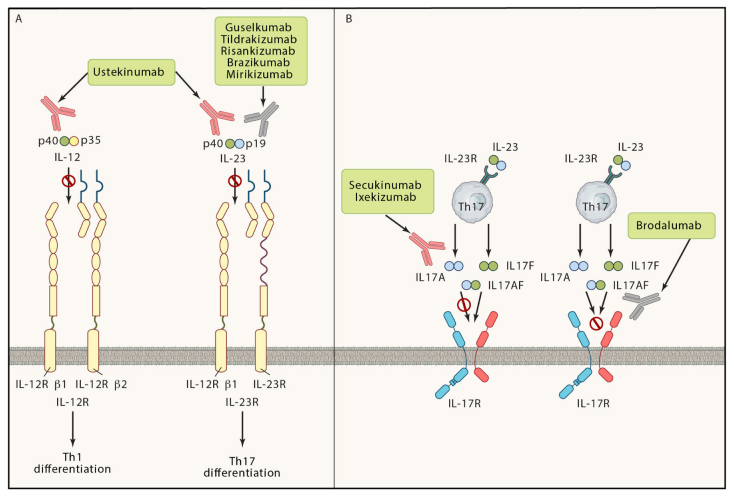
IL-17、IL-12/23和IL-23靶向生物制剂的作用机制[10]
2017年,再生元联袂赛诺菲出品的度普利尤单抗获准上市,通过挖掘Th2通路上的IL-4Rα用于治疗中重度特应性皮炎,丰富了白介素类产品阵容。近期,度普利尤单抗的III期BOREAS研究全面告捷,标志着生物制剂在慢性阻塞性肺病(COPD)领域的一个重要里程碑。同年,IL-23单抗古塞奇尤单抗问世,在阿达木单抗或司库奇尤单抗的头对头研究中彰显出更持久的疗效改善,进一步扩充银屑病治疗“武器库”[11,12]。在生物制剂占据自免药物市场主导地位的同时,以JAK抑制剂为代表的口服小分子靶向药也逐渐崭露头角。第一代JAK抑制剂中,芦可替尼稳扎稳打地拓展了白癜风和特应性皮炎的适应症,巴瑞替尼更是解锁了生物制剂未触及的斑秃领域,但它们无法选择性地抑制JAK家族的某种亚型,安全性方面时常令人担忧。以乌帕替尼为代表的第二代JAK抑制剂虽然优化提高了选择性,但安全性问题的改善仍然有限。2022年上市的TYK2抑制剂氘可来昔替尼使JAK制剂迎来转机,摆脱了FDA的黑框警告,但对于广泛人群长期应用的安全性还有待检验。
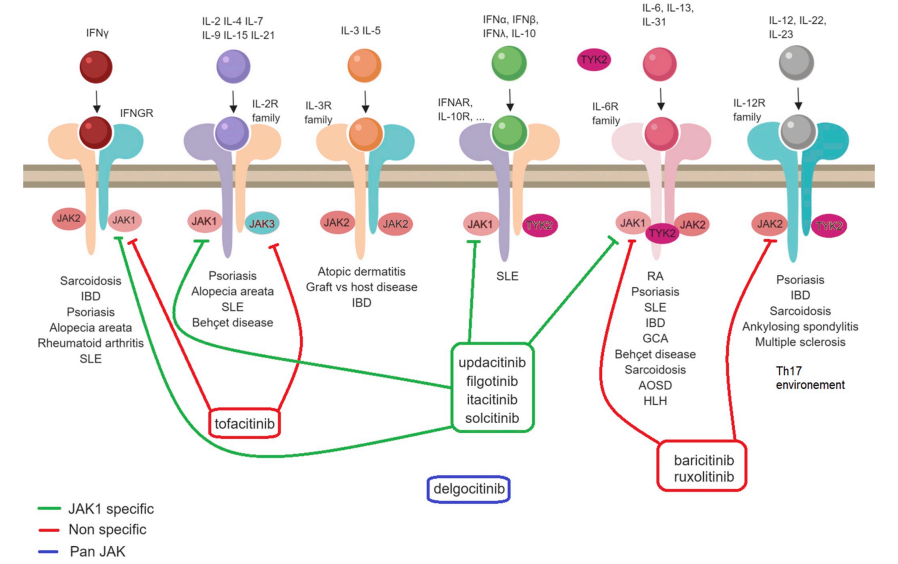
JAK抑制剂作用机制[13]
总体而言,自免领域现有的疗法仍存在较大的提升空间。从疗效上看,很多药物远没有达成颠覆性的治疗突破。比如托珠单抗治疗RA的效果虽算得上突出,第24周时ACR70(症状达到70%的缓解)应答率也达到甲氨蝶呤的两倍,但具体比值也仅有28%[14],不能实现大部分患者临床缓解的治疗目标。安全性方面,由于自免疾病病程缓慢,长期用药的安全性和耐药性是两大痛点。现有自免疗法大多通过减少免疫系统的信号传导来起效,会削减B细胞和T细胞的部分功能,增加患者的严重感染或过敏风险[15],进一步导致自免治疗依从性降低。此外,大多数传统DMARDs都会因耐药而流失疗效,生物制剂也面临同样的问题。在炎症性肠病(IBD)领域,大约有三分之一的患者对生物制剂没有响应;即便患者对于初始治疗产生响应,还是有高达半数患者会发生获得性耐药[16]。不过,凡事都有两面性,现有疗法的不完美正是未被满足的临床需求所在,这也是自免领域玩家的破局契机。
全球自免市场格局:一半海水,一半火焰
自免药物市场在全球和中国几乎是两样风景。据医药魔方数据库显示,国外已上市377款自免领域的创新疗法,而国内已上市的自免新药为117款,其中仅有21款由本土药企自研。不仅国内外的上市药物在数量上差距悬殊,市场销售表现也是冰火两重天。根据公司财报数据,2022年全球销售额超50亿美元的27个超级重磅炸弹药物中,自免药物占据7个席位,丝毫不逊色于肿瘤产品。更值得称道的是,很多制药巨头麾下的销售冠军都来自于自免领域,比如成就艾伯维的Humira(阿达木单抗),为强生扛起大旗的Stelara(乌司奴单抗),稳坐罗氏头牌的Ocrevus(奥瑞珠单抗),救赛诺菲于水火的Dupixent(度普利尤单抗)。

2022年,艾伯维、强生和罗氏等10大制药巨头在自免领域合计收获1052亿美元的销售收入。惊人的业务体量背后,蕴藏着行业巨擎们在自免领域中长久的深耕与全面的布局。不过从巨头自免业务销售收入的地域贡献上看,国内的市场的热度远远不及国外。2021年,中国自免药物市场规模约为30亿美元[4],甚至不及司库奇尤单抗一个产品全球一年的销售额。
造成中国自免药物市场冷清的原因有很多,比如:
1)自免领域的创新药品供给长期不足。即便是2016年起始的药政改革加速了创新药供给,但首要的还是推动了肿瘤新药的数量。自免领域的情况直到近两年才有明显改善,比如赛诺菲的支柱产品度普利尤单抗在中国也积极开发上市,勃林格殷格翰的IL-36受体单抗实现中美同步开发。由于之前获批上市的自免创新药有限,也就导致国内自免药物市场的空间迟迟未能打开。
2)患者用药的可及性有待改善。虽然进口自免新药的价格经过医保谈判后变得相对可及,但众多的自免患者还是分布在经济欠发达地区,支付能力很弱。自免领域药品消费升级的普及性还远不如肿瘤领域。
3)自免疾病一般进展缓慢,通常不像肿瘤会在短期内严重至危及生命,由于患者对疾病认知不充分,导致其治疗意识较薄弱和治疗依从性较差。虽然自免患者群体庞大,但经就诊率、治疗率这样层层过滤后,有效的目标患者群体数量还是会大幅降低。
4)中国自免药物市场仍以传统小分子制剂为主导,生物制剂的市场份额到2021年也仅占1/3左右[4],这与全球自免药物市场的情况截然不同,同时也是中国自免药物市场规模不大的一个因素。因此,本土药企若想在自免疾病的蓝海市场中占据一席之地,首先要加快自主研发药物的上市步伐,突破各大MNC在自免领域构筑的产品防线,尤其是生物药。其次,上市之后可以通过医保谈判实现快速市场准入,布局下沉市场,挖掘更多的存量和增量空间,提高自免新药的可及性。最后,国内自免市场的壮大需要加强医患教育和市场教育,在患者得到最佳治疗获益的同时,最大限度地实现自免新药的商业价值。
多元布局:本土药企蓄势待发
对于自免疾病这样一个充满想象力的蓝海市场,国内不少头部药企和创新药企均有涉猎,比如恒瑞医药、信达生物、康方生物和康诺亚等。在它们的管线布局中,针对主流的IL靶点开发抗体药物几乎成为必选。如果从公司整体业务看,这些玩家中较多还是采用左手肿瘤、右手免疫的双驱动模式,完全专注于自免领域的药企较为稀少。近日,来自于江苏泰州中国医药城的荃信生物向港交所递交了IPO上市申请,这是国内为数不多的专注于自免疾病业务的公司,其管线布局对于国内自免领域的玩家也颇具借鉴意义,我们将对此做进一步介绍。
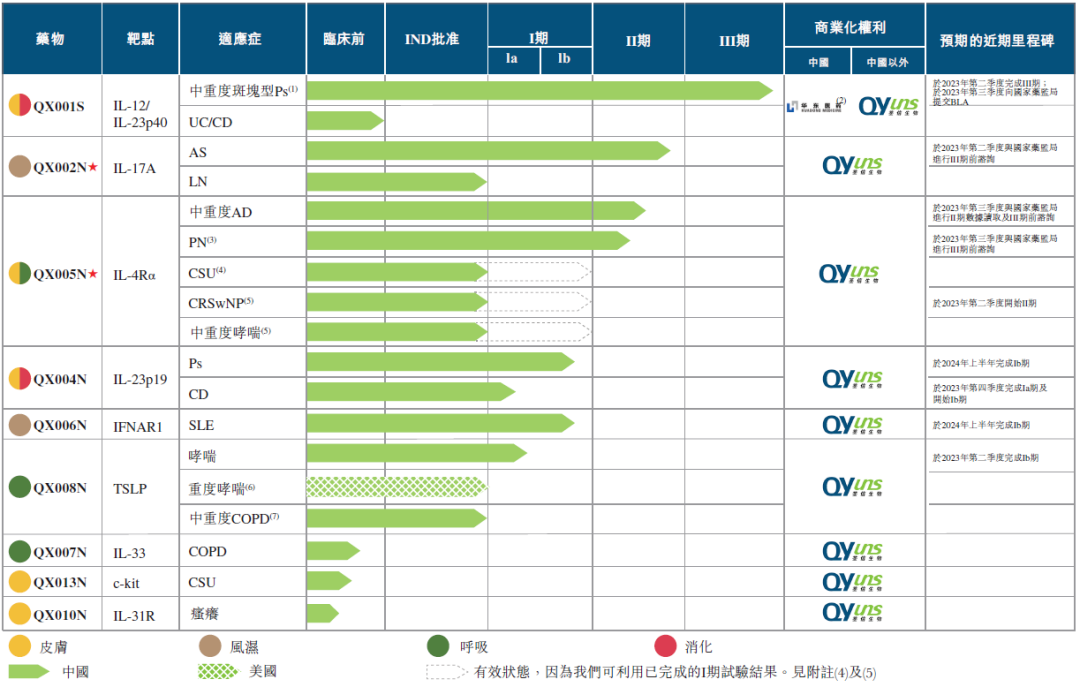
来源:荃信生物招股书
IL靶点的多元化覆盖是荃信生物管线的最大亮点。先来看生物类似药资产,IL-12/23双靶向的QX001S是荃信生物管线中进展最快的一款生物制剂,不仅获得华东医药的青睐助力商业化进程,也有望拔得头筹,成为国内首款上市的乌司奴单抗生物类似药。2022年,乌司奴单抗原研已逼近百亿美元营收。对于biotech而言,通过率先商业化生物类似药来打通自我造血能力,算是公司运营战略的上策。荃信生物在创新药上的布局更为丰富,通过IL-17A单抗QX002N、IL-23单抗QX004N、IL-4Rα单抗QX005N和IL-33单抗QX007N四款抗体,将时下最具市场确定性的IL靶点一网打尽,全面拓展强直性脊柱炎、斑块状银屑病、克罗恩病、特应性皮炎和哮喘等疾病版图。目前,IL-17A单抗QX002N和IL-4Rα单抗QX005N都已推进至II期临床阶段,QX007N有望成为首个进入临床的国产IL-33单抗。荃信生物的管线布局并不局限于IL靶点,QX006N单抗以IFNAR1靶标,发力系统性红斑狼疮。IFNAR1赛道竞跑者甚少,全球范围内仅有阿斯利康开发的Saphnelo撞线,国内布局该靶点的药企仅有两家。TSLP单抗QX008N是荃信生物在呼吸系统自免疾病领域布局的另一力作,目前仅有阿斯利康/安进首创的Tezspire攻克TSLP壁垒。细品之下,荃信生物在自免领域的差异化布局让人眼前一亮。首先,荃信生物在仿创结合之路中逐渐领跑国内IL-12/23赛道,有望凭先发优势抢占市场;其次,通过多元布局IL系列靶点,开发丰富且高度协同的自免适应症,构筑产品竞争壁垒;最后,以相对小众的IFNAR1与TSLP靶点作为自免领域的有力补充,打造产品的差异化优势。
小结
未来,肿瘤领域的内卷之势将愈演愈烈,而自免领域这块沃土的潜力尚未被完全开垦,这势必将成为中国生物制药行业的下一风口。国外自免领域的治疗迭代与成熟发展已给中国自免市场树立了鲜活的典范。目前,MNC先行一步,旗下自免产品已快速启动中国市场;而本土创新势力也不落人后,多款自免产品商业化蓄势待发,有望在不久的将来,搅动中国自免市场的格局变幻。
参考资料
[1] 全球自免协会,自免疾病清单
[2] Fan Cao, Yi-Sheng He, Yan Wang, et al. Global burden and cross-country inequalities in autoimmune diseases from 1990 to 2019. Available online 22 March 2023
[3] Global spread of autoimmune disease blamed on western diet
[4]荃信生物招股书
[5] Targan SR, Hanauer SB, van Deventer SJ, et al. A short-term study of chimeric monoclonal antibody cA2 to tumor necrosis factor alpha for Crohn's disease. Crohn's Disease cA2 Study Group. N Engl J Med 1997;337:1029-35.
[6] Jang DI, Lee AH, Shin HY, et al. The Role of Tumor Necrosis Factor Alpha (TNF-α) in Autoimmune Disease and Current TNF-α Inhibitors in Therapeutics. Int J Mol Sci. 2021 Mar 8;22(5):2719.
[7] Bijlsma JW, Welsing PM, Woodworth TG, et al. Early rheumatoid arthritis treated with tocilizumab, methotrexate, or their combination (U-Act-Early): amulticentre, randomised, double-blind, double-dummy, strategy trial. Lancet, 2016, 388(10042): 343-55.
[8] Reich K, Armstrong AW, Langley RG, Flavin S, Randazzo B, Li S, Hsu MC, Branigan P, Blauvelt A.Lancet. 2019 Sep 7;394(10201):831-839.doi: 10.1016/S0140-6736(19)31773-8.
[9] Blauvelt A, et al. Secukinumab is superior to ustekinumab in clearing skin of subjects with moderate-to-severe plaque psoriasis up to 1 year: Results from the CLEAR study. J Am Acad Dermatol, 2017, 76(1): 60-69.e69.
[10] McGeachy MJ, Cua DJ, Gaffen SL. The IL-17 Family of Cytokines in Health and Disease. Immunity. 2019 Apr 16;50(4):892-906.
[11] Blauvelt A, Papp KA, Griffiths CEM, et al. Efficacy and safety of guselkumab, an anti-interleukin-23 monoclonal antibody, compared with adalimumab for the continuous treatment of patients with moderate to severe psoriasis: Results from the phase III, double-blinded, placebo- and active comparator-controlled VOYAGE 1 trial. J Am Acad Dermatol. 2017 Mar;76(3):405-417.
[12] Reich K, Armstrong AW, Langley RG, et al. Guselkumab versus secukinumab for the treatment of moderate-to-severe psoriasis (ECLIPSE): results from a phase 3, randomised controlled trial. Lancet. 2019 Sep 7;394(10201):831-839.
[13] Jamilloux Y, El Jammal T, Vuitton L, et al. JAK inhibitors for the treatment of autoimmune and inflammatory diseases. Autoimmun Rev. 2019 Nov;18(11):102390.
[14] Scott LJ. Tocilizumab: A Review in Rheumatoid Arthritis. Drugs (2017) 77:1865–1879
[15] Immunosuppressive Medication for the Treatment of Autoimmune Disease
[16] Nilesh Lodhia and Shanti Rao.Updates in therapeutic drug monitoring in inflammatory bowel disease. World J Gastroenterol. 2022 Jun 7; 28(21): 2282–2290.
 产业资讯
产业资讯
 智药局
智药局  2025-12-15
2025-12-15
 82
82

 产业资讯
产业资讯
 Medaverse
Medaverse  2025-12-15
2025-12-15
 70
70

 产业资讯
产业资讯
 生物药大时代
生物药大时代  2025-12-15
2025-12-15
 65
65