 产业资讯
产业资讯
 招财小黄鸭
招财小黄鸭  2023-04-19
2023-04-19
 4129
4129
近日辉瑞启动了一项 PF-07817883 的 2b 期临床试验,皆在了解该药物在确诊有症状新冠感染但未住院的成年患者中的效果和安全性。临床试验设计分为四个组,分别为 100 mg,300 mg,600 mg 和安慰剂组,q12h*5d,主要终点为病毒载量变化。

PF-07817883 是一种 3CL pro 抑制剂,其结构式类似于奈玛特韦,但无需利托那韦维持血药浓度,根据目前临床试验设计推测 PF-07817883 的适应症为:用于治疗轻中度新型冠状病毒感染(COVID-19)的成年患者。
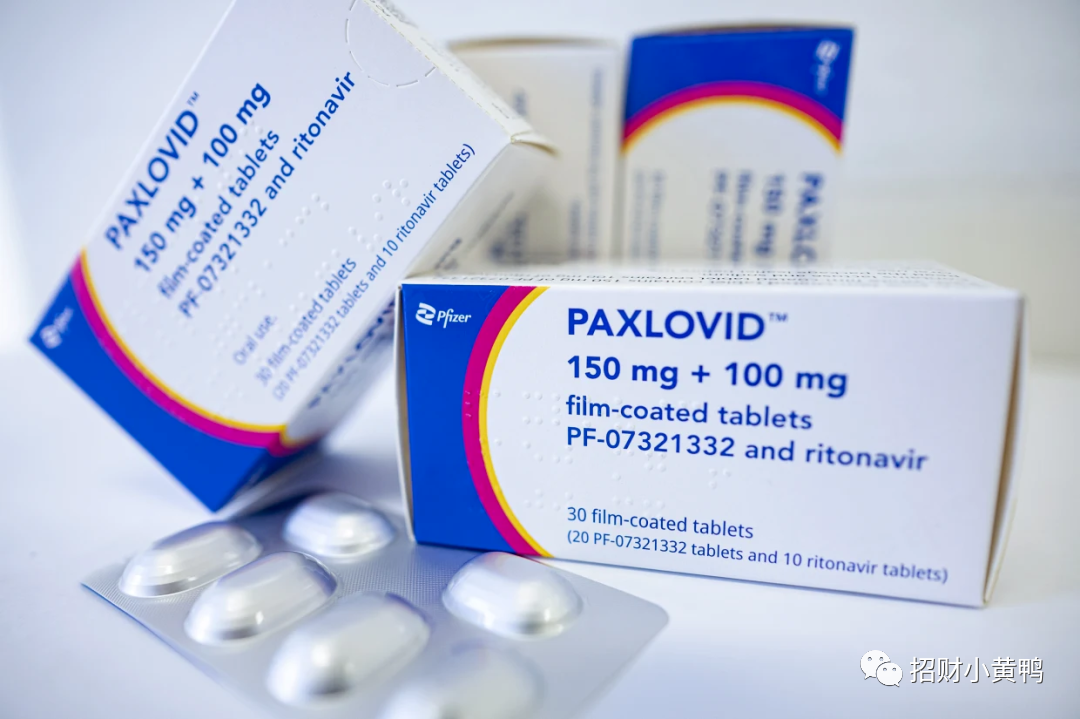
辉瑞公司的管理层则预测,Paxlovid(奈玛特韦+力拓那韦)2023年的销售额将下降到80亿美元。
在中国,辉瑞的奈玛特韦片/利托那韦片(即Paxlovid)组合包装价格下调至1790元/盒,此前该药的医保支付价格为1890元/盒,已下调100元。而且不再享受医保临时支付。
国内已有一款3CL单药上市。
3月23日,众生药业控股子公司广东众生睿创生物科技有限公司新冠口服药来瑞特韦片(商品名称:乐睿灵)获国家药监局附条件批准上市,用于治疗轻中度新型冠状病毒感染 (COVID-19)的成年患者。
来瑞特韦片只需要单药服用,不需要联合肝药酶抑制剂(CYP酶抑制剂)利托那韦。
另外,英矽智能抗新冠3CL单药临床试验申请在2月获批。
ISM3312是一款具有高选择性的3CLpro抑制剂,其新颖的分子结构是由生成化学平台Chemistry42基于冠状病毒主蛋白酶结构全新生成的化合物优化而来。与现有同靶点药物相比,ISM3312具有更广谱的抗冠状病毒活性、优秀的单药口服生物利用度、以及潜在抗临床耐药突变能力。也无需联用利托那韦。
国内获批上市的新冠口服药已达6款。其中包含辉瑞的Paxlovid和默沙东的莫诺拉韦这两款进口药物,以及真实生物的阿兹夫定片,先声药业的先诺欣和君实生物的民得维,众生药业的在内的乐睿灵。

 产业资讯
产业资讯
 医麦创新药
医麦创新药  2025-08-04
2025-08-04
 9
9

 产业资讯
产业资讯
 药时空
药时空  2025-08-04
2025-08-04
 8
8

 产业资讯
产业资讯
 Medaverse
Medaverse  2025-08-04
2025-08-04
 9
9