 产业资讯
产业资讯
 创药网
创药网  2023-11-03
2023-11-03
 4782
4782
创新药物研发最珍贵的就是首创性,其成功既可造福于患者,又能带来丰厚的市场回报。在当前国内生物医药创新发展大背景下,中国生物医药企业加快转变创新模式,越来越多的企业开始专注首创药物的研发。本文汇总了当下国内企业开发的有望成为首创的候选药物,并对这些新型治疗靶标与作用机制药物开发情况进行简要剖析。
首创(“First-in-class”)药物一般是指第一个能够治疗某个疾病的药物,被授予“First-in-class”的药物是指使用全新的、独特的作用机制来治疗某种疾病的药物,是一类彻底的创新药,在NMPA的申报当中属于1类新药。“First-in-class”药物的上市多有赖于创新、有效药物靶标的发现,也是驱动疾病疗法产生根本性突破的源头。
本文对当前国内新药研发管线的候选药物进行分析,一些已经进入临床Ⅱ期的全新靶标或作用机制药物,被认为是有望开发成为“First-in-class”药物(表1)。以下分别对这些潜力靶标及其药物研发进展进行简介。
表1:国内“First-in-class”潜力候选药物作用靶标及国内外开发情况
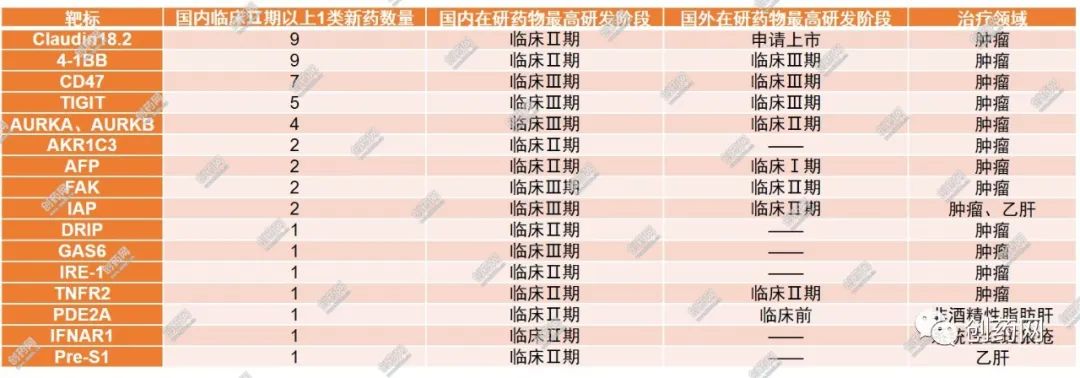
注:数据截至2023年8月17日
01 AFP
甲胎蛋白(Alpha-fetoprotein,AFP)是一种70kDa糖蛋白,类似于白蛋白,主要由肝细胞癌和胎儿干细胞等产生,其中,肝细胞癌细胞合成AFP称为肿瘤源性AFP(tumor-derived AFP,tAFP),与肝细胞癌患者肿瘤大小、分化分期和较低的生存率相关。JWATM203是药明巨诺开发的潜在同类首创以AFP为靶标治疗肝细胞癌的T细胞模拟抗体(TCRm)T细胞疗法,有潜质成为AFP阳性肝细胞癌患者的创新治疗手段。目前,药明巨诺合作伙伴优瑞科已于美国推动其AFP TCRm T细胞疗法候选产品进行临床Ⅱ期试验。此外,通过与Lyell的合作,药明巨诺还在开发另一种以AFP为靶标治疗肝细胞癌的TCRm T细胞疗法JWATM213,或将进一步加强T细胞功能并提高疗效,目前该项目处于临床前研究。北京合生基因科技有限公司研发的SynOV1.1腺病毒注射液是利用合成生物技术改造人5型腺病毒而获得一种重组溶瘤腺病毒,以AFP为启动子,主要针对AFP阳性的实体瘤患者,SynOV1.1已在美国获批临床,用于治疗包括中晚期肝癌在内的AFP阳性实体瘤,该药物最高研发阶段为临床Ⅱ期,用于治疗肝细胞癌(NCT04612504)。作为一个经典的癌蛋白,AFP是诊断原发性肝细胞癌常用而又重要的方法。AFP作为维持母胎耐受的免疫抑制蛋白被发现已经接近50年了,但是现在在肿瘤免疫中的研究并不多。国际上进展最快的AFP调节剂HLA-A24 AFP是由Adaptimmune公司研发的一种TCR细胞疗法和基因疗法,目前治疗肝癌处于临床Ⅰ期阶段。
02 FAK
局部粘着斑激酶(Focal adhesion kinase,FAK)是一类胞质非受体蛋白酪氨酸激酶,属于蛋白酪氨酸激酶超家族,在细胞信号转导中发挥重要作用,它是胞内外信号出入的中枢,介导多条信号通路。FAK可以接受来自整合素、生长因子以及机械刺激等的信号,激活胞内PI3K/Akt、Ras/MAPK等信号通路,调节细胞生长;此外,还与胚胎发育、肿瘤发生与迁移有关。FAK几乎表达于所有的细胞和组织类型,在睾丸和脑中高表达。由于在肿瘤向恶性侵袭表型演进的过程中起着重要的作用,FAK被认为是一种具有潜力的新型抗癌药物靶标。已有研究表明,FAK抑制剂是一种克服化疗、放疗或靶向治疗耐药性的潜在策略,也有研究证实了FAK抑制用于乳腺癌脑转移治疗的可行性。
目前尚未有针对FAK的药物上市,处于在研阶段的药物共20余种,多数处于临床临床前的研究阶段。国内赛林泰医药研发的小分子药物Conteltinib是一种ALK抑制剂、FAK2抑制剂、IGF1R拮抗剂和FAK1抑制剂,目前该药物处于临床Ⅲ期阶段,用于治疗非小细胞肺癌;应世生物自主开发的高效和高选择性的FAK抑制剂IN10018,目前用于包括铂耐药复发卵巢癌、三阴乳腺癌、头颈部肿瘤、胰腺癌、RAS突变肿瘤等多种缺乏有效治疗方案的实体瘤适应症临床Ⅱ期试验;APG-2449是由亚盛医药开发的新型FAK抑制剂和第三代ALK/ROS1酪氨酸激酶抑制剂,在非小细胞肺癌患者中具有良好的安全性与抗肿瘤有效性,目前处于临床Ⅰ期开发。国际上,跨国公司葛兰素史克(GSK)的GSK-2256098、辉瑞的Defactinib以及Amplia公司的AMP945等最高处于临床Ⅱ期阶段。国内药企在FAK抑制剂开发进程较快,有望实现该靶标首创药物开发。
03 IAP
凋亡抑制因子(Inhibitor of apoptosis proteins,IAPs)是一类高度保守的内源性抗细胞凋亡因子家族,是继Bcl-2家族蛋白之后发现的又一个抑制细胞凋亡的家族蛋白,主要通过抑制半胱天冬酶(Caspase)活性和参与调节核因子NF-κB的作用而抑制细胞凋亡。至今已发现8个人类IAPs家族蛋白成员,包括NAIP、c-IAP1、c-IAP2、XIAP、Survivin、Apolon、ML-IAP和ILP2。研究认为,IAPs介导的凋亡抑制可能是肿瘤细胞产生耐药性的原因之一,IAPs蛋白是调控肿瘤细胞凋亡和对化疗药物敏感性的关键分子,有可能发展为逆转肿瘤细胞耐药、提高疗效的新靶标。
迄今,针对IAP蛋白靶标,全球尚无获批药物,已进入临床研究阶段的IAP小分子抑制剂除了处于临床Ⅲ期的Xevinapant以外,还有LCL161、Birinapant(TL32711)以及APG-1387。
Xevinapant是由Ascenta和默克雪兰诺研发的一种合成多肽,是一种cIAP1/cIAP2抑制剂和IAP3抑制剂,为中国化药1类。它一款潜在口服IAP拮抗剂,能够通过促进细胞凋亡和改善抗肿瘤免疫反应,让肿瘤细胞对化学放射疗法(CRT)更为敏感,基于Xevinapant在临床Ⅱ期试验中的结果,获得FDA授予的头颈部鳞状细胞癌突破性疗法认定。Xevinapant目前正在关键临床Ⅲ期TrilynX研究中,联合含铂化疗和标准分割调强放疗,用于既往未经治疗的高危局部晚期头颈部鳞状细胞癌(LA SCCHN)患者。除正进行的临床Ⅲ期试验,多个治疗实体瘤的临床试验正在进行中,包括非小细胞肺癌、卵巢癌、头颈部肿瘤等。此外,Xevinapant联合放疗、放化疗及PD-L1抑制剂等的研究也在开展。
APG-1387是亚盛医药开发的IAP特异性抑制剂,也是我国首个进入临床开发阶段的IAP标靶药物,主要通过模拟内源性SMAC分子降解IAPs来诱导和加速细胞凋亡的进程。在乙肝药研作用机理方面,APG-1387可清除受乙肝病毒(HBV)感染细胞凋亡而不清除未受HBV感染细胞凋亡,已公布其针对我国慢乙肝受试者(CHB)的临床Ⅰ期试验研究结果,并呈现初步的有效性和安全性,目前正处在临床Ⅱ期组合疗法临床开发中。在实体瘤、晚期胰腺癌等方面,也正在开展组合疗法的临床Ⅱ期试验。APG-1387有望在乙肝创新药开发领域,实现突破性进展。
国际上,同进展阶段药物诺华制药小分子药物cIAP1/cIAP2抑制剂LCL161,目前最高研发阶段为临床Ⅱ期,用于治疗骨髓纤维化和真性红细胞增多症。另有Birinapant是由Princeton University研发的一种合成多肽,目前该药物最高研发阶段为临床Ⅰ期,用于治疗鳞状细胞癌和头颈部鳞状细胞癌。
04 GAS6
生长停滞特异性蛋白6(Growth arrest-specific protein 6,GAS6)是一个75kDa的可溶性糖蛋白,其下游受体被称为TAM受体,属于受体酪氨酸激酶家族,在肿瘤细胞上,GAS6与TAM受体结合激活Akt、Grb2、ERK及PI3K等下游信号通路,从而发挥其生物学效应,促进肿瘤细胞的存活、增殖和迁移。肿瘤微环境中,GAS6/TAM被持续激活,导致一系列免疫抑制信号的产生,如诱导肿瘤细胞表面的MHC-Ⅰ表达水平下降,引起肿瘤细胞中免疫检查点PD-L1表达升高,诱导分泌一些免疫抑制的细胞因子和趋化因子,如TGF-β、TNF-α、IL-3、CCL-3及CXCL2等,抑制宿主的抗肿瘤免疫应答,从而介导肿瘤的免疫逃逸。
针对GAS6/TAM信号通路中的上下游靶标正在进行一系列的新药研发,包括小分子抑制剂、单抗、ADC及诱饵蛋白等多种药物类型,目前均已有项目进入临床药效验证阶段,但尚无获批上市药物。在国内,思路迪的单靶标选择性AXL抑制剂3D-229(AVB-500)申报临床,成为进展最快的GAS6/TAM靶向药物,3D-229是对GAS6有高亲和力的Fc融合诱饵中和蛋白,是目前唯一可以同时阻断GAS6与三个受体结合的生物大分子类药物。当前,国内共有2项临床研究正在进行中,包括3D-229联合紫杉醇对比安慰剂联合紫杉醇治疗铂类耐药复发性卵巢癌的有效性与安全性的随机、双盲、对照、适应性Ⅲ期研究;评价3D229静脉单次给药剂量递增和重复给药在健康受试者中安全性和耐受性的单盲、随机和安慰剂对照的临床Ⅰ期研究。
【参考资料】
1. 药渡数据库.
2. 知乎、药融圈等公开报道.

 产业资讯
产业资讯
 国际肿瘤资讯
国际肿瘤资讯  2026-04-02
2026-04-02
 13
13
 产业资讯
产业资讯
 识林
识林  2026-04-02
2026-04-02
 18
18

 产业资讯
产业资讯
 医药地理
医药地理  2026-04-02
2026-04-02
 15
15