 产业资讯
产业资讯
 医药魔方Pro
医药魔方Pro  2024-12-11
2024-12-11
 953
953
12月10日,基因疗法公司uniQure宣布与FDA就AMT-130加速批准途径的关键要素达成了协议。

对于UniQure的再生医学先进疗法(Regenerative Medicine Advanced Therapy,RMAT),FDA同意将其正在进行的I/II期研究的数据与自然历史外部对照进行比较,以此加速批准路径,从而避免额外的预提交步骤。
受此消息影响,UniQure股价暴涨110%,总市值7.46亿美元。

来源:雪球
亨廷顿氏病是一种罕见的致命性神经退行性遗传疾病,会影响运动功能,导致行为症状和认知能力下降,从而导致青壮年的身体和智力全面衰退。亨廷顿氏病由编码亨廷顿蛋白的多功能基因外显子1中的CAG三核苷酸异常扩增引起。
AMT-130是uniQure首个聚焦中枢神经系统的基因疗法,由AAV5载体携带专门沉默HTT基因表达的微小RNA,利用专有的miQURE沉默技术,抑制突变亨廷顿蛋白(mHTT)的产生。
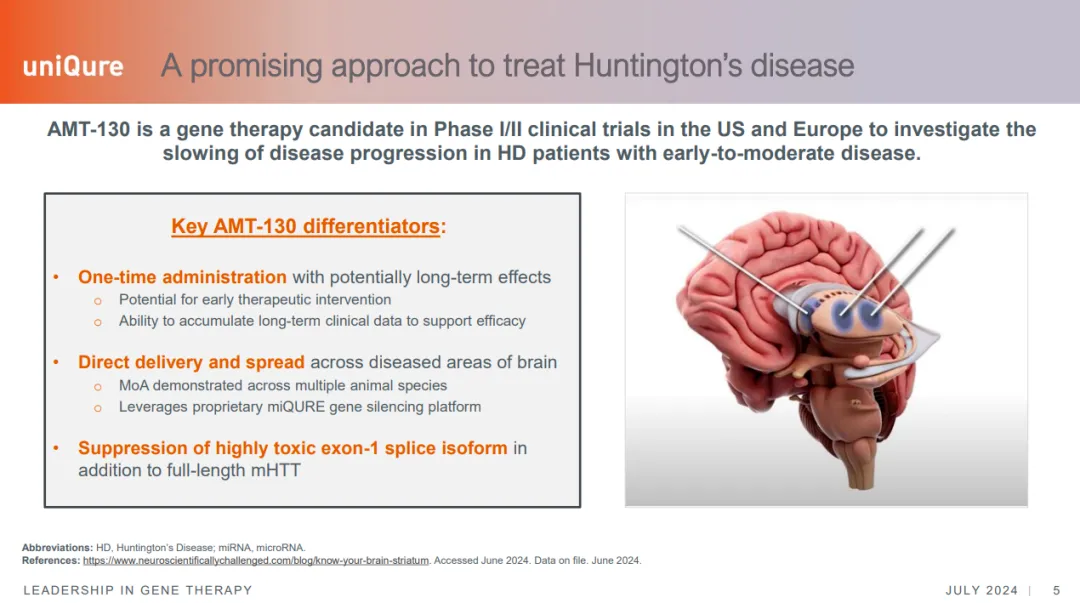
来源:uniQure官网
2024年5月,AMT-130获FDA的RMAT认定。2024年7月,uniQure公布了AMT-130在24个月时的中期数据,结果显示,疾病进展出现持久的剂量依赖性减缓,且与基线相比,24个月时,接受治疗的患者的CSF NfL(神经变性的衡量指标)减少。
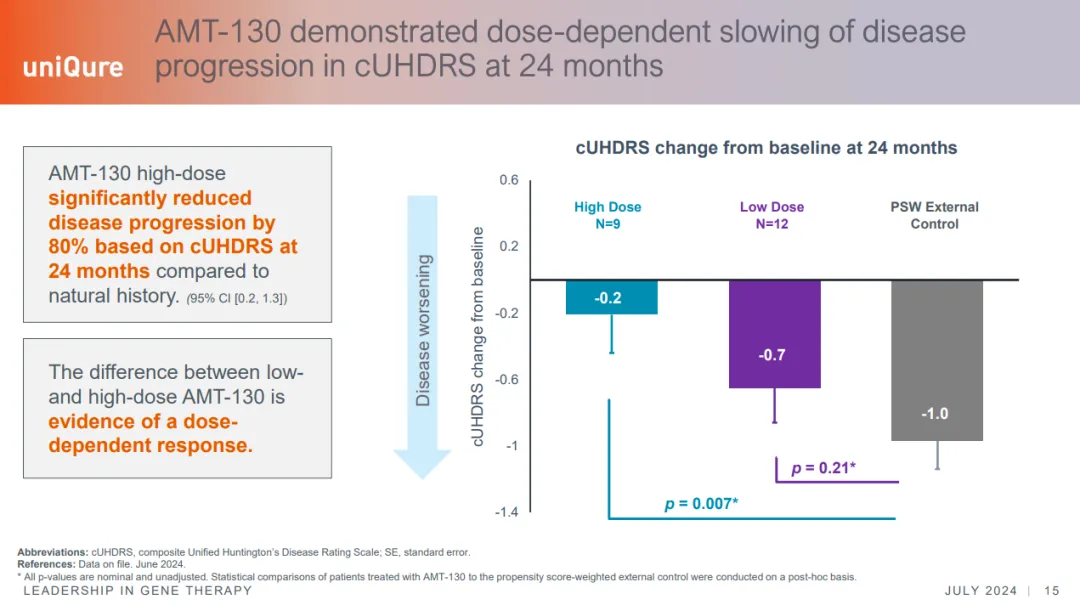
来源:uniQure官网
uniQure正在进行两项多中心、剂量递增的I/II期临床研究。
在美国的研究中,共有26例有早期显性亨廷顿病的患者被随机分配接受治疗(n=6,小剂量;n=10,高剂量)或模拟(假)手术(n=10)。接受治疗的患者通过MRI引导的传导增强立体定向神经外科手术直接将AMT-130注射到纹状体(尾状核和壳核)。
在欧洲的研究中,开放标签Ib/II期研究纳入了13例早期显性亨廷顿病患者(n=6,低剂量;n=7,高剂量)。
第三个队列正在美国和欧盟各研究中心纳入另外12例患者。该队列被随机分组,采用目前已确立的立体定向给药程序,研究两种剂量的AMT-130联合免疫抑制。
uniQure首席医学官Walid Abi-Saab博士表示:“我们已经启动了BLA准备活动,期待2025年上半年与FDA进一步接触,讨论统计分析计划和技术CMC要求。”
参考资料:
https://www.uniqure.com/investors-media/press-releases

 产业资讯
产业资讯
 研发客
研发客  2026-04-03
2026-04-03
 357
357

 产业资讯
产业资讯
 研发客
研发客  2026-04-09
2026-04-09
 48
48

 产业资讯
产业资讯
 MedTrend医趋势
MedTrend医趋势  2026-04-09
2026-04-09
 50
50