 产业资讯
产业资讯
 CPHI制药在线
CPHI制药在线  2025-03-13
2025-03-13
 3629
3629
2025年,医药行业的创新步伐将在过去几年的基础之上进一步加快,各大制药公司在具有高度开发价值的领域内继续深耕,通过各自的管线研发为将来占据有利的市场位置打下基础。通过净现值(NPV)可以判断哪些开发项目具有更高的回报预期。对于净现值的准确预测,不仅可以评估每个项目的潜在经济收益,还能帮助企业在资源有限的情况下做出最优的投资决策。
根据Evaluate Pharma的预测,2025年最具价值的研发项目归属诺和诺德的肥胖症药物CagriSema,尽管这款药物的III期临床数据“仅仅”给出了23%的减重率,但凭借其特殊的作用机制和相对较高的安全性,仍然被相当的投资者看好。
另一款极具潜在价值的项目是礼来的“3G减肥药”retatrutide,其优异的II期临床数据已经令人对它的商业化前景非常期待。礼来的另一项小分子口服减肥药orforglipron同样具有极高的潜力,将为减肥药领域带来递送方面的突破性进展。Orforglipron即将于今年晚些时间公布的III期数据也是行业最期待的事件之一。
从适应症角度来看,代谢、免疫和肿瘤学仍然代表着具有价值的开发领域(图1)。
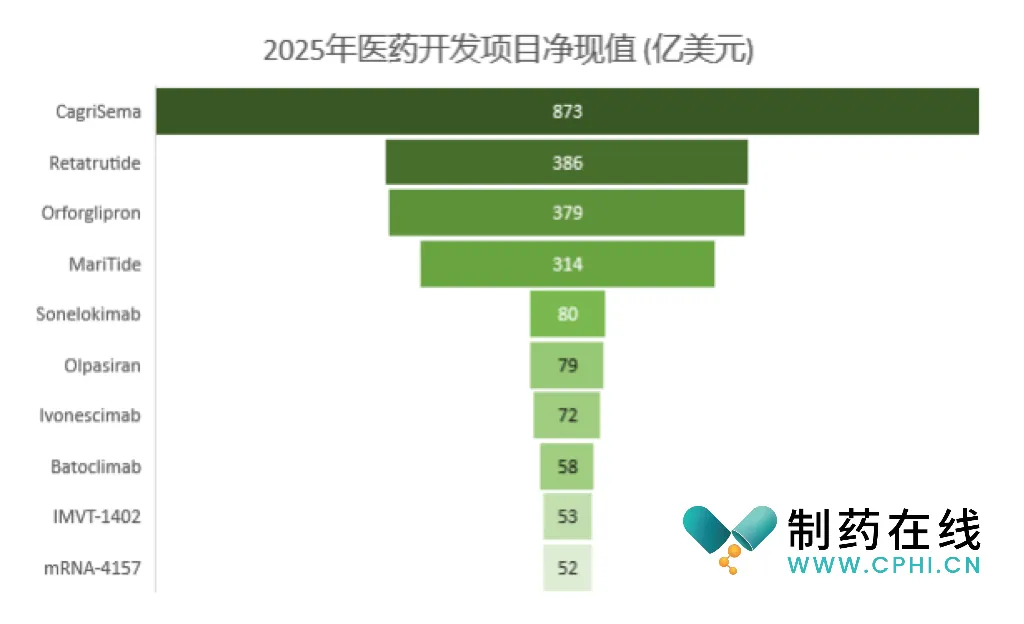
图1 2025年最具价值的医药开发项目净现值排名
01CagriSema
● 开发商:诺和诺德
● 模态:多肽
● 适应症:肥胖症
● 净现值:873亿美元
● 背景及重要性:
在Semaglutide取得商业领域的巨大成功之后,诺和诺德迫切需要一波后浪来巩固其在II型糖尿病和肥胖症领域中的领袖地位,在这种形势下,CagriSema肩负了诺和诺德“弄潮儿向涛头立”的志向。CagriSema是semaglutide和胰淀素类似物cagrilintide的联合疗法,其III期研究实现了68周内帮助参与者平均减重约23%的成绩,但这并不足以满足投资者被高高吊起的胃口,在数据公布后的短短几个小时之后,诺和的股价遭遇了大幅跳水。尽管CagriSema的研究结果显示出比单药疗法更为优越的减重效果,但在与Zepbound的减重对比上并没有占据上风。诺和诺德表示将继续进行进一步的研究,并将在2025年上半年发布一项针对2型糖尿病患者的第二项III期试验结果。
最新消息显示,诺和诺德正计划对CagriSema 进行新的III期试验,测试不同的剂量和更长的治疗时间。诺和诺德计划在 2026 年初申请CagriSema 的监管批准。
02Retatrutide
● 开发商:礼来
● 模态:多肽
● 适应症:肥胖症
● 净现值:386亿美元
● 背景及重要性:
礼来的新一代减肥药Retatrutide头顶“3G减肥药”的头衔,凭借其非常出色的中期数据,已经成为了投资者眼中的明星项目。由于同时靶向Glucagon,GLP-1和GIP受体,retatrutide具有成为首创新药的潜力。礼来最近表示,他们将比预期提前几个月公布retatrutide的III期数据,时间就在今年,而原本的计划是在2026年2月公布III期顶线数据。礼来坚信,retatrutide的减重效果将优于他们眼下的当家花魁Zepbound。除此之外,retatrutide还在针对阻塞性睡眠呼吸暂停 (OSA) 和膝骨关节炎 (OA)进行研究。
在一项针对肥胖或超重成年人的中期试验中,Retatrutide的II期减重数据为48周24.2%,安慰剂调整后为22.1%,这已经是一个相当优异的成绩,难怪投资者对于retatrutide的III期数据翘首以待。
03Orforglipron
● 开发商:礼来
● 模态:小分子
● 适应症:肥胖症
● 净现值:379亿美元
● 背景及重要性:
除了retatrutide之外,礼来的减肥药管线中还有一款同样令人期待的候选药,小分子口服减肥药orforglipron,其商业前景同样受到投资者看好。
同目前大红大紫的semaglutide和tirzepatide具有显著区别的是,orforglipron 是一款口服小分子候选药物,作用机制同样是GLP-1受体激动剂。Orforglipron的中期数据显示,26 周内可使肥胖人群体重减轻约 10%,并具有改善血压和循环脂肪分子水平的功效。
礼来表示,orforgliron计划将于 2025 年完成 III 期试验,可能于 2026 年获得FDA的批准。作为最接近上市的口服减肥药药物,orforglipron的命运对于整个行业的未来发展方向将起到前瞻性的作用。
04MariTide
● 开发商:安进
● 模态:抗体-多肽偶联物 (Peptibody)
● 适应症:肥胖症
● 净现值:314亿美元
● 背景及重要性:
榜单第四名的仍然是一款减肥药,安进的MariTide。MariTide的最大看点在于其模态,它是一款相当特殊的抗体-多肽偶联物(也被简称为Peptibody)。MariTide由与抗 GIP抗体缀合两个 GLP-1 受体激动剂多肽组成。这种多肽抗体偶联物的模态在药物开发中本就不是很常见,在减肥药物中就更加罕见。
MariTide目前处于临床III期,其中期数据给出了52周减重20%的结果。MariTide的另一大看点在于其可能实现每月一次的给药频率,甚至有可能实现每季度给药一次的“远大目标”。除此之外,MariTide 已显示出在最后一次给药后数月维持减肥效果的能力,这一点对于减肥药的市场位置至关重要。
05Sonelokimab
● 开发商:Moonlake Immunotherapeutics
● 模态:纳米抗体
● 适应症:复杂免疫疾病
● 净现值:80亿美元
● 背景及重要性:
Sonelokimab是一款人源化纳米抗体,由三个 VHH 结构域组成,通过甘氨酸-丝氨酸spacer共价连接。Sonelokimab 具有两个结构域,可以高亲和力选择性结合 IL-17A 和 IL-17F,从而抑制 IL-17A/A、IL-17A/F 和 IL-17F/F 二聚体。
Sonelokimab针对两种适应症进行开发,即HS(化脓性汗腺炎)和银屑病关节炎 (PsA),开发它的Moonlake也在寻求皮肤病学和风湿病学的其他适应症,包括青少年 HS、PPP(掌跖脓疱病)和 axSpA(轴性脊柱关节炎)。Sonelokimab目前处于针对HS成年患者的3 期试验,针对青少年HS的3期试验也在进行之中。
Sonelokimab标志着针对复杂免疫疾病的创新解决方案,对炎症疾病的传统疗法提出了挑战。分析师预测,到 2035 年,其创新产品线可能会取得巨大成功,销售额将超过 80 亿美元。与现有的 TNF 抑制剂相比,Sonelokimab 提供了一种新的作用机制,可能对某些患者群体产生更好的疗效,这也得益于其纳米抗体的模态优势。它能够穿透困难的组织环境,这可能使其比阿达木单抗或依那西普等传统疗法更具竞争优势。
06Olpasiran
● 开发商:安进
● 模态:siRNA
● 适应症:心血管疾病
● 净现值:79亿美元
● 背景及重要性:
Lipoprotein(a)(Lp(a),脂蛋白(a))被认为是炎症和动脉粥样硬化的主要驱动因素,因为它能够运输氧化磷脂,而氧化磷脂会导致血管中斑块积聚。由安进(Amgen)研发的小干扰RNA(siRNA)药物 Olpasiran,通过诱导载脂蛋白(a)信使RNA(mRNA)的降解来阻止脂蛋白(a)的生成。最新研究发现,在动脉粥样硬化性心血管疾病患者中,高剂量的Olpasiran可使 Lp(a) 降低 95% 以上。除了降低脂蛋白 (a)外,Olpasiran还降低了氧化磷脂的水平,而氧化磷脂被认为会促进动脉粥样硬化。Olpasiran目前处于3期临床研究,进一步评估其改善心血管患者临床结果的潜力。如果成功,这种创新的siRNA的方法将提供一种全新高效的心脏疾病管理策略。
07Ivonescimab
● 开发商:Akeso/Summit
● 模态:双特异性抗体
● 适应症:肺癌
● 净现值:72亿美元
● 背景及重要性:
康方生物和Summit的肿瘤学抗体药物Ivonescimab是一款在机制上引人关注的PD-1/VEGF双特异性抗体。它将肿瘤学中两种已验证的机制融入一种新型四价分子中。PD-1 与 VEGF 阻断剂同时相互作用有可能产生协同抗肿瘤活性:抑制VEGF可以通过调节肿瘤微环境(TME)来帮助提高免疫治疗的效果。VEGF 是正常血管发育的关键细胞因子,也是血管、肿瘤和其他发生异常血管生成的组织发育的关键细胞因子。通过阻断这种通路,可以改变肿瘤微环境,并抑制血管生成和异常血管生长;另一方面,增强 PD-1 阻断有助于激活 T 细胞,起到免疫检查点抑制剂的功效。除此之外,ivonescimab 的半衰期较短,与其他药物相比,其安全性可能更高。
Ivonescimab 在 2024 年 IASLC 世界肺癌大会 (WCLC) 上名声鹊起,因为其3期数据显示,与PD-1抑制剂Keytruda相比,Ivonescimab在晚期非小细胞肺癌 (NSCLC) 患者中的疗效具有临床显著改善。FDA已授予 ivonescimab 联合铂类化疗的快速通道资格,用于治疗在 EGFR-TKI 治疗后病情进展的局部晚期或转移性 EGFR 突变型 NSCLC 成年患者,其前景非常值得期待。
08Batoclimab
● 开发商:Immunovant/Roivant
● 模态:单抗
● 适应症:自免疫疾病
● 净现值:58亿美元
● 背景及重要性:
格雷夫斯病(Graves' disease)是一种自身免疫性疾病,是甲状腺功能亢进的最常见原因之一。在格雷夫斯病中,免疫系统错误地攻击甲状腺,导致其分泌过量的甲状腺激素。甲状腺激素是调节新陈代谢、心跳、体温等重要生理功能的关键激素。预计到 2033 年,全球格雷夫斯病市场规模将达到 6.146 亿美元。Immunovant/Roivant开发的单抗候选药Batoclimab在其中期研究中给出了相当不错的成绩,受试者实现了很高的响应率。Batoclimab在对包括格雷夫斯病和重症肌无力在内的自免疫疾病进行临床研究。如果能够成功,Batoclimab将对目前市场上的Vyvgart构成直接竞争,后者今年的销售额预计将达到33亿美元。
09IMVT-1402
● 开发商:Immunovant/Roivant
● 模态:单抗
● 适应症:格雷夫斯病
● 净现值:53亿美元
● 背景及重要性:
IMVT-1402是一款由 Immunovant/Roivant开发的FcRn抑制剂类药物,通过抑制 FcRn 受体的作用来减少体内循环中的免疫球蛋白 G(IgG)水平,进而降低由自身抗体引发的免疫反应,主要用于治疗包括格雷夫斯病在内的自身免疫性疾病。Immunovant已经开始对 IMVT-1402 在其他具有巨大商业潜力的相关自身免疫性疾病中进行 3 期研究,包括格雷夫斯病和慢性炎症性脱髓鞘性多发性神经病,在这些疾病中,降低 IgG 有望带来有意义的益处。Immunovant/Roivant还将启动 IMVT-1402 在重症肌无力中的III期研究。到 2026 年,预计将开展 10 项 IMVT-1402 的III期注册研究。
10mRNA-4157
● 开发商:莫德纳/默沙东
● 模态:疫苗
● 适应症:黑色素瘤等肿瘤
● 净现值:52亿美元
● 背景及重要性:
癌症疫苗在如今的肿瘤学产品开发中占据的作用越来越重要。癌症疫苗的开发具有重要性,因为它们能够通过增强免疫系统的抗癌能力,在不增加毒性的情况下提升免疫治疗的效果,特别是在转移性和高复发率的癌症中。癌症疫苗的开发不仅为患者提供了新的治疗选择,还能与现有的免疫疗法如PD-1抑制剂等联合使用,提高疗效并延长无病生存期。
莫德纳与默沙东联合开发的mRNA-4157是一种个性化新抗原疗法 (INT, Individualized Neoantigen Therapy),可能通过产生新生肿瘤特异性 T 细胞活性与免疫检查点抑制剂协同作用。在 其2b 期 KEYNOTE-942 研究中,与单独使用Keytruda相比,mRNA-4157 + Keytruda的联合疗法显示出对 III/IV 期黑色素瘤的临床结果的改善。
mRNA-4157的辅助性黑色素瘤的 3 期临床试验已全面招募。两项针对非小细胞肺癌的 3 期研究、一项针对高风险肌肉浸润性膀胱癌的随机 2 期研究,以及一项针对辅助性肾细胞癌的随机 2 期研究也都在招募之中。
参考来源:
1.Tirrell, M. An experimental drug drove people to lose 23% of their body weight. It’s still seen as a disappointment. CNN Health. 20. 12. 2024.
2.Gardner, J. Novo outlines new late-stage study of obesity drug CagriSema. Biopharm Dive. 05. 02. 2025.
3.Eli Lilly's Next-Generation Weight Loss Drug: Retatrutide Set for Early Release in 2025. AInvest. 06. 02. 2025.
4.Guglielmi, G. The weight-loss drugs being tested in 2025: will they beat Ozempic? Nature. 06. 02. 2025.
5.Feuerstein, A. Previewing Immunovant’s myasthenia gravis study readout — with all its quirky nuance. STAT. 06. 02. 2025.
6.Chrisomalis, T. Immunovant: Continued FcRn Targeting With IMVT-1402 Pivotal Study. Seeking Alpha. 27. 12. 2024.
7.MoonLake initiates three new clinical trials and further expands the portfolio of indications for the Nanobody? sonelokimab. Moonlake Press Release. 08. 01. 2025.
8.Will MoonLake Immunotherapeutics Lead Healthcare Stocks’ Resurgence? DSA. 21. 02. 2025.
9.Iapoce, C. Olpasiran Reduces Oxidized Phospholipids on ApoB in OCEAN(a)-DOSE Trial. HCP Live. 12. 02. 2025.
10.Motzer, R. J. et al. NTerpath-004: A phase 2, randomized, double-blind study of adjuvant pembrolizumab (pembro) with V940 (mRNA-4157) or placebo for renal cell carcinoma (RCC). Journal of Clinical Oncology. 2025. 43. https://doi.org/10.1200/JCO.2025.43.5_suppl.TPS61
11.Chan, A. Potential Applications of Cancer Vaccines Continue to Expand in Squamous Cell Carcinoma. OncLive. 12. 02. 2025.
12.Hollasch, M. The Novel Bispecific Antibody Ivonescimab May be Poised to Change the SOC in

 产业资讯
产业资讯
 药通社
药通社  2026-06-06
2026-06-06
 511
511

 产业资讯
产业资讯
 赛柏蓝
赛柏蓝  2026-06-06
2026-06-06
 411
411

 产业资讯
产业资讯
 摩熵医药
摩熵医药  2026-06-06
2026-06-06
 429
429
 热门资讯
热门资讯