 会员动态
会员动态
 医药魔方
医药魔方  2022-08-19
2022-08-19
 3703
3703
近日,国际顶尖医学杂志《Nature Medicine》发表了一项临床试验(ARROW, NCT03037385)的更新数据,引起了业内对“泛瘤种”治疗的关注。该临床试验药物为基石药业的一款已上市产品——普吉华®(普拉替尼,Pralsetinib),这是国内首个且唯一获批准上市的一款高选择性RET抑制剂。此次公布的数据证明了普拉替尼在RET融合阳性的多种实体肿瘤中具有良好的治疗效果,为普拉替尼应用于泛瘤种提供了初步数据支持。

ARROW是一项全球I/II期临床研究,旨在评估普拉替尼在RET融合阳性非小细胞肺癌(NSCLC)、RET突变型甲状腺髓样癌(MTC)和其他RET融合的晚期实体瘤患者中的安全性、耐受性和有效性。基于此项研究之前公布的数据,普拉替尼在中国大陆已先后获批两大适应症:1)既往接受过含铂化疗的RET融合阳性的局部晚期或转移性NSCLC;2)晚期或转移性RET突变型MTC和RET融合阳性甲状腺癌(TC)。
此次期刊发表公布了普拉替尼在早先纳入的各种RET融合阳性肿瘤患者中的疗效和安全性数据,共计29例患者,12种不同肿瘤类型,不包括上述获批适应症类型。在这29例患者中,有23例患者被最终纳入疗效分析的患者数据。其中女性患者14例(61%),转移性患者20例(87%),且均在基线时接受过既往治疗。癌症类型包括:胰腺癌(4)、胆管癌(3)、神经内分泌癌(3)、肉瘤(3)、结直肠癌(2)、小细胞肺癌(2),汗腺癌、唾液腺导管癌、胃癌、卵巢癌各1例等。
结果显示,研究主要终点的总缓解率(ORR) 达57%(Cl 95% , 35~77),其中完全缓解(CR) 3例(13%),部分缓解(PR) 10例(43%)。在中位随访时间26.7个月时,患者临床获益率(CBR)达70%,疾病控制率(DCR)达83%,中位缓解持续时间(DOR)为11.7个月。在获得CR或PR的13例患者中,9例的DOR ≥6个月,2例的缓解持续时间 ≥24个月。
根据RECIST 1.1标准进行基线后肿瘤评估,91%的患者靶病灶缩小;1例患者出现新发病部位进展,未接受基线后的靶病变评估(未展示在下图a中)。
在数据截止时,31%(4/13)的患者仍处于缓解状态,首次缓解的中位时间为1.9个月(1.7~3.6)。
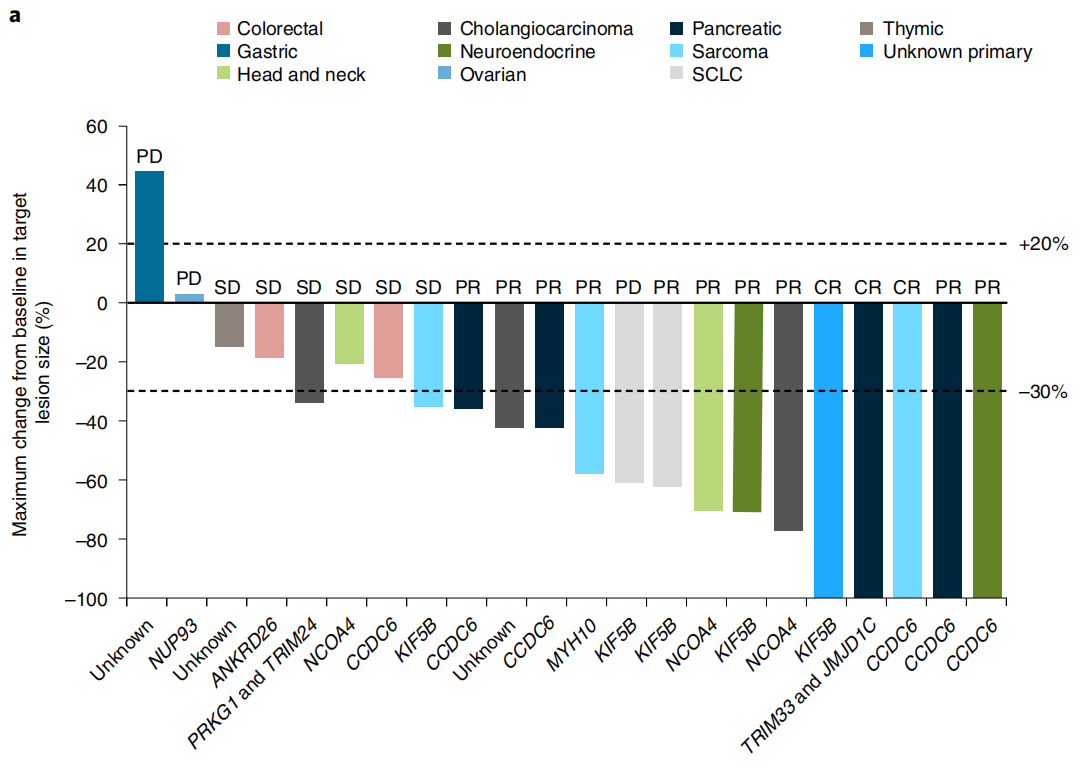
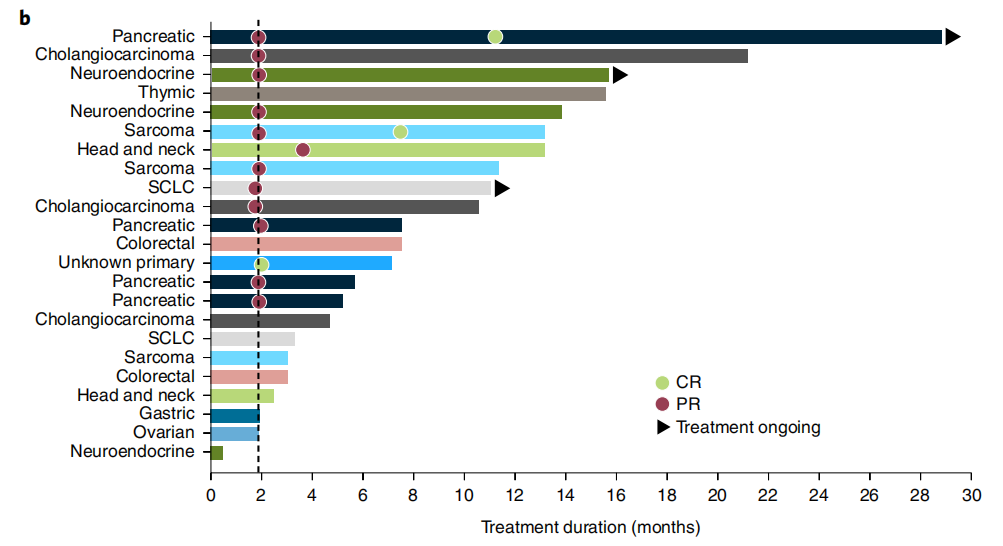
疗效可评价人群的个体肿瘤反应和治疗持续时间瀑布图&泳道图
这一结果令人倍受鼓舞,这些患者所患疾病在标准治疗中的缓解率通常不足30%,因此人们对能够改善临床获益的更好的治疗方法需求非常高。
在安全性方面,此批患者的表现与之前在RET融合阳性NSCLC以及甲状腺癌患者中报告的结果一致,未发现新的安全信号。最常见的不良事件为丙氨酸转氨酶(ALT)与天冬氨酸转氨酶(AST)升高,中性粒细胞减少以及贫血。
这是普拉替尼首个在除已获批适应症的晚期或转移性RET融合阳性实体瘤患者中的潜在泛瘤种注册研究,不论肿瘤类型如何,普拉替尼均显示出稳健且持久的抗肿瘤活性。这不仅再次验证了RET作为靶向基因组进行肿瘤精准治疗的潜力,也预示了普拉替尼在泛瘤种治疗中的希望。
打开RET抑制剂泛肿瘤治疗前景
RET基因,属于肿瘤罕见驱动基因,在多个瘤种中都有发现RET基因改变。在细胞生长过程中,RET基因发生点突变和融合突变会使RET基因逃脱配体调控,自我磷酸化强化、信号转导功能增强,促使激酶的活化以及原癌基因的转化,最终诱发肿瘤。
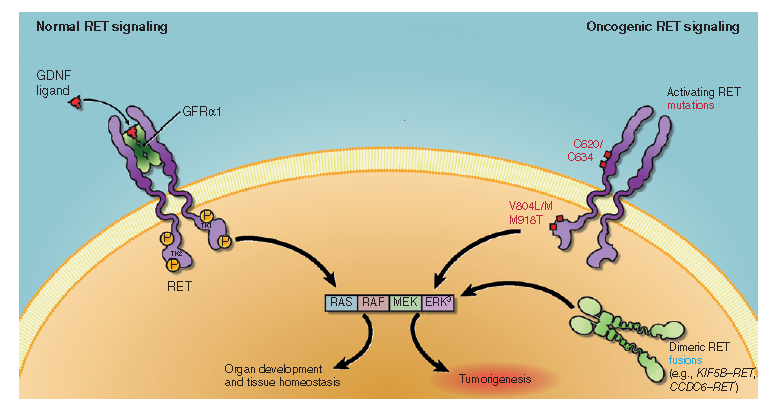
RET基因变体诱发肿瘤示意图
目前,在NSCLC、MTC、乳头状甲状腺癌、胸膜间皮瘤、结直肠癌及胰腺癌等多种肿瘤中,均观察到了不同程度的RET基因变异现象。因此,针对RET基因变异的治疗有望成为一种不限癌种的治疗方式。
在过去的15年中,靶向治疗在RET变异实体瘤中的应用大幅增加,已获批多款多激酶抑制剂(MKI),如凡德他尼(Vandetanib)、卡博替尼(Carbozantinib)、舒尼替尼(Sunitinib)。但上述药物整体对于RET基因融合/突变的靶向性并不强,有效性相对较差。同时MKI对酪氨酸激酶的非选择性抑制会产生脱靶毒性,RET变异实体瘤患者需要疗效更佳、安全性更好的治疗方案。
2020年开始,国际上对选择性RET抑制剂的开发有了质的突破,2款新药相继获批上市,其中基石药业的高选择性RET抑制剂普拉替尼率先进入国内市场,改变了国内尚无精准靶向RET抑制剂的格局。目前该药已有两大适应症在不同国家和地区陆续获批。
2020年9月4日,FDA批准普拉替尼用于治疗晚期RET融合阳性NSCLC成人患者;
2021年3月24日,中国国家药品监督管理局(NMPA)批准普拉替尼用于二线治疗RET基因融合阳性的局部晚期或转移性NSCLC成人患者;
2022年2月,中国台湾食品药物管理署(TFDA)受理其用于治疗局部晚期或转移性RET融合阳性NSCLC、RET突变MTC及 RET融合阳性TC患者的NDA;
2022年3月11日,NMPA批准普拉替尼用于一线治疗晚期或转移性RET突变型MTC及RET融合阳性TC患者;
2022年7月15日,中国香港批准普拉替尼用于治疗RET基因融合阳性的NSCLC成人患者。
这款药物在上市第一天就在近百家医院使200多例患者获益,上市后一个月内便已覆盖约70个城市的80家DTP药房。同时基石药业2021年财报显示,普拉替尼的销售额实现快速增长,在上市后的前八个月内便与泰吉华®(阿伐替尼)合计创下人民币1.628亿元的净销售额。
不仅如此,该产品已纳入超60个主要省市的商业保险中,包括北京京惠保、成都惠蓉保、苏州苏惠保、海南乐城、珠海大爱无疆等,进一步提升产品在患者端的可及性。
此次新公布的ARROW研究23例RET融合阳性实体瘤患者临床数据,让我们对普拉替尼在泛癌种治疗中的潜力信心倍增。据预计,在2025年,中国被新诊断出RET基因变异的患者将达7万人。而普拉替尼作为一款可精准靶向的选择性RET抑制剂,未来市场不可限量。

 会员动态
会员动态
 中国医药创新促进会
中国医药创新促进会  2026-03-16
2026-03-16
 73
73

 会员动态
会员动态
 长风药业
长风药业  2026-03-14
2026-03-14
 76
76

 会员动态
会员动态
 医药观澜
医药观澜  2026-03-14
2026-03-14
 152
152