 研发追踪
研发追踪
 药明康德
药明康德  2023-01-09
2023-01-09
 3222
3222
今日,Roivant Sciences公司宣布,潜在“first-in-class“抗TL1A单克隆抗体RVT-3101在2b期临床试验中获得积极结果。经过生物标志物筛选的患者群体中,接受预期3期临床试验剂量治疗的患者达到40%的临床缓解率(clinical remission)和56%的内镜改善率。新闻稿指出,这款疗法具有成为治疗溃疡性结肠炎患者的“first-in-class”和“best-in-class”皮下注射疗法的潜力。
溃疡性肠炎是炎症性肠病(IBD)的一种,是一种影响结肠的慢性疾病。由于免疫系统的过度活跃反应,结肠内壁出现炎症,并且产生溃疡,患者症状包括持续腹泻、腹痛、便血、食欲不良、体重减轻和疲惫等。Roivant Sciences指出,即便接受先进疗法治疗,仍然只有10~15%的患者获得临床缓解。
RVT-3101是一款抗TL1A单克隆抗体,最初由辉瑞(Pfizer)公司开发。TL1A阻断剂代表着一种治疗炎症性和纤维化疾病的新方式。对这项临床试验中获得的患者样本的分析显示,RVT-3101可以调节多种炎症和纤维化生物标志物的水平。辉瑞在去年12月与Roivant Sciences共同创建一家Roivant Sciences旗下的子公司,合作开发这一候选疗法。

▲阻断TL1A具有治疗广泛炎症和纤维化疾病的潜力(图片来源:Roivant Sciences官网)
在这项名为TUSCANY-2的随机双盲,含安慰剂对照的剂量递增2b期临床试验中,中重度溃疡性结肠炎患者接受了不同剂量的RVT-3101或安慰剂的治疗。中期结果显示,在所有患者群体中,RVT-3101组达到32%的临床缓解率,安慰剂组为12%(p=0.01)。RVT-3101组达到40%的内镜改善率,安慰剂组为19%(p=0.01)。
在经过生物标志物筛选的患者群体中,接受预期3期临床试验剂量RVT-3101治疗的患者的临床缓解率为40%,是安慰剂组(10%)的4倍(p=0.02)。这一群体的内镜改善率为56%,是安慰剂组(10%)的5.6倍(p=0.0005)。生物标志物阳性的患者群体约占总患者群体的60%。
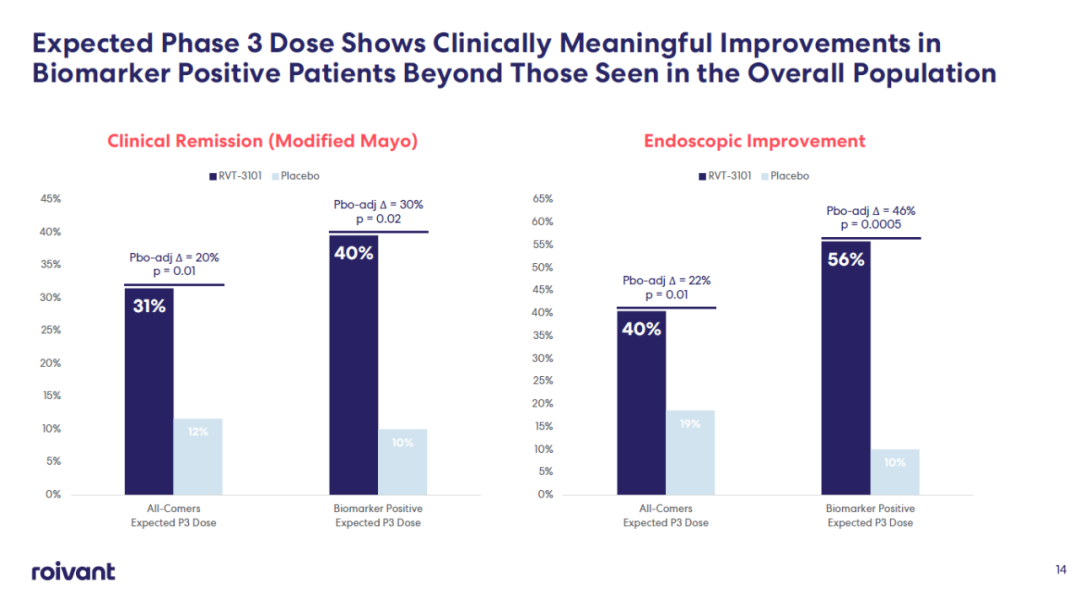
图片来源:Roivant Sciences官网
在生物标志物阳性且接受过生物制品治疗的患者群体中,RVT-3101组达到41%的临床缓解率和56%的内镜改善率,安慰剂组的这两个数值均为0%。
“我们对这些初步数据非常满意,RVT-3101不但在整体患者中表现出较高疗效和可喜的安全性特征,而且在生物标志物阳性患者中的效力进一步提升,包括曾经接受过生物制品治疗的患者。我们期待能够将这款创新疗法带给上百万期待更有效疗法的患者。”Roivant首席执行官Matt Gline先生说。
原文链接:https://investor.roivant.com/static-files/60d82fd7-2c60-4476-8155-57d648532d26

 研发追踪
研发追踪
 DailyBio
DailyBio  2025-05-12
2025-05-12
 161
161

 研发追踪
研发追踪
 UmabsDB
UmabsDB  2025-05-12
2025-05-12
 161
161
 研发追踪
研发追踪
 药明康德
药明康德  2025-05-12
2025-05-12
 168
168