 研发追踪
研发追踪
 生物制品圈
生物制品圈  2023-02-27
2023-02-27
 3255
3255
2月21日辉瑞公司宣布,美国食品和药物管理局(FDA)接受了呼吸道合胞病毒(RSV)候选药物RSVpreF的生物制品许可申请(BLA)的优先审查。RSVpreF(PF-06928316)为在研的RSV疫苗,通过孕妇主动免疫,预防从出生到六个月大的婴儿因RSV引起的就医下呼吸道疾病(MA-LRTI)和严重的MA-LRTI。若获批,此疫苗将会成为使用于怀孕妇女,以避免婴孩出生后感染RSV相关疾病的首款疫苗。这次的申请主要是基于MATISSE临床3期试验的积极顶线数据。该研究评估了RSVpreF在大约7400名妊娠24至36周的孕妇(≤49岁)中的疗效和安全性。
预定中期分析显示,MATISSE试验达成两个主要终点的其中一项。即疫苗避免婴孩出生后90天内感染严重性MA-LRTI的保护力达81.8%(CI:40.6-96.3%),避免婴孩在出生后6个月的追踪期间感染严重性MA-LRTI的保护力达69.4%(CI:44.3-84.1%)。虽然第二个主要终点没有达到统计显著水平,但仍可在第二项主要终点的分析上,见到疫苗的效力。即疫苗避免婴孩出生后90天内,预防MA-LRTI感染的保护力达57.1%(CI:14.7-79.8%),避免婴孩在出生后6个月的追踪期间内感染MA-LRTI的保护力达51.3%(CI:29.4-66.8%)。

在试验期间内预定,由外部数据监测委员会(DMC)所进行的定期安全性检验,显示此在研疫苗具良好的耐受性,对接种的妇女与其婴孩没有安全上的顾虑。辉瑞公司的疫苗研发部门高级副总裁兼首席科学官Annaliesa Anderson博士说道“如果获得批准,RSVpreF将能自婴孩首次呼吸开始,便帮助他们避免RSV传染病的影响”“鉴于其在预防婴儿RSV方面为全球健康做出积极贡献的巨大潜力,我们期待着与FDA和其他监管机构一起推进对辉瑞公司RSV母体候选疫苗的审查。”
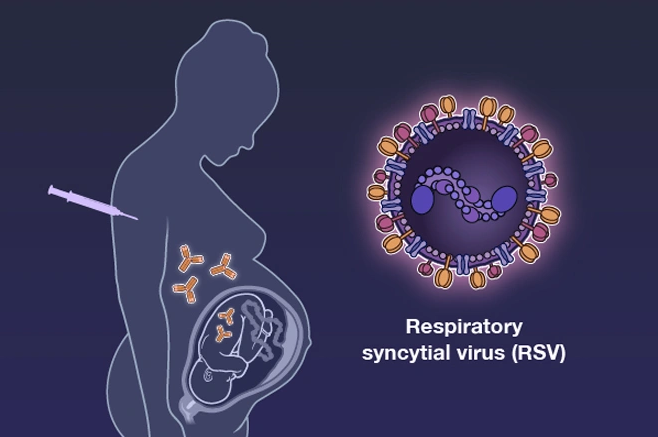
关于respiratory syncytial virus(RSV)
RSV是下呼吸道感染最常见的原因,也是导致全球婴儿住院的首要致病因素,且大多数住院发生在健康足月婴儿中。老年人亦是RSV易感人群。据统计,全球每年约10.2万名儿童死于RSV感染。目前,还没有针对所有婴儿和老年人的预防方案,治疗也仅限于缓解症状。FDA于2022年3月授予RSVpreF突破性疗法认定。11月,辉瑞公布了关键的3期MATISSE临床试验的正面顶线数据,基于其优先审评状态,FDA将疫苗的PDUFA日期定为2023年8月。2022年12月向FDA递交用于老年人预防RSV感染的BLA,并且该BLA同样获FDA优先审评,PDUFA时间为2023年5月。

 研发追踪
研发追踪
 药智网
药智网  2025-10-13
2025-10-13
 778
778

 研发追踪
研发追踪
 药闻天下
药闻天下  2025-10-13
2025-10-13
 706
706

 研发追踪
研发追踪
 丁香园Insight数据库
丁香园Insight数据库  2025-10-13
2025-10-13
 715
715