 产业资讯
产业资讯
 2015-08-18
2015-08-18
 3632
3632
来源:南京文德医药 2015-08-18
2014年是全国药品注册管理在改革与探索中前进的一年,江苏省药品注册工作任务空前繁重。通过强化药品技术审评能力建设、推进药物研究机构质量管理体系建设、进一步完善药品注册管理机制,江苏省药品注册管理工作在平稳中前行,药品注册各项指标保持全国领先,现对相关数据资料进行统计、对比与分析,旨在为促进公众健康做出应有的贡献。
2 药品注册审批情况及分析2.1药品注册申请批准率逐年提高
2014年江苏省共收到国家总局药品注册审评批件673件,其中批准件565件(含复审批临床2件),批准率为84%,比上年提高14个百分点。565件批准件中,药品注册批准件180件,批准率80%,比上年提高4个百分点;药品补充申请批准件 383件,批准率87 %,比上年提高19个百分点。近五年江苏省药品注册申请批准情况见表3。

从全国各省(市)的批准情况来看,江苏省药品注册申请受理量遥遥领先,不批准率低于全国平均水平(见图8)。
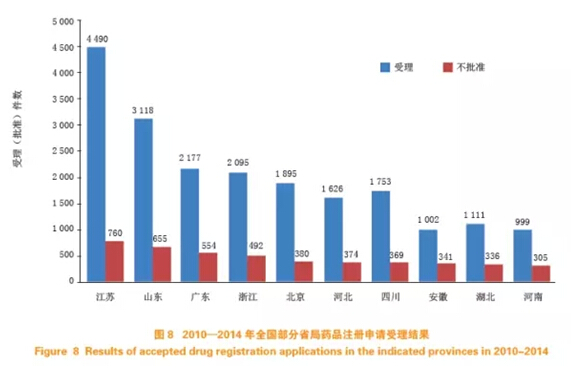
2.2创新药收获显著
2014年江苏省获生产批准文号的药品有81件(见表4),全部为化学药品,占全国新批准药品上市总数(456 件)的17.8%,其中化药1.1类8件(全国共11件),涉及3个品种,分别是江苏恒瑞医药股份有限公司的甲磺酸阿帕替尼、江苏豪森药业股份有限公司的吗啉硝唑、苏州二叶制药有限公司的阿德福韦酯。
2014年江苏省获批准进入临床研究的品种有99件,占全国总数(880件)的11%。其中,化药1.1类(23件)占全国(68件)的34%,有两个品种进入临床研究的企业分别是江苏恒瑞医药股份有限公司、江苏豪森药业股份有限公司、江苏亚盛医药开发有限公司。
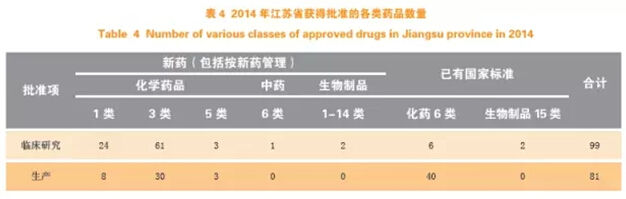
2.3注册的政策导向发挥作用
近五年江苏省药品注册批准数量呈新药增长、仿制药下降的趋势(见图9)。
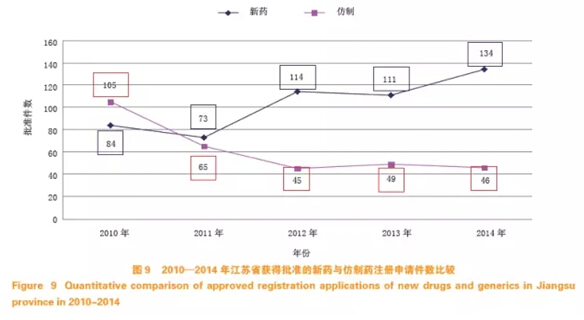
药物研发需要良好的创新性生态体系,这个体系要以企业为创新主体,以市场配置资源为发展方式,以政府的前瞻性规划吸引为政策引导。江苏省药品注册呈现量增质升的喜人趋势,其原因:一是医药产业的持续高速发展,为新药研发奠定了较为雄厚的经济基础,重点制药企业研发投入占销售收入的比例普遍在5%以上;二是地方政府大力实施创新驱动发展战略,集聚了人才和项目,搭建了公共服务平台;三是独特的科教优势和人文环境,多种形式的专业培训与交流研讨,为我省药物研究营造了良好的技术氛围;四是药监部门鼓励创新、推动产业结构调整的药品注册管理政策发挥了导向作用。
2.4药品注册退审情况及分析
2014年,江苏省收到的国家总局药品注册审评批件中,退审件共44件,其中因技术性原因退审的29件,企业自撤的有13件,因真实性问题退审的有2件。2014年,江苏省收到的国家总局药品补充申请审评批件中,退审件为59件,其中因技术性原因退审的有50件,企业自撤的有9件。
因技术性原因退审的主要问题是:①品种立题依据不足,有效性及安全性研究结果均不能支持申请事项;②质量标准中有关物质研究存在缺陷,无法有效控制产品的质量,且未与进口原研药品进行质量对比研究,不能证明其质量的一致性;③剂型选择不合理,根据《化学药品注射剂基本技术要求(试行)》(国食药监注【2008】7号)中剂型选择的一般原则,已有采用终端灭菌工艺的同品种注射剂上市,如申报品种采用无菌灌装生产工艺,则不再批准相关的申请;④未结合原料药结构和制剂工艺特点,分析制剂的杂质谱,并建立合理可行的有关物质检查方法,对杂质进行控制;⑤新规格依据不充分;⑥变更后工艺质量可控性尚不能评价,灭菌工艺验证资料不全面;⑦无法证实药包材与制剂有良好的相容性及可能的安全性风险。
3 药品注册现场核查情况及分析
2014年江苏省全年共组织开展各类注册核查1 162次,其中药品研制现场核查715次(较上年增长27%),临床试验核查44次,委托市局生产现场检查295次,药包材注册核查72次。2014年江苏省组织开展了多次药物临床试验机构监督检查,共抽查19家GCP机构的86个临床试验项目。2014年江苏省接受国家总局组织的GLP检查3次,疫苗临床试验一次性资格认定检查6次,注册生产现场检查8次,均全部通过。
注册核查发现的主要问题有:①部分研究机构质量管理体系不健全,没有专职质量管理人员,缺少研究机构质量管理方面的制度与措施;②关键仪器设备未进行校验或缺少日常使用校验;③原始记录存在重新誊抄现象;④人员流动性大,导致部分研究资料保管不全,现有人员不能全面了解项目研究情况;⑤个别机构在电子数据上有弄虚作假的行为,特别是稳定性考察数据的原始性和真实性难以确定;⑥样品小试、中试采用空白样,多家相同申报品种采用窜样形式;⑦生物等效性试验或人体药代试验缺少过程管理,试验样品的真实性存疑。
4 展望
2015年, 国家总局深化药品注册审评审批制度改革的措施将陆续出台,应密切关注创新药上市许可持有人制度、仿制药审批新政、药品注册受理模式调整、药用辅料药包材与药品关联审评等重大制度的实施,充分发挥药品注册管理的杠杆作用,促进我省医药经济健康发展。
 产业资讯
产业资讯
 瞪羚社
瞪羚社  2025-12-17
2025-12-17
 29
29

 产业资讯
产业资讯
 智药局
智药局  2025-12-17
2025-12-17
 28
28

 产业资讯
产业资讯
 BiG生物创新社
BiG生物创新社  2025-12-17
2025-12-17
 30
30