 产业资讯
产业资讯
 医药魔方
医药魔方  2021-06-21
2021-06-21
 5073
5073
6月11日,日本第一三共株式会社宣布其溶瘤病毒产品G47∆被日本厚生劳动省(MHLW)批准,用于治疗恶性胶质细胞瘤。时隔6年,G47∆成为继美国安进公司溶瘤病毒产品T-VEC之后,获批的第二个溶瘤单纯疱疹病毒产品,也是全球首款获批治疗恶性胶质细胞瘤的溶瘤病毒产品。
升级版G207
G47∆的前世今生
HSV-1 G207由Robert Martuza博士团队研制,它删除了ICP34.5。G47∆是第一三共与日本东京大学医学科学研究所的Tomoki Todo博士在G207敲除ICP34.5的基础上,删除了ICP47之后得到的新一代HSV-1溶瘤病毒产品。
Tomoki Todo博士对G207和G47Δ两款产品进行了比较。结果显示,HSV1病毒下调MHC-I的表达,而缺失了ICP47的G47Δ株对MHC-I的表达无明显影响。证明ICP47缺失后,可阻止HSV1下调MHC-I的表达,在促进肿瘤抗原递呈和抗肿瘤免疫方面发挥了重要作用。在U87MG人神经胶质瘤和Neuro2a鼠神经母细胞瘤的小鼠植瘤模型中,分别给予G207和G47Δ治疗,G47Δ疗效明显优于G207[1]。
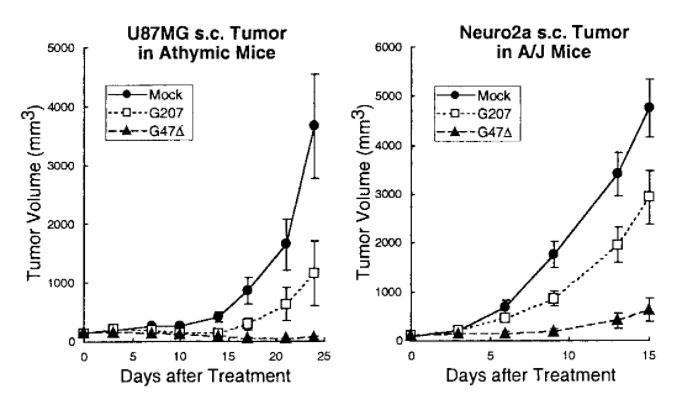
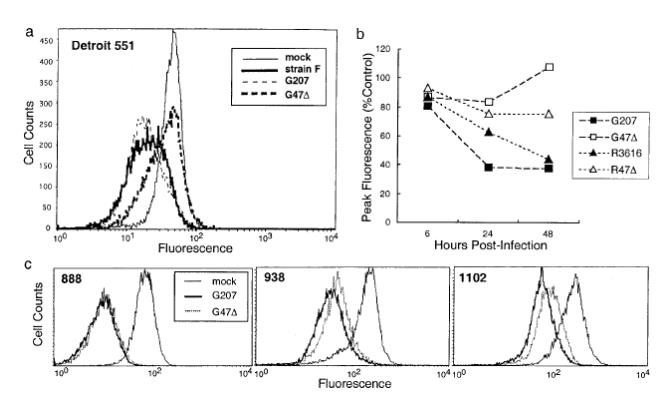
临床前研究中,G47Δ几乎在所有的癌症类型和实验模型中都表现出了抗肿瘤功效。基于临床前研究的有效性和安全性,G47Δ在日本开展了多个临床试验,在一项针对恶性、复发性神经胶质母细胞瘤的临床试验中,13例患者中有12例患者在治疗后的生存期长达1年以上,1年生存率为92.3%,到达了主要终点,较标准治疗15%的1年生存率显著提高。临床研究进一步证明ICP47的缺失增强了病毒的复制能力和免疫系统抗肿瘤免疫反应[2]。
他山之石,足以攻玉
T-VEC原研团队夯实研发基础
早在2003年,英国BioVex研究团队就在《Gene Therapy》发表文章,证明HSV1删除ICP47后明显增强了BALB/c鼠体内抑瘤效果[3]。进入临床III期研究,因为疗效显著,被美国安进公司收购,2015年被FDA批准,成为首个上市的溶瘤疱疹病毒药物T-VEC。
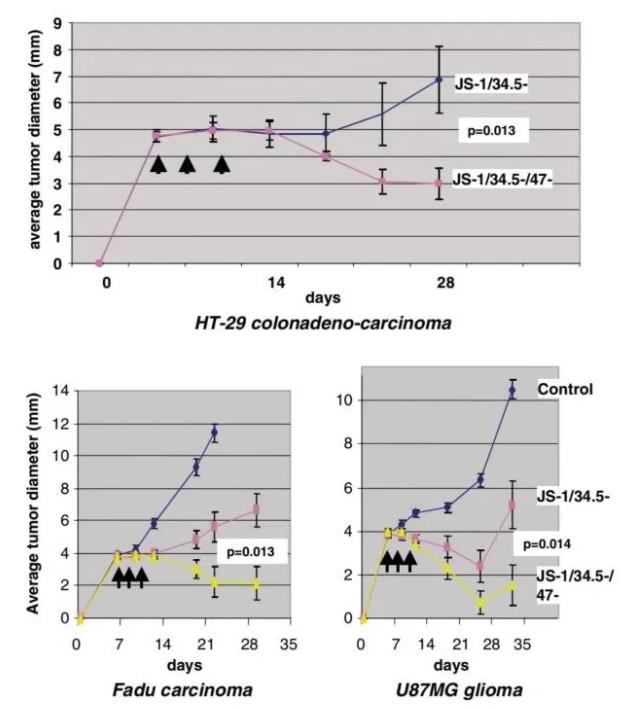
2020年,Journal for ImmunoTherapy of Cancer发表的综述《Clinical landscape of oncolytic virus research in 2020》分析了2000年至2020年溶瘤病毒公开的97项独立临床试验。该篇综述发现,单纯疱疹病毒的临床反应要优于腺病毒、呼肠孤病毒、牛痘病毒等其他溶瘤病毒。又一款溶瘤单纯疱疹病毒获批,无疑振奋了整个溶瘤病毒研究领域,更让单纯疱疹病毒光彩夺目。
百舸争流,奋楫者先
两款在研溶瘤单纯疱疹病毒临床数据惊艳
目前获批上市的T-VEC和G47Δ均以单纯疱疹病毒为载体,并敲除了ICP34.5和ICP47,而另外两款在研的溶瘤单纯疱疹病毒也公布了积极的临床数据:
Replimune公司RP1
美国Replimune公司联合创始人兼CEO Robert Coffin此前是英国BioVex创始人,T-VEC正是安进公司收购BioVex的产品。Replimune建立了专有溶瘤病毒技术平台Immulytic™,开发了RP1、RP2、RP3三款候选产品,其病毒的改造敲除了ICP34.5和ICP47。2020年10月,Replimune公司在SITC2020年会公布了RP1单药或/和nivolumab联用治疗皮肤癌的临床试验数据:在包括对PD-1耐药的皮肤癌患者和鳞状细胞癌(CSCC)患者中,RP1和nivolumab联合疗法显示出积极的抗肿瘤活性;在CSCC患者中(N=11),客观缓解率(ORR)为72.7%(8/11),完全缓解率(CR)为45.5%(5/11)[4]。
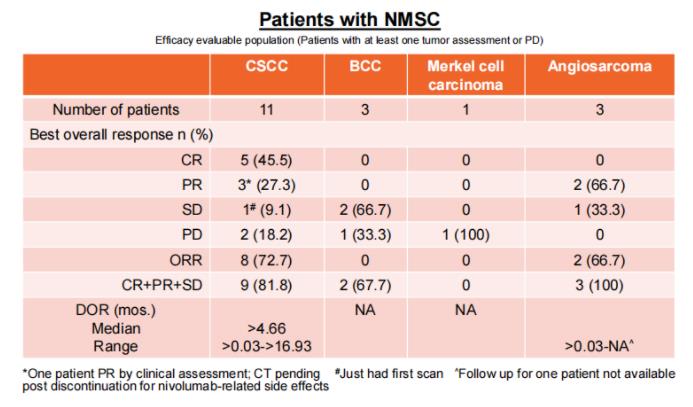
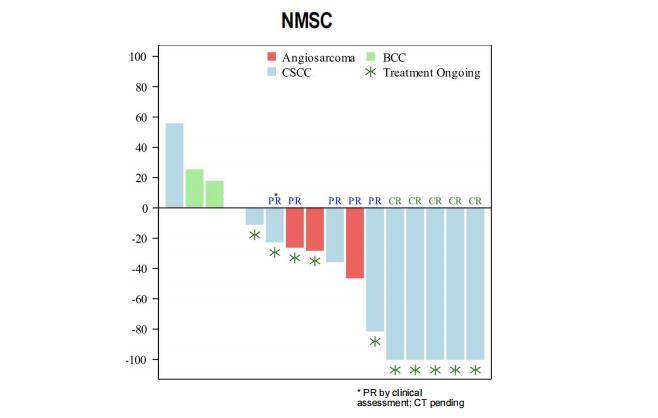
滨会生物OH2
2021年4月,发表在Journal for ImmunoTherapy of Cancer的文章公布了滨会生物OH2注射液应用于晚期实体瘤患者的安全性、耐受性和抗肿瘤活性的临床试验结果[5]。滨会生物搭建了新型oHSV2溶瘤病毒平台,开发的系列oHSV2溶瘤病毒均敲除了ICP 34.5和ICP 47基因。首款溶瘤病毒OH2注射液2018年获得NMPA批准开展临床研究,先后针对黑色素瘤、多种实体瘤(结直肠癌、食管癌、头颈癌、胰腺癌、肺癌等)适应症,采取单药、联合免疫检查点抑制剂(ICI)给药,开展多中心、多队列的临床试验,在越来越多的肿瘤患者身上看到积极疗效。尤其是结直肠癌适应症,单药队列的可评估病例(17例)客观缓解率(ORR)达到12.5%,是目前结直肠癌三线治疗首推药物呋喹替尼(ORR为4.7%)的2.6倍。
单纯疱疹病毒同时具有基因组容量大的特点,免疫调节分子(如:hGM-CSF、IL-2、IL-4、IL-10、 IL-12等)和单克隆抗体(如PD-1/PD-L1单抗)已被广泛应用于溶瘤单纯疱疹病毒,用这些外源基因“武装”病毒可以进一步增强病毒感染和裂解肿瘤细胞的疗效,但如何使外源治疗基因在肿瘤细胞中高表达,仍取决于病毒在肿瘤内复制的能力。同时敲除ICP34.5和ICP47的单纯疱疹病毒,在肿瘤组织中特异复制增殖的特性更加明显,成为了更加理想的平台。相信将有更多的外源基因装载到这个平台,发挥不同的作用,去开启溶瘤世界一扇扇新的大门。
参考资料
[1] Oncolytic herpes simplex virus vector with enhanced MHC class I presentation and tumor cell killing. Proc Natl Acad Sci U S A. 2001 May 22;98(11):6396-401. doi: 10.1073/pnas.101136398.
[2] 依靠II期单臂试验IIT数据,第一三共申请溶瘤病毒药物在日上市|第一现场. 研发客
[3] ICP34.5 deleted herpes simplex virus with enhanced oncolytic, immune stimulating, and anti-tumour properties. Gene Ther. 2003 Feb; 10(4): 292-303. doi: 10.1038/sj.gt.3301885.
[4] Replimune Poster Presentation of RP1 Update in the Skin Cancer Cohorts at the Society for Immunotherapy of Cancer (SITC) 2020Annual Meeting
[5] Intratumoral OH2, an oncolytic herpes simplex virus 2, in patients with advanced solid tumors: a multi-center, phase 1/2 clinical trial. J Immunother Cancer. 2021 Apr;9(4):e002224. doi: 10.1136/jitc-2020-002224.

 产业资讯
产业资讯
 识林
识林  2026-05-23
2026-05-23
 509
509

 产业资讯
产业资讯
 米内网
米内网  2026-05-23
2026-05-23
 419
419

 产业资讯
产业资讯
 药通社
药通社  2026-05-23
2026-05-23
 432
432
 热门资讯
热门资讯