 产业资讯
产业资讯
 Insight数据库
Insight数据库  2021-07-09
2021-07-09
 4953
4953
7 月 8 日,CDE 突破性疗法栏目更新,拟将正大天晴的 TQ-B3525 纳入突破性疗法。TQ-B3525 是一款新型、选择性口服 PI3K α/δ 抑制剂,本次突破性疗法的适应症为既往至少二线治疗失败的复发/难治滤泡性淋巴瘤。
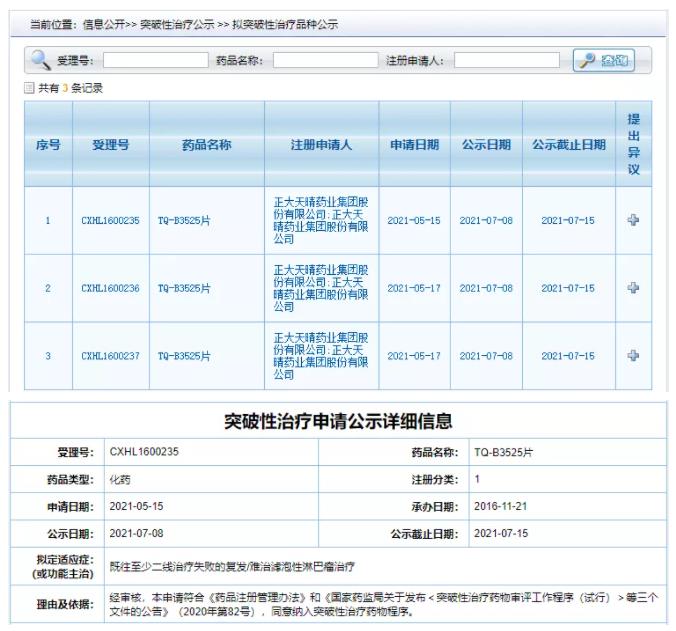
PI3Kα/δ 抑制剂
PI3K 即磷脂酰肌醇 3-激酶,可分为 I 型、II 型、III 型三类,目前广泛研究的是 I 型 PI3K,已有研究表明这种分型的 PI3K 与肿瘤关系密切。I 型 PI3K 是由调节亚基 p85 和催化亚基 p110 组成的异源二聚体,催化亚基又分为 α、β、δ、γ 四种,其中 PI3Kα、PI3Kβ 在多种细胞中表达,而 PI3Kδ、PI3Kγ 只在免疫系统中表达。
TQ-B3525 属于 PI3K α/δ 双重抑制剂,它既可以克服单独抑制 PI3Kδ 亚基时引起的 PI3Kα 亚基活性上调导致的耐药问题,同时较之 PI3K 泛抑制剂又显著降低了毒副作用。临床前结果显示,其抑制 PI3Kα 和 PI3Kδ 的活性分别是 Buparlisib 的 41 和 138 倍。
目前,根据 Insight 数据库,天晴在国内共启动了 6 项临床,主要针对血液瘤。其中进展最快的 2 项已进入 2 期临床,分别针对复发/难治性套细胞淋巴瘤(MCL)和复发/难治性滤泡性淋巴瘤(FL)。除此之外,天晴还开发 TQ-B3525 用于慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)。
实体瘤方面,天晴也启动了 1 项联合氟维司群治疗 HR 阳性、HER2 阴性 PIK3CA 突变晚期乳腺癌的 1b 期临床,另有 1 项针对 PI3KA 突变或 PTEN 缺失/低表达进展期骨肿瘤的 1b 期临床正在招募中。
TQ-B3525 国内临床概况
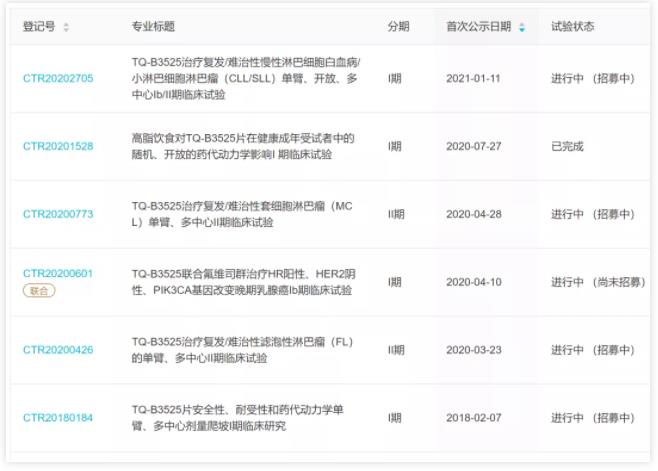
来自 Insight 数据库(http://db.dxy.cn/v5/home/)
在 2020 ASCO 会议上,天晴公布了 1 期临床(登记号:NCT03510767)的临床数据。这是一项评估 TQ-B3525 治疗中国晚期恶性肿瘤的安全性、耐受性、药代动力学和抗肿瘤活性的 1 期临床,纳入的患者包括既往接受过至少 2 线抗肿瘤治疗的复发/难治性(R/R)淋巴瘤患者以及标准治疗失败的晚期实体瘤患者。截至 2020 年 3 月,共入组了 40 例患者。
患者基线数据
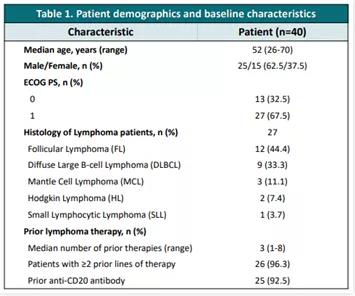
来自 2020 ASCO
根据 2014 Lugano 分类,23 名淋巴瘤患者可评估临床疗效。总有效率(ORR)为 60.9%(14/23,4 例 CR,10 例 PR),DCR 为 87.0%(20/23)。其中 ≥10 mg qd 的 ORR 和 DCR 分别为 70.0%(14/20)和 95.0%(19/20)。
分癌种而言,对于 R/R FL 患者(11 例既往接受过利妥昔单抗治疗),ORR 为 72.7%(8/11,2 例 CR)。对于 R/R MCL 患者(2 例既往接受过 BTK 抑制剂治疗),ORR 100%(3/3)。对于 R/R DLBCL 患者,ORR 为 42.9%(3/7),其中≥10 mg qd 的 ORR 为 60%(3/5,2 例 CR)。
至数据截止(2020.3.15)时,淋巴瘤患者中位 PFS 未达到(事件发生率:33.3%);1 例 FL 患者反应持续时间至数据截止时达到了 15.8 个月。
TQ-B3525 治疗血液瘤的疗效数据
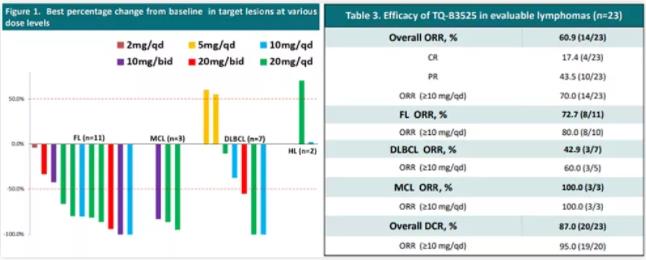
来自 2020 ASCO
安全性方面,共 39 例患者(97.5%)出现治疗相关的 AE(TRAE),其中 3 或 4 级 TRAE 12 例(30 %)。
结果显示,TQ-B3525 治疗中国晚期恶性肿瘤患者可耐受,并在 R/R 淋巴瘤中展现了具有前景的抗肿瘤活性。
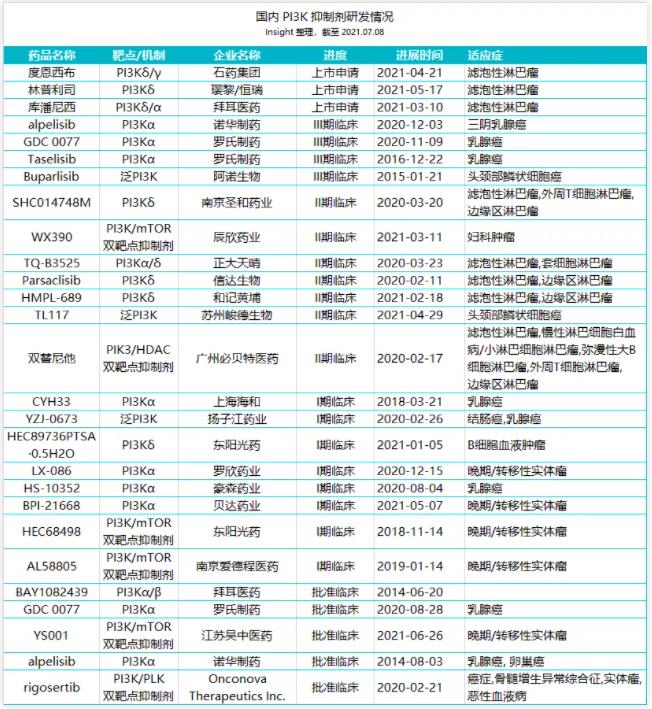
在国内,已有 25 款 PI3K 抑制剂在研,既有靶向 PI3K 不同亚基的药物,也有泛 PI3K 抑制剂或双靶点抑制剂,不过尚无企业有相关产品获批上市,进展最快的 3 款已经报产,石药引进的 PI3Kδ/γ 抑制剂度恩西布、璎黎药业/恒瑞医药的 PI3Kδ 抑制剂林普利司以及拜耳的 PI3Kα/δ 抑制剂库潘尼西。亚基选择性和临床开发适应症的不同,或许将是未来产品竞争力的重要影响因素。
2020 年研发投入近 30 亿,
60 个项目打造创新药管线
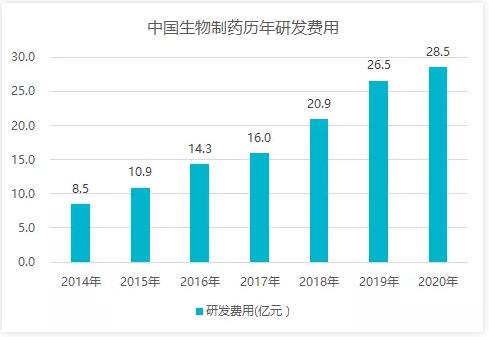
创新是企业的生命线。如今,在政策倒逼、市场竞争加剧之下,药企纷纷下重金研发,中国生物制药的研发投入亦是逐年上涨,在 2020 年已经达到了 28.53 亿元,约占当年总营收的 12.1%,在国内药企中排到前五。
根据 Insight 数据库,中国生物制药目前拥有一条包括 60 款临床阶段新药的管线,大部分来自于子公司正大天晴。其中以小分子化药为主,45 款小分子创新药蓄势待发;9 款生物类似药和 6 款生物创新药也颇具竞争力。
化药进展最快的是 ALK 抑制剂 TQ-B3139,已经启动头对头克唑替尼的 III 期临床,对克唑替尼耐药后的非小细胞肺癌也有多个临床研究开展到 II 期。抗肿瘤领域在研的 CDK4/6 抑制剂、c-Met 抑制剂、ROS1 等均进展到 II 期临床。
其中 CDK4/6 抑制剂国内已有礼来的阿贝西利、辉瑞的哌柏西利分别在 2020 年和 2018 年获批进口,国产恒瑞的 CDK4/6 抑制剂率先报产,正大天晴 TQB3616 胶囊和复星医药的 FCN-437c 胶囊紧随其后。此外,中生还布局了三代 EGFR 抑制剂 FHND9041 和四代 EGFR 抑制剂 TQB3804。
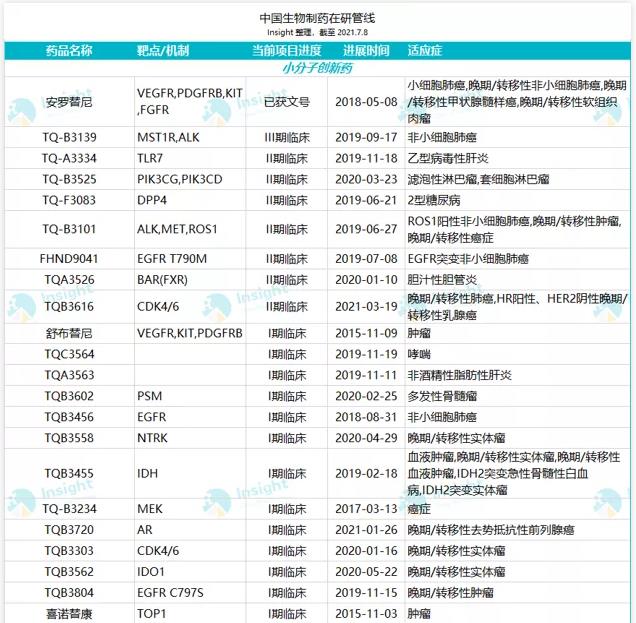

*靶点根据官方信息整理,欢迎评论区补充
天晴最接近于上市的生物创新药是与康方生物合作的派安普利单抗。这款 PD-1 单抗最初于 2020 年在国内报产,目前有经典型霍奇金淋巴瘤(cHL)和一线鳞状 NSCLC 两项适应症在审评中,预计年内获批;今年 5 月,派安普利单抗还迈出了出海的重要一步:向 FDA 递交了 NDA。
在自研管线之内,天晴另有一款处于 III 期临床的 PD-L1 单抗 TQB2450。这款单抗在 2017 年申报 IND,目前已经针对非小细胞肺癌、三阴乳腺癌、头颈部鳞状细胞癌、宫颈癌等十余个癌种启动了 18 项临床。此外,天晴还布局多个潜力备受看好的靶点:PD-L1/TGFβ 双抗、TIM-3 单抗。这些靶点的价值都已经被跨国药企的临床数据所证实。
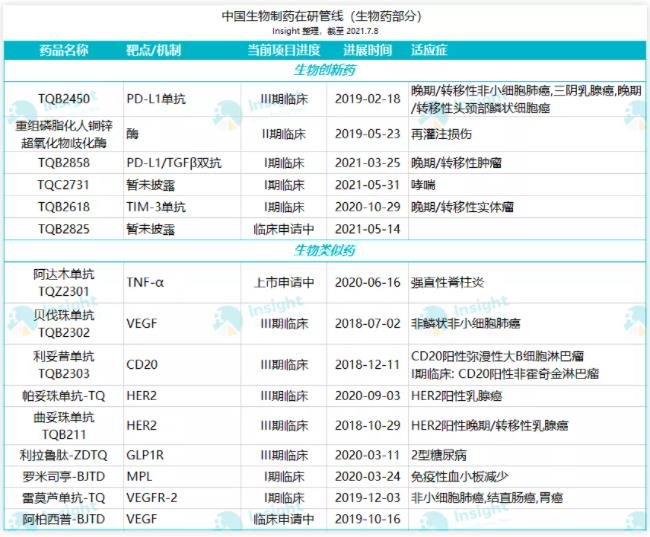
生物类似药方面,中国生物制药有 9 款在开发中。包括竞争激烈的阿达木、贝伐珠、利妥昔、曲妥珠……另外 5 款生物类似药目前都尚无国产类似药报产,天晴大多属于第一梯队。
小结
相较于创新型企业,天晴作为仿创结合的老牌药企在创新药方面的起步稍晚于同行,不过从研发投入和管线建设方面可以看出天晴创新转型的决心。本次突破性疗法认定也是对天晴创新能力的一种认可,意味着天晴的创新药开发不仅数量上持续提升,在质量上也达到了新的高度。

 产业资讯
产业资讯
 识林
识林  2025-05-08
2025-05-08
 37
37

 产业资讯
产业资讯
 阿基米德Biotech
阿基米德Biotech  2025-05-08
2025-05-08
 42
42

 产业资讯
产业资讯
 研发客
研发客  2025-05-08
2025-05-08
 41
41