 产业资讯
产业资讯
 药融圈
药融圈  2021-10-09
2021-10-09
 4557
4557
根据药融云数据库显示。2021年9月(截止9月30日),美国FDA共批准:
4款创新药,包含3个新分子实体和1个生物药。Livmarli、Ulipta、Tivdak、Exkivity这四款药物均为全球首次获批上市。
2款改良型新药
35款仿制药,其中2个仿制药为暂定批准。中国药企获4个ANDA批文,涉及复星医药旗下印度GLAND、上海上药中西制药、海南双成药业、台湾安成药业。其中上海上药中西制药的醋酸艾司利卡西平为临时性批准。
9月FDA批准的创新药

(数据来源:药融云数据库)
9月FDA批准的改良型新药

(数据来源:药融云数据库)
9月中国药企获批的ANDA批文

(数据来源:药融云数据库)
Maralixibat 首款儿童肝脏疾病创新疗法
9月29日,美国FDA批准Mirum Pharma Inc 的创新药Livmarli (Maralixibat) 用于治疗1岁以上Alagille综合症(ALGS)儿童患者的胆汁淤积性瘙痒。Maralixibat是FDA批准的首款治疗该类肝脏疾病的药物。
目前欧洲药品管理局正在审评Maralixibat 用于治疗进行性家族性肝内胆汁淤积症(PFIC2)的上市申请。
Maralixibat是一款口服的选择性顶端钠依赖性胆汁酸转运蛋白(ASBT)抑制剂,ASBT介导小肠内胆汁酸的吸收,并帮助其循环回肝脏。Maralixibat可以使更多的胆汁酸随粪便排出,防止过量胆汁酸积累,控制与胆汁淤积性肝病相关的极度瘙痒。
Alagille综合症是一种罕见的遗传病,患者的胆管先天发育不良,导致胆汁在肝脏内积累,阻止肝脏正常工作。ALGS可累及肝脏,心脏,肾脏和中枢神经系统等身体器官。15%-47%的患者最终需要进行肝移植。严重瘙痒是该疾病的主要特征,在3岁左右的患者中最为常见。
北海康成引进
2021年 4月29日 Mirum制药有限公司和北海康成制药双方已签订许可协议,授权北海康成在大中华区(包括中国大陆、香港、澳门和台湾地区)对Maralixibat进行开发和商业化。Mirum有权获得1100万美元的预付款,研发资金,和在实现未来注册和商业化Maralixibat后最高1.09亿美元的里程碑款项,以及基于产品净销售额可观的双位数的梯度特许权使用费。

来源:药融云全球药物研发数据库
Atogepant 首款预防发作性偏头痛的口服gepant
9月28日,美国FDA批准艾伯维新药Ulipta (Atogepant)上市,用于预防成人偏头痛。是第一款专门为预防性治疗发作性偏头痛(EM)而开发的口服gepant。
Atogepant是一种口服降钙素基因相关肽(CGRP)受体拮抗剂(gepant),专门开发用于偏头痛的预防性治疗。CGRP及其受体表达于与偏头痛病理生理相关的神经系统区域。研究表明,CGRP水平在偏头痛发作期间升高,选择性CGRP受体拮抗剂对偏头痛有临床疗效。
在偏头痛领域,艾伯维正在销售BOTOX(肉毒杆菌毒素A,onabotulinumtoxinA)和Ubrelvy(ubrogepant)。其中,BOTOX是美国FDA批准的第一个针对成人慢性偏头痛的预防性药物,Ubrelvy则是美国FDA批准的第一种口服CGRP受体拮抗剂(gepant),用于成人偏头痛(有或无先兆)的急性治疗。
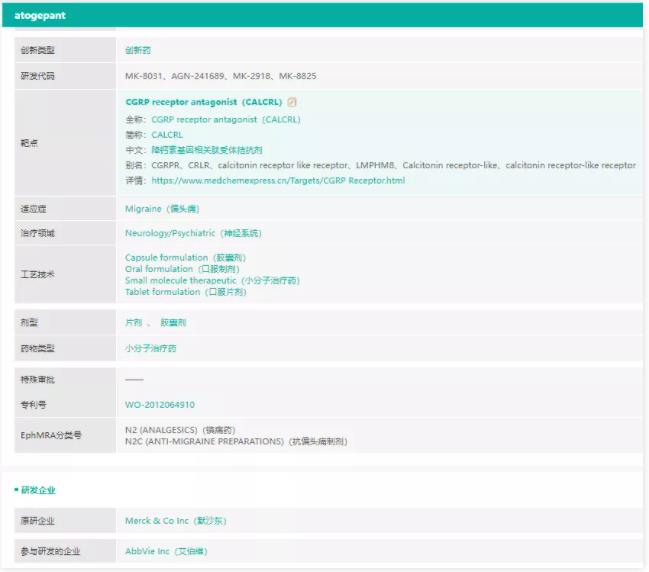
来源:药融云全球药物研发数据库
Tivdak 宫颈癌首款ADC疗法
9月20日,美国(FDA)加速批准了Seagen公司 ADC药物Tivdak(Tisotumab vedotin)上市,用于治疗复发性或转移性宫颈癌。值得一提的是,Tivdak是宫颈癌的第一个也是目前唯一一个获批的抗体药物偶联物(ADC),对于宫颈癌女性来说是一个重要的里程碑。
Tisotumab vedotin是一种靶向组织因子(TF)的在研ADC药物,该药旨在靶向癌细胞上的TF抗原,并将细胞毒制剂MMAE(单甲基奥瑞他汀E)直接递送至癌细胞内。在癌症生物学中,TF是一种参与肿瘤信号传导和血管生成的蛋白质,在绝大多数宫颈癌患者和许多其他实体瘤(包括卵巢、肺、胰腺、结直肠和头颈部癌症)中过度表达。基于TF因子在许多实体瘤中的高表达和快速内化,TF成为了开发ADC药物的理想标靶。

来源:药融云全球药物研发数据库
Mobocertinib 首个EGFR 外显子20插入突变肺癌的口服疗法
9月 15日,美国FDA批准武田新药Exkivity(Mobocertinib Succinate)上市,用于治疗先前接受含铂化疗期间或之后病情进展、经FDA批准的检测方法证实为携带表皮生长因子受体(EGFR)20号外显子插入突变(EGFRex20ins)的局部晚期或转移性非小细胞肺癌(mNSCLC)成人患者。FDA的批准让该类肺癌患者有了全新的针对性治疗选择。
Exkivity是第一个也是唯一一个被批准专门选择性靶向EGFRex20ins突变的口服疗法。Exkivity的活性药物成分为mobocertinib,这是一种新型、强效小分子酪氨酸激酶抑制剂(TKI),旨在高选择性靶向于EGFR和人表皮生长因子受体2(HER2)20号外显子插入突变。在中国和美国,该药均被授予突破性疗法认定(BTD)。
目前武田已于今年7月向中国提交mobocertinib的上市申请并被纳入优先审评,不久将为中国该类肺癌患者带来福音。
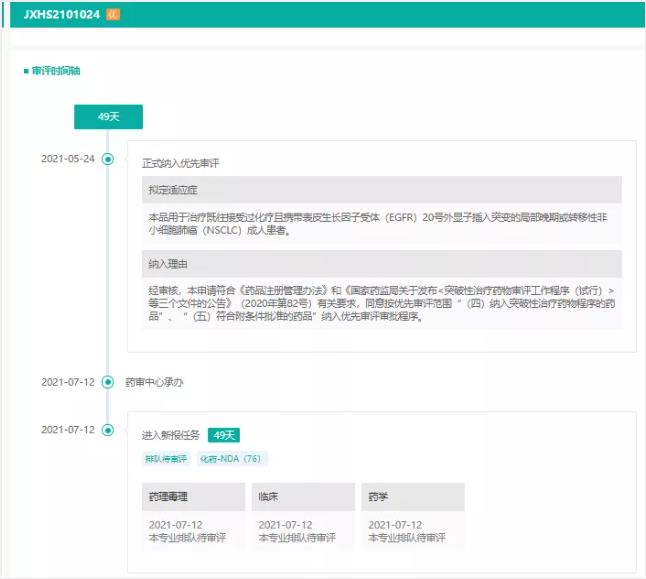
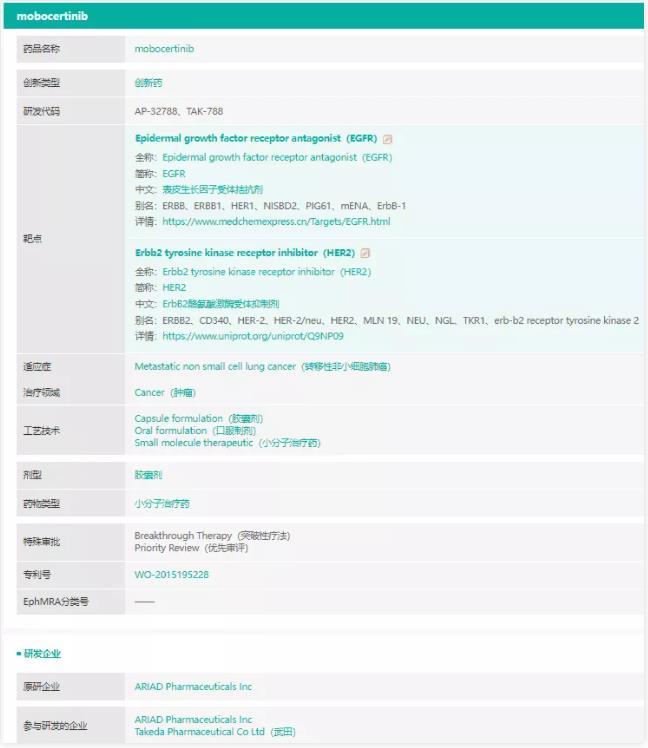
来源:药融云全球药物研发数据库

 产业资讯
产业资讯
 细胞基因治疗前沿
细胞基因治疗前沿  2026-05-25
2026-05-25
 43
43

 产业资讯
产业资讯
 研发客
研发客  2026-05-25
2026-05-25
 509
509

 产业资讯
产业资讯
 一度医药
一度医药  2026-05-25
2026-05-25
 445
445
 热门资讯
热门资讯