 产业资讯
产业资讯
 GBIHealth
GBIHealth  2022-03-03
2022-03-03
 3146
3146
据GBI此前发布的新药审批专题报告,2021年我国新药审批全面加速,共81种新分子(按有批准文号的西药分子名计,不区分剂型)首次在国内上市,这是自2017年中国加入国际人用药品注册技术协调会(ICH)以来批准新药最多的一年,也是中国药品审批具有里程碑意义的一年。
尤其值得关注的是,本土企业自主创新成果在2021年集中落地,自研新药占比高达35.8%(图1),与进口新药齐平,这体现了国内企业开启创新转型的决心,并已表现出初步成效。
图1. 国内创新药比重逐年增加
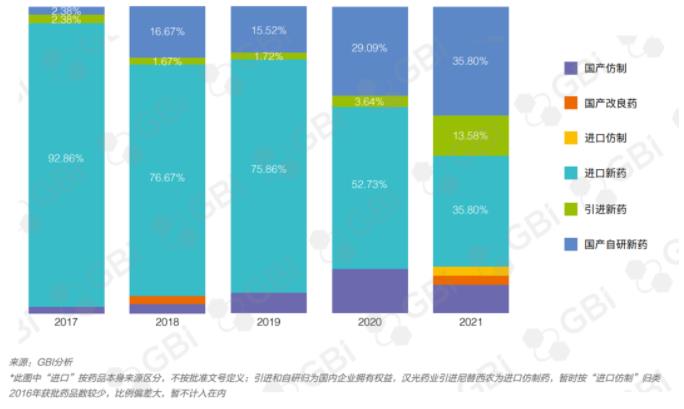
来源:GBI专题报告《2021年新药里程碑,国产创新厚积薄发》
然而,“新药研发,九死一生”,喜人成果的背后是较少被人们谈起的无数失败挫折。本期,小G根据GBI SOURCE资讯版块和公开信息,整理了2021年部分涉及国内药企的“挫折案例”,当中既有因市场竞争格局变化的主动终止,也有令人惋惜的三期临试失败,还有“扬帆出海”进程中的上市受挫。
市场格局变化,主动终止
百奥泰 BAT8001、BAT8003、BAT1306
2021年3月5日,百奥泰宣布决定终止针对候选抗癌药物BAT8003和BAT1306的临床试验。同年2月,由于III期临床试验未达到预设的优效目标,百奥泰还终止了乳腺癌ADC制剂BAT8001项目的后续临床开发。据悉,BAT8003项目的终止是由于Trop2抗体偶联药物领域的市场格局变化,BAT1306项目是因考虑到国内PD-1单抗研发赛道尤为拥挤,市场竞争过于激烈而终止。
复星医药 万格列净
2021年12月29日,复星医药发布公告称,旗下控股子公司万邦生化医药决定终止1类新药万格列净片的临床试验及后续开发工作。据悉,由于该新药目前尚处于I期临床试验阶段,而国内外SGLT-2抑制剂市场竞争已相对激烈,基于对新药后续开发投入和市场价值等因素的评估,万邦医药决定终止其开发工作。
基石药业 CS3002
2021年4月,据Clinicaltrials.gov信息,基石药业旗下在研CDK4/6选择性抑制剂CS3002在澳大利亚开展的开放性、多剂量、剂量递增与剂量扩展的I期临床研究已终止。据悉,该研究的终止系出于“战略及商业原因(strategic and business reasons)”。
最后关头,Ⅲ期临床失败
泽璟制药 多纳非尼
2021年8月17日,泽璟制药发布公告称甲苯磺酸多纳非尼治疗二线以上晚期结直肠癌Ⅲ期临床试验未达到预设的优效目标,决定终止多纳非尼单药治疗该适应证的进一步开发。多纳非尼是一种口服多靶点、多激酶抑制剂类小分子抗肿瘤药物,2021年6月多纳非尼一线治疗晚期肝细胞癌适应证获批上市。
开拓药业 普克鲁胺
2021年12月27日,开拓药业公布了普克鲁胺治疗轻中症非住院新冠患者Ⅲ期临床试验的进展。根据348例新冠患者的中期分析数据显示,由于事件数较少未达到统计学显著性。普克鲁胺作为一款雄激素受体(AR)拮抗剂和降解剂,目前正在开发用于新冠、前列腺癌和乳腺癌治疗的临床试验中。
康弘药业 康柏西普
2021年4月9日,康弘药业宣布停止康柏西普眼用注射液治疗新生血管性年龄相关性黄斑变性患者全球多中心临床试验。4月26日,康弘药业再发公告称,鉴于康柏西普国际Ⅲ期临床失败,公司2020年业绩净利润从8.4亿元变为-2.7亿元。
万事俱备,上市波折
万春药业 普那布林
2021年12月,万春药业普那布林美国上市申请遇挫,FDA指出普那布林提供的注册试验结果不足以证明其获益,需要进行额外的对照试验提供支持CIN适应证的实质性证据。公告当日,受此事件影响,万春药业美股股价暴跌61%。
传奇生物 西达基奥仑赛
2022年3月1日,传奇生物旗下CAR-T产品西达基奥仑赛获得美国FDA批准,商品名:CARVYKTI,成为国内首款成功出海的细胞治疗产品,也是全球第2款获批的BCMA CAR-T治疗。这一“出海”里程碑事件使业内备受鼓舞。然而西达基奥仑赛的美国上市之路也曾遇到波折,去年11月,FDA以“需要更多时间审查信息”延迟了西达基奥仑赛的上市审批,将处方药用户付费法案目标审评日期从2021年11月29日推迟至2022年2月28号。
Agenus 巴替利单抗
2021年10月,美国生物技术公司Agenus被FDA建议撤回其PD-1抑制剂巴替利单抗的上市申请,原因主要是默沙东的可瑞达联合化疗已经在此之前获得了相同的适应证许可,这意味着Agenus需要再开展完全双盲的临床试验。因此,Agenus放弃了巴替利单抗在卵巢癌中的开发,转而专注于联合疗法。这一消息对拥有该药的相关权益的贝达药业也造成了影响。
经得起失败,打有准备之仗
从近年来国产创新成果的落地情况,我们已经看到本土企业加速创新转型的决心。中国创新医药已踏上从拼数量(me-too)、拼速度(me-quicker)到拼质量(me-better)、拼创新(first-in-class)的进阶征程。
在这个过程中,就更需要相关从业人员耐得住寂寞,经得起失败。正如GBI首席顾问陈怡博士曾指出的:“要宣传创新文化,回归初心价值,激励科研精神,包容创新失败,因为有了包容,企业家才去做一些创新。如果我们的支付、我们的社会对创新药没有容忍失败的心态,大家都不敢做创新药,今后创新的难度会更大,也意味着失败率也越来越大。所以大家一定要有这种心态和理念,创新要有承担失败的勇气。”
此外,当国产创新的含金量逐步提高,企业必将会放眼更加广阔的海外市场,“出海”势在必行,此行任重道远且充满挑战。无论是因市场格局变化主动终止临床试验,还是在上市最后关头遭到当地监管部门的质疑,“先行者”已为“后继者”提供了经验与参考——提前布局,打有准备之仗。若企业有意拓展海外市场,需要将产品的出海布局在整体研发策略中前置考虑,在自身产品“过硬”的前提下,充分了解海外市场的竞争格局和监管政策等信息,努力降低从临床开发到上市各个环节遇挫的可能。毕竟,失败与挫折对于管线丰富的跨国药企巨头可能只是“阵痛”,但对于众多抗风险能力较低、“孤注一掷”且仍未实现商业化的Biotech来说,任何环节的失败都可能是致命一击。

 产业资讯
产业资讯
 瞪羚社
瞪羚社  2025-05-01
2025-05-01
 48
48

 产业资讯
产业资讯
 医药经济报
医药经济报  2025-05-01
2025-05-01
 49
49

 产业资讯
产业资讯
 药渡Daily
药渡Daily  2025-05-01
2025-05-01
 47
47