 产业资讯
产业资讯
 Insight数据库
Insight数据库  2022-03-07
2022-03-07
 3292
3292
据 Insight 数据库统计,2.28 - 3.5共有 29 款创新药研发进度推进到了新的阶段,其中 21 款为国产药。化药占到 9 个,单抗紧随其后,5 款有了新进展。
早期项目中,9 款新药首次获批临床,8 款新药首次启动临床;后期项目中,2 款新药进入 III 期临床,1 款新药首次申报上市。Insight 将摘取部分重点项目做介绍。
发生变化的创新药在研进度分布
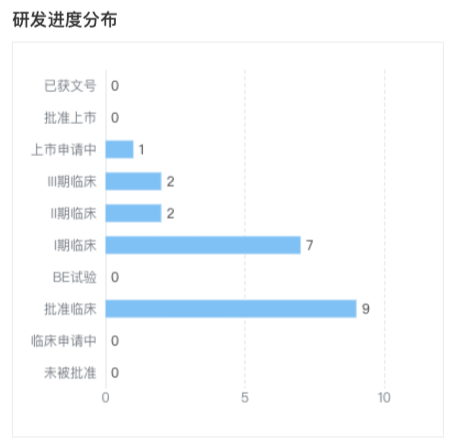
来自:Insight 数据库
1 款 1 类新药申报上市
2 月 28 日,四环制药 1 类新药「加格列净」上市申请获 CDE 受理(CXHS2200012)。这是国产第 2 款申报上市的 SGLT-2 抑制剂新药。SGLT2 抑制剂通过减少肾脏对葡萄糖的重吸收而降低血糖,是一类非胰岛素依赖性的降血糖药物。
据 Insight 数据库,这款新药在 2014 年首次提交 IND 申请,2017 年首次启动临床试验,临床开发历时近 5 年。
「加格列净」项目时光轴

来自:Insight 数据库
从国内来看,在降糖领域,小分子药物们无一不面临着激烈的竞争,各进口药多已在国内获批上市多年,并有相应仿制药上市,甚至进入集采。从 SGLT-2 靶点看,除 2020 年 7 月新上市的艾格列净之外,恩格列净、卡格列净、达格列净分别有 5、3、2 款国产仿制药获批。
尽管如此,仍有不少企业的 1 类新药还在冲刺中。恒瑞医药的恒格列净是最快冲线的同靶点新药,在去年 12 月 31 日刚刚获批,为国产首款,加格列净紧随其后。而 III 期临床项目中还包括东阳光药的荣格列净、赛诺菲的索格列净和 Theracos 的 Bexagliflozin。
2 款新药进入 III 期临床
1、康诺亚 IL-4R 单抗 CM310
2 月 28 日,康诺亚首次公示启动 CM310 用于中重度特应性皮炎的 III 期临床(登记号:CTR20220326),国内拟入组 500 人。
CM310 是康诺亚研发的一种抗 IL-4Rα 重组人源化单抗,通过与人白细胞介素 4 受体 α 亚基特异性结合,从而抑制炎症反应,用于中重度哮喘、COPD、特应性皮炎等适应症。该项目首次国内临床登记起始于 2019 年。
CM310 项目时光轴
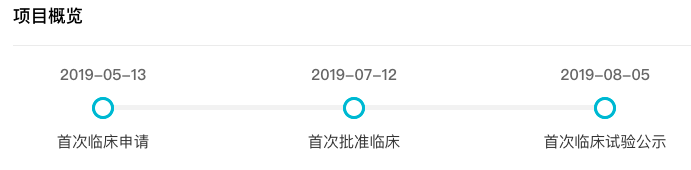
来自:Insight 数据库
2021 年 3 月,石药集团与康诺亚达成合作,获得 CM310 在不包括港澳台在内的中国地区针对呼吸系统疾病进行开发和商业化的权益,并成为上市许可持有人(MAH),这笔交易中康诺亚获得 7000 万元首付款 + 1 亿元潜在开发里程碑付款,后续还有望获得销售里程碑款和销售提成。目前,用于哮喘、慢性鼻窦炎伴鼻息肉病的适应症还处于 II 期临床开发中。
2、必贝特 CDK4/6 抑制剂
必贝特的 BEBT-209 本周首次启动 III 期临床(CTR20220426),联合氟维司群治疗 HR 阳性,HER2 阴性晚期乳腺癌患者。这是国产第 6 款进入 III 期临床开发的同类新药。
国内临床试验阶段 CDK4/6 抑制剂
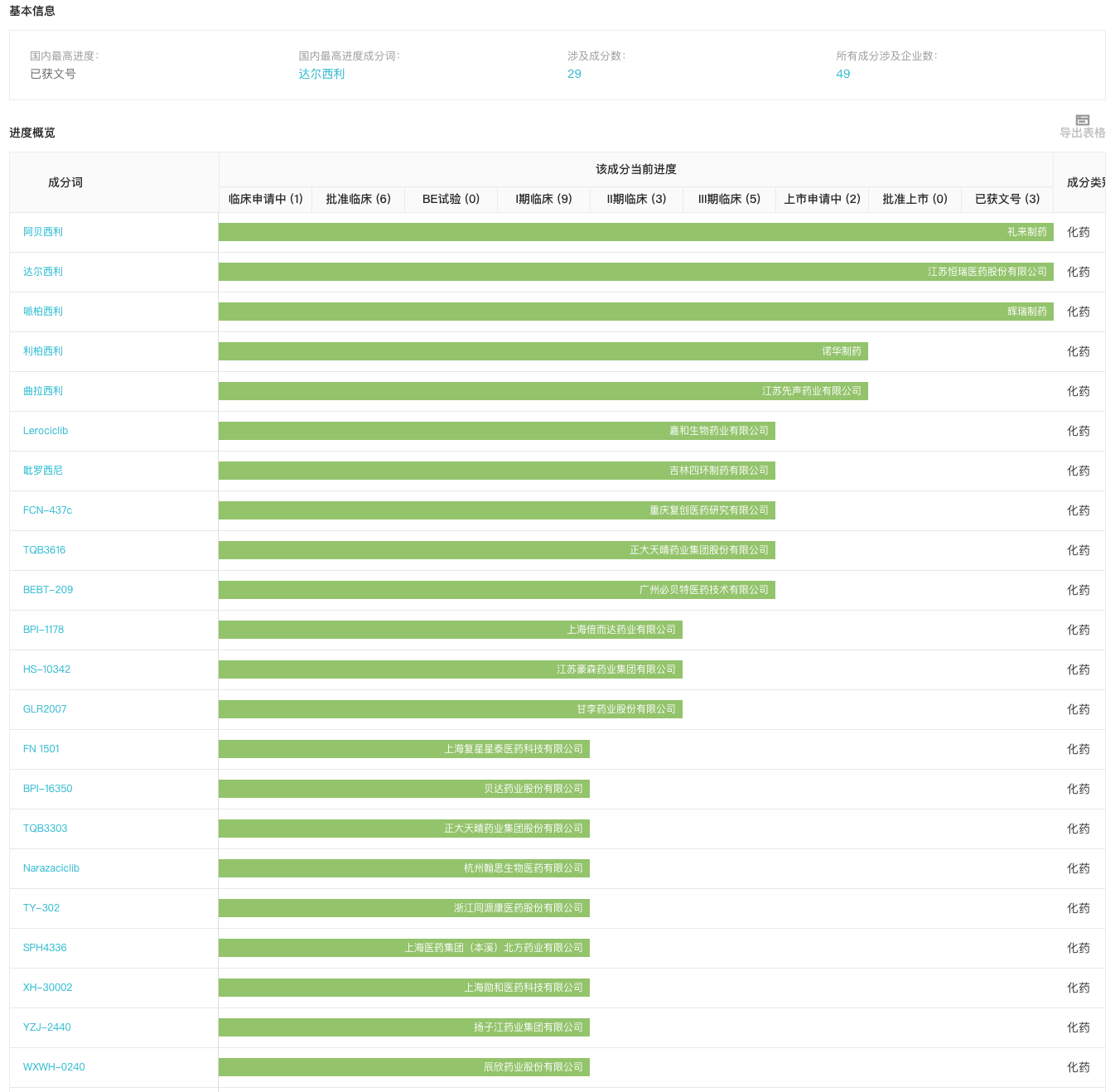
来自:Insight 数据库
8 款新药首次启动临床
1、百济神州 BTK PROTAC 启动临床
2 月 28 日,Insight 数据库显示,百济神州的 BTK 靶向 PROTAC 药物 BGB-16673 首次在国内启动临床(登记号:CTR20220399)。
从 Insight 项目开发时光轴可以看到,这款 PROTAC 新药最早在 2021 年 8 月即在国外启动了临床试验,国内首次 IND 申请则起始于 10 月,推进快速。目前,国内除百济神州外,海思科也拥有一款在研 BTK PROTAC 药物 HSK29116 散,2021 年 4 月启动了国际多中心临床试验。
BGB-16673 项目关键节点
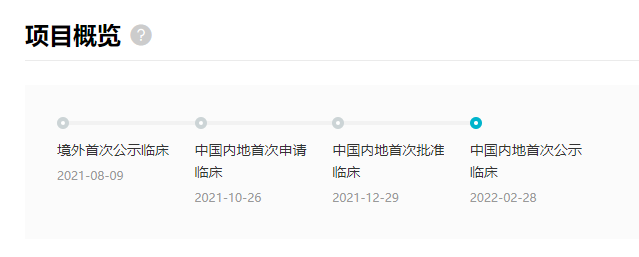
来自:Insight 数据库
2、君实生物 2 款新药启动临床
2 月 28 日,君实生物 CD39 单抗 JS019 首次在国内启动临床(CTR20220434)。这款新药项目由君实与北京恩瑞尼共同投资的苏州科博瑞君申报。
CD39 为负责在肿瘤微环境中将免疫刺激性细胞外三磷酸腺苷(ATP)转化为免疫抑制腺苷(ADO)的初始步骤的酶,在肿瘤微环境免疫抑制反应中扮演着重要角色。研究表明,CD39 在各种人类肿瘤中均呈现高表达现象,包括淋巴瘤、肉瘤、肺癌、胰腺癌、卵巢癌、肾细胞癌、甲状腺癌和睾丸癌等。
2020 年 9 月,君实生物与北京恩瑞尼订立合作协议,共同成立苏州科博瑞君负责 CD39 药物的研发、临床应用及商业化,双方各拥有苏州科博瑞君 50% 的权益,CD39 项目直接或间接产生的利益将按双方于苏州科博瑞君的股权比例分派。据 Insight 数据库 显示,JS019 在 2021 年 10 月首次在国内申报临床。目前,同靶点仅科望生物的 ES002 同样在国内获批了临床,但尚未登记临床试验。
JS019 国内关键节点
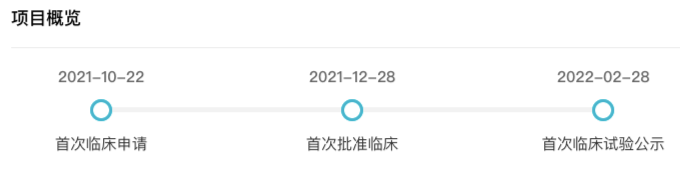
来自:Insight 数据库
3 月 3 日,君境生物的口服小分子 Aurora A 抑制剂 WJ05129(即 JS112)首次在国内登记启动 I/II 期临床试验(CTR20220398)。君境生物由君实生物与微境生物共同投资成立,WJ05129 是两家公司合作的 4 款抗肿瘤小分子药物之一,君实拥有其 50% 权益。
研究显示,Aurora A 抑制剂与 KARS G12C 抑制剂联用可以克服后者的耐药,与 RB1 基因缺失或失活具有合成致死的效果,可用于治疗小细胞肺癌和三阴乳腺癌等 RB1 缺失或失活的恶性肿瘤。WJ05129 也是国内首款进入临床的 Aurora A 抑制剂。
3、康方生物 NGF 单抗 AK115
3 月 3 日,康方生物首次在国内登记启动抗 NGF 单抗 AK115 注射液的 I 期临床(CTR20220431)。AK115 是康方生物首款疼痛管理领域新药,具备长效安全、无成瘾性等特征。康方生物将优先评估 AK115 在癌症晚期患者中的安全性和有效性,该药有望有效提高对阿片类耐药的癌症晚期患者的生活质量。
据 Insight 数据库显示,AK115 在 2021 年 11 月首次递交 IND 申请。目前国内共 4 款 NGF 单抗处于临床开发中,详见下图:
NGF 单抗国内竞争格局

来自:Insight 数据库
此外,本周新启动临床的国产创新药还包括海思科 HSK31679,用于原发性高胆固醇血症;广生堂 GST-HG151,针对 NASH;智翔金泰 CD3/BCMA 双抗 GR1803;步长制药子公司丹红制药 AGTR2 拮抗剂 WXSH0024,用于神经痛,该药为与药明康德合作开发。
还有 9 款新药在本周首次获批临床,其中包括 2 款双靶点降糖药,恒瑞医药的 SHR-1816 和鸿运华宁的 GMA106;复星凯特第 2 款 CD19 CAR-T 疗法,来自 Kite Pharma 的 Tecartus;轩竹生物的 HER2 双抗。篇幅有限,在此不再赘述,可通过 Insight 数据库 小程序及网页版查询项目详情,公众号也会持续追踪。

 产业资讯
产业资讯
 医药财经
医药财经  2025-10-14
2025-10-14
 654
654

 产业资讯
产业资讯
 医药魔方Invest
医药魔方Invest  2025-10-14
2025-10-14
 664
664

 产业资讯
产业资讯
 同写意
同写意  2025-10-14
2025-10-14
 630
630