 产业资讯
产业资讯
 动脉新医药
动脉新医药  2022-09-09
2022-09-09
 5736
5736
伴随着基因和细胞治疗(Cell and Gene Therapy,下文简称CGT)成为各大药企争相布局的下一个决胜点,CGT CDMO赛道也被誉为是下一个“十年十倍”的黄金赛道。Frost & Sullivan预估,到2025年,全球细胞和基因治疗CMO/CDMO市场将达到101亿美元,2020年至2025年的复合年增长率为34.9%。
极具诱惑的市场蛋糕吸引大量玩家入局。据动脉新医药不完全统计,截至2022年7月底,国内已经有19家公司争相入局CGT CDMO赛道,包括药明康德、康龙化成、博腾股份、凯莱英等国内一众CXO龙头全部入局。
2022上半年,不仅是诸多新玩家陆续进场,资本市场也表现地十分热情——据动脉新医药不完全统计,2022年上半年CGT CDMO市场融资总金额达到40.25亿元,是2021年CGT CDMO市场全年融资总额(19.7亿元)的2.04倍。背后主要原因在于和元生物的上市,以及凯莱英拟与高瓴创投、海河凯莱英基金等达成合作协议,向凯莱英生物合计增资近26亿元大手笔高调布局CGT CDMO赛道。
然而,在CGT CDMO赛道火爆的表象之下,潜藏着部分隐忧。
动脉新医药观察到,为了增强自身业务能力,满足日益严苛的行业监管法规以及客户的生产需求,几乎所有的CGT CDMO都铆足劲地建立大型GMP厂房车间,进行产能的扩张、再扩张。
正在进行快速扩张的CGT CDMO企业似乎并没有意识到未来市场可能面临的“供过于求”情况。CGT产品个体化差异大、生产批量小,订单小;另外,当下一些头部CGT企业选择自建产能,再考虑到今后该领域还不断有新玩家入场——部分抗体药物研发企业、CGT企业以及CGT CRO企业向CGT CDMO转型的可能,未来CGT CDMO的市场将被进一步瓜分。
扎堆的CGT CDMO,有限的CGT CDMO市场。究竟哪些企业能“笑”到最后?行业的下一步,应该怎么走?CGT CDMO行业火热发展势头之下,正在进行产能扩建的创业者、正在广泛布局的投资者,或许应该多一份冷静和理性。
CGT赛道发展火热,引发CGT CDMO供不应求
近几年,伴随着多款CGT产品的相继获批,全球对于CGT产品的研发热情节节攀升,CGT领域成为各大药企争相布局的下一个决胜点。据《Alliance for Regenerative Medicine 》数据统计,2020年处在临床研发阶段的细胞和基因疗法药物的数量为1220项,相比2015年的631项实现了翻倍。
FDA预测,2020至2025年每年将会有10-20个CGT药物获批上市,预计2025年全球CGT市场规模突破300亿美元(2020-2025年CAGR=71%)。
CGT市场的火爆,吸引了大批的“掘金者”,CGT研发企业如雨后春笋般出现,同时也催生了“卖水人”CGT CDMO的春天。Frost & Sullivan预估,中国的细胞和基因治疗CMO/CDMO市场将成为全球增长最快的市场,2020年至2025年的复合年增长率预计将达到51.1%。
在广阔市场前景的吸引下,越来越多的新玩家涌入CGT CDMO赛道,2022年尤甚。

近三年,进场CGT CDMO领域的新玩家既包括像康龙化成、凯莱英一类向CGT CDMO领域进行跨界布局的传统CXO龙头,也包括通过分拆子公司的形式(蓬勃生物、谱新生物、希济生物等)进军CGT CDMO赛道的国内头部生物科技公司(金斯瑞生物、普瑞金生物、艺妙神州);此外,成长于中国本土或从海外留学/工作归来的初创CGT CDMO团队也是行业重要力量。
我们观察到,近三年加入CGT CDMO赛道的企业(9家)尤其密集,几乎是当今CGT CDMO企业总数量(19家)的一半。
火热进场的背后,是来自资本的热情支持。
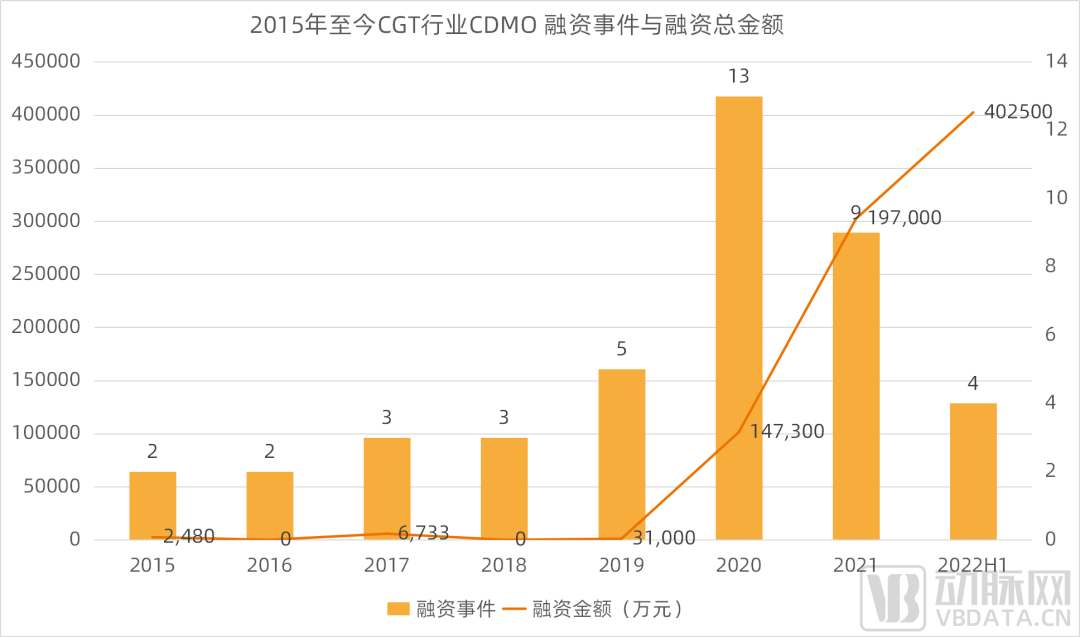
▲ 注:在本次统计中,融资额未披露事件的融资金额均计为零;融资额为数千万元/逾千万元均计为1千万元;融资额为数亿元/逾亿元/超亿元均计为1亿元。
从上图可以看到,自2015年开始,CGT CDMO领域融资一直保持上涨态势。其中,2020年可以看作是CGT CDMO市场的转折点——相比2019年,2020年的融资事件数量是2019年融资事件数量的2倍多,融资总额是2019年的近5倍。(由于部分企业融资未透露具体金额,因此存在有融资事件存在但融资金额为零的反常情况。)
从近三年的情况来看,2022年表现地尤其出彩——2022年上半年的融资总金额已然是2021年全年融资金额的2.04倍。2022年,资本市场表现出彩的背后的原因主要在于和元生物的上市以及凯莱英在CGT CDMO领域的高调入局。
2022年3月22日,和元生物登陆科创板,被产业人士称作“科创板CGT CDMO第一股”。上市当天,公司募资总额为13.23亿元。2022年3月25日,凯莱英发布公告,拟与高瓴创投、海河凯莱英基金等达成合作协议,向凯莱英生物合计增资不超过25.34亿元,从而将凯莱英生物打造成为全球生物药及先进疗法CDMO的领军企业。
赛道火热的另一个表象是,部分CGT CDMO企业对行业的需求应接不暇。
诸如药明生基等头部CGT CDMO企业,根本无暇承接国内部分初创CGT企业的订单。“遥远的订单排期着实让我们等得伤心,而CGT企业在发展初期,产品开发速度又格外关键。”一位不具名的CGT企业员工透露说。此外,动脉新医药还了解到,在今年4月份的时候,宜明细胞的企业订单都已经排到了9月开外。
因此,建立GMP车间,扩充产能,是CGT CDMO行业近两年的“主旋律”。

但“远水”解不了“近渴”,GMP车间的建设与产能的扩充,不是一两天就能解决的事情。
宜明细胞创始人李琦琛告诉动脉新医药,一个企业从从开始筹划建设GMP厂房到可以正式接单,至少需要1年半到2年的时间。
李琦琛介绍,建设GMP厂房首先需要寻找符合标准的场地载体,这得花不少时间。找好场地之后要开始设计,“没有4-6个月的时间,做不出一个好的工业设计来。”设计之后,还面临GMP车间的洁净装修,这又需要最少半年时间,“用8-12个月时间进行装修工作都很常见。”
另外,装修期间还要做好设备采购,在双线并行不耽误的情况下,最终还要进行厂房的验收、小试工艺的确认等。整体来看,“有能力在一年半的时间走完整个流程,算是非常牛的团队。”
然而,正是由于“水”在远、“渴”在近,整个行业都埋着头、卯着劲匆匆向前进发,似乎压根儿没有注意到身边已经有多少同行者。
行业开始往不太理性的方向发展,近似于创新药领域的“靶点扎堆”。
未来,可能不需要这么多的CGT CDMO和产能
当前已然入局的19家CGT CDMO在产能扩张上动作一致,再加上未来可能入局CGT CDMO领域的其他企业,引出一个新问题,未来是否真的需要这么多CGT CDMO和他们建立的庞大产能?
此前CGT CDMO行业的供不应求会不会变成未来的供过于求,甚至供过于求?如果国内的CGT CDMO企业不参与到国际竞争、单倚靠国内的CGT CDMO市场,在更多新企业不断入局的情况下,国内的CGT CDMO市场蛋糕似乎不够分。
首先,相比传统药物,细胞与基因药物个性化需求高、产量小、需求不稳定,不同产品之间技术壁垒大,技术的高门槛以及生产的小批量其实难以支撑大量CGT CDMO生存。且国内CGT领域目前还处于早期研发阶段,大部分管线用不到太大规模的生产体量。
一位资深的CGT领域业内人士告诉动脉新医药,CGT产品跟抗体类大分子药物在生产上很不一样。“抗体类大分子药物是‘货架式’产品,可以完成集约式生产,技术含量相对不高。但CGT产品因为个体差异大、生产批量小,相比抗体类大分子药物,所需产能并不高,并且要求产品的前段研发和后端生产合作必须非常紧密。”
亦诺微医药董事长兼CEO周国瑛也表示,做病毒药物研发的“路数”跟做一般的抗体完全不一样,没有普遍规律可循。“做病毒药物研发的门槛很高,因为每种病毒的生物学功能、抗肿瘤原理、特点都完全不同。CGT产品个性化的特点决定了它不可能按照一个产品的模式批量生产。”
“两类产品在量的需求上差别蛮大的。”国内某CGT企业核心高管以临床阶段所需的药品用量向我们举例说明:在条件同样的情况下,一家CDMO公司生产一批抗体类产品,对于一家抗体药企业开展临床3期试验来讲可能存在用量不够的情况,但对于一家CGT公司而言,生产的同样产能的CGT产品可能足够其开展I-III期临床试验甚至还有结余。
此前,动脉新医药曾专门撰文探讨过和元生物为什么能成为中国CGT CDMO第一股(详见《两家溶瘤病毒订单撬动一个IPO,给国内CGT CDMO带来哪些启示?》),其中一个很重要的原因在于,和元生物的主营业务是溶瘤病毒业务——这家公司主要依靠开展溶瘤病毒CDMO业务做大做强。
亦诺微医药周国瑛介绍,溶瘤病毒一个很大的特点在于,它不是一种个体化治疗,而是类似通用型治疗,因此对溶瘤病毒产品的生产体量要求比较大,相对需要CDMO企业承担的任务更重。
从和元的招股书我们也可以看到,和元也布局了其他CGT业务,但相应营收占比并不大——比如,和元在细胞治疗方面的客户不少,但没有一家是像亦诺微医药、复诺健这类的大客户。
“此外,国内CGT市场大部分管线还处于临床早期研发阶段,商业化生产规模的CDMO订单放量仍需时间。”中平资本孔令赫表示。
其次,由于当下大多CGT CDMO企业能力有待提升,以及CGT一类生物技术产品工艺往往涉及商业机密,不能对外透露,因此许多CGT企业会选择产能自建,进一步降低了对CGT CDMO的需求。
虽然CGT行业经历了起起伏伏、已经发展了近30年,但我国其实是在2017年左右才把CGT纳入药物监管,2018年左右,国内才开始有企业系统布局CGT药物。
基因与细胞治疗作为生物制药领域的新兴技术,到目前为止,从产业化的角度来看还是处于一个相对比较早期的发展阶段。国际CGT人才不多,中国CGT人才则更加紧俏。除了少数在CGT领域有数十年科学研究或工业界经验的科学家或产业人士,大部分CGT团队的能力仍有较大进步空间。
瑞风生物CEO梁峻彬回忆,当初公司在开发针对地中海贫血的基因编辑疗法时,原本是想要通过和一些CGT CDMO达成合作共同进行产品在生产端的制造,但由于没有找到合适的合作伙伴,最终还是依靠内部团队承担了相应业务。
“当时很多CGT CDMO公司对我们公司所做的新产品不熟悉、不了解,甚至没有任何概念。由于没有直接经验,他们的能力又没有得到验证,深入的战略合作其实没有办法展开。”不过,瑞风生物最终找到了一些外部合作方进行部分非核心原料的供应。
“如果从产品本身来讲,目前国内大部分CGT CDMO公司基本上是能够做出满足国内IND报批要求的产品。但由于CGT领域还比较新,目前国内大多CGT CDMO的能力还没有经过验证,很多方面仍有待完善。”
目前,瑞风生物也在尝试与国内CGT CDMO企业建立更进一步的合作关系,他们希望借助这些企业的现有厂房和硬件设施、包括一些通用能力,结合自身在产品开发上的认知和研发优势,实现两个团队的双赢。“我们认为,当下CGT企业与CDMO的合作,本身是在帮助产业链进行不断的完善。需要大家携手共进,产业才能发展地更好更快。”梁峻彬说道。
从国外CGT市场情况来看,CGT企业在发展早期委托CDMO,在后期到晚期临床商业化阶段会陆续开始自建生产厂房,将终产品“放在自己手里”。这种现象非常明显,国内同样表现了这种趋势。
对于CGT企业而言,产品的核心工艺往往因为涉及商业机密不能对外透露,需要“抓”在自己手里。因此,CGT企业一般会自己做终产品,而只是将质粒、病毒载体等当作定制化原材料委托CDMO生产。
在企业成立早期,团队缺钱少人。而搭建GMP产能厂房及配套设施需要资金,需要人才,需要经验,需要时间,这些初创公司都缺。另外,产品报批IND也面临失败风险。因此,在缺乏团队经验及厂房设施而且面临不确定性风险的情况下,初创企业对CDMO报有强烈需求——利用其已经建好的GMP厂房及设施,完成符合IND审批要求的CGT样品生产。
但一旦CGT企业有一两款产品顺利进入临床(或者到达某个里程碑),其面临的时间竞赛没有那么紧张,在公司厂房及团队各方面齐全后,CGT企业一般会将产品拿回来自己做,而仅仅将质粒病毒等非核心原料继续委托给CDMO。我们注意到,国内朗信生物团队便是采取了此类做法。
2022年7月,朗信生物旗下上海朗昇生物产品LX101注射液完成I期临床首例受试者给药。据动脉新医药了解,在进行该款产品的IND申报过程中,朗信与宜明细胞、派真生物两家国内CGT CDMO企业达成了战略合作。但朗信团队其实在2021年初就已经建成近5000平米的研发与生产基地,该基地于2021年5月就正式投产,在同年10月便实现了200L AAV规模产品的生产和放行检测。朗信生物汪枫桦博士曾在此前的专访中向我们介绍,朗信目前的第二款产品,包括IIT研究所需样品,已经实现了自主生产。
当然,CGT企业选择自建产能的因素还包括很多,比如能够使项目的推进速度变得更快、质量更高、降低终产品成本;能够更加灵活地调整产品需求与生产之间的关系;在CDMO面临突发问题导致生产停滞的情况下,CGT企业自身有能力及时承担起生产业务,降低产品生产风险,保证临床到商业阶段的样品生产不间断等等。
考虑到未来部分CGT/CGT CRO以及其他领域的企业会向CGT CDMO转型的情况,CGT CDMO的有限市场被进一步瓜分。
“目前抗体药都做‘烂’了,未来一批做抗体药的公司肯定会往这个赛道转;一些CRO也会把‘手’向这个领域延伸;另外,一些做CGT药物内卷失败的公司也可能往这个赛道‘挤’。多方力量卷入,国内CGT CDMO的市场蛋糕可能不够分。”一位不具名的CGT企业研发生产总监表达了他对未来CGT CDMO市场将面临激烈竞争的担忧。
结合产业调研,我们也发现,国内CGT CDMO领域可能要面临的激烈竞争,已经不仅仅是对未来的担忧,而是当下就开始有所显现。身处其中的一些CGT CDMO企业感受尤其强烈。
“有一段时间,IIT的订单在恶性竞争的冲击下,价格被压到特别低——比如我们正常报价二三百万的订单,有些企业压低到50万。这还怎么竞争?”宜明细胞李琦琛的话语间透出一丝无奈。
“50万,严格按照GMP体系来运营可能成本都不够。对于宜明细胞来讲,我们严格要求公司生产的所有产品,只要是用给人的,无论是IIT还是IND,都严格按照GMP标准进行生产,所有试剂耗材一律按照法规要求非常严格。即使IIT所用样品不像IND需要三批次、对方法学开发要求不多、不需要建三级库,但其他所有用到的试剂、耗材、团队、环境、仪器设备等都是跟IND申报产品标准一致,成本根本降不了那么多。”
好在宜明在CGT CDMO行业耕耘多年,在AAV腺相关病毒方面建立起了独特的技术优势且有多个成功交付案例在手,IND订单是其主流服务类型。因此受IIT的价格竞争战影响会小一些。
但李琦琛也道出他的担忧,“无论报价多少,CDMO服务必须要在GMP体系下进行生产,必须要达到国家药监局要求的药物标准。太低的报价如果对成本的涵盖有影响,保证质量标准可能会受到挑战”。过度的价格战可能会有损行业的发展。
行业下一步,怎么走?
无疑,CGT CDMO行业非理性的产能扩张已然埋下隐忧的种子。那么,对于身处其中的企业而言,下一步怎么走很重要。
或许我们可以从全球CGT CDMO市场的发展局势中窥见一些启示。
遥望全球市场,大部分市场被几家CGT CDMO龙头占领,剩余市场被众多具有特色业务的中小型CGT CDMO分割。据某二级市场证券机构统计,全球细胞和基因治疗CDMO赛道相比传统CXO赛道集中度更高,Lonza、Catalent、赛默飞世尔、药明系这几家排名前四的企业,所占全球市场份额已然逼近50%。
对于国内有相当实力的CGT CDMO龙头而言,战略布局或许毋须多言,公司的品牌体系以及资本就已经在其中起到相当大的赋能。这一类企业最重要的是将体系和能力进行横向延伸,进行全领域布局。
CGT领域包含很多方向,比如CAR-T、TCR-T、TIL、AAV、腺病毒、溶瘤病毒以及mRNA 小核苷酸等,由于这些细分赛道的差异很大,最大的担心还是监管严格,因此没有一个赛道有确定性,头部CGT CDMO需要充足的储备在各个方面都有布局,以便在日后有爆火的赛道时,迅速跟上。
对于中型CGT CDMO而言,在已然形成差异化技术优势的情况下,可以根据市场需求判断未来潜力CGT细分领域,适当做有选择的横向业务扩张。与此同时,提升自身的业务能力以及产品交付标准,在工艺、合规等方面努力得到像FDA、欧盟这样的国际审批机构的认可,参与国际化竞争,开拓海外市场。
已然形成差异化技术优势的CGT CDMO企业需要根据自身情况选择性地押宝新技术。和元生物能够成为科创板CGT CDMO第一股,其中一个很重要的原因即是其抓住了溶瘤病毒的业务机会,这与其此前在相关领域的努力与准备分不开。任何行业,机会总是留给有准备的人。
与此同时,在国内CGT CDMO赛道已趋饱和的情况下,将眼光放远,参与全球竞争是未来发展的必然路径。国内市场前景很大,产业期望也很大,但目前CGT领域毕竟还处于早期研发阶段,大部分管线用不到当前太大规模的生产体量。
对于正在进步阶段的小型CGT CDMO而言,精进自身业务能力、建立特色业务、找准自身定位是当前布局首要。广开“炉灶”、广扩产能只会快速透支小型CGT CDMO本就不多的资源。什么都做,不容易构筑优势;做得好比做得广更重要。
“CGT行业大的发展趋势是往上走,但往上走的过程中可能面临起起伏伏。在这些起起伏伏中,参与其中的每家企业都需要做好准备,否则就面临被淘汰出局的风险。无论是手头资金的使用,还是业务布局,眼光远方能走得长。”以宜明细胞李琦琛总的一段话为本文收尾。往以上分析和建议能够给产业相关人士带来些许思考。
特别鸣谢以下产业人士为本文内容做出贡献:
宜明细胞联合创始人李琦琛
瑞风生物CEO梁峻彬
亦诺微医药董事长兼CEO周国瑛
中平资本孔令赫
其他未具名的产业人士
(以上排名不分先后)

 产业资讯
产业资讯
 BiG生物创新社
BiG生物创新社  2026-06-02
2026-06-02
 424
424

 产业资讯
产业资讯
 氨基观察
氨基观察  2026-06-02
2026-06-02
 416
416

 产业资讯
产业资讯
 药智网
药智网  2026-06-02
2026-06-02
 409
409
 热门资讯
热门资讯