 医改专题
医改专题
 GBIHealth
GBIHealth  2023-01-06
2023-01-06
 4644
4644
万众期待的2022年国家医保目录调整现场谈判环节于昨日开启。据21世纪经济报道消息,谈判首日全国人大会议中心门口人头攒动,上午8时左右陆续有企业进场。据悉,5日上午约10家药企进行谈判,包括大冢制药、以及首次参加谈判的科伦药业等。
GBI此前曾梳理过本次医保谈判的几大亮点,2022年医保谈判国产PD-(L)1竞争格局,以及通过形式审查的新冠相关药物信息。本期,小G将盘点即将参与今年医保谈判的抗体偶联药物(ADC),包括一款目录内国产药品,和三款目录外跨国药企产品。
荣昌生物维迪西妥单抗:首款国产ADC
维迪西妥单抗(商品名:爱地希)是一款抗HER2的ADC,也是首款获批上市的国产ADC。GBI既往报道,该药于2021年6月9日获NMPA附条件批准,用于至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃癌及胃食管结合部腺癌(G/GEJ)患者的治疗。2021年医保谈判中,维迪西妥单抗进入医保乙类目录。据GBI SOURCE全球药品数据库【谈判药品价格趋势分析工具】,该药首次谈判价格从13500元降至3800元,降幅高达71.85%。
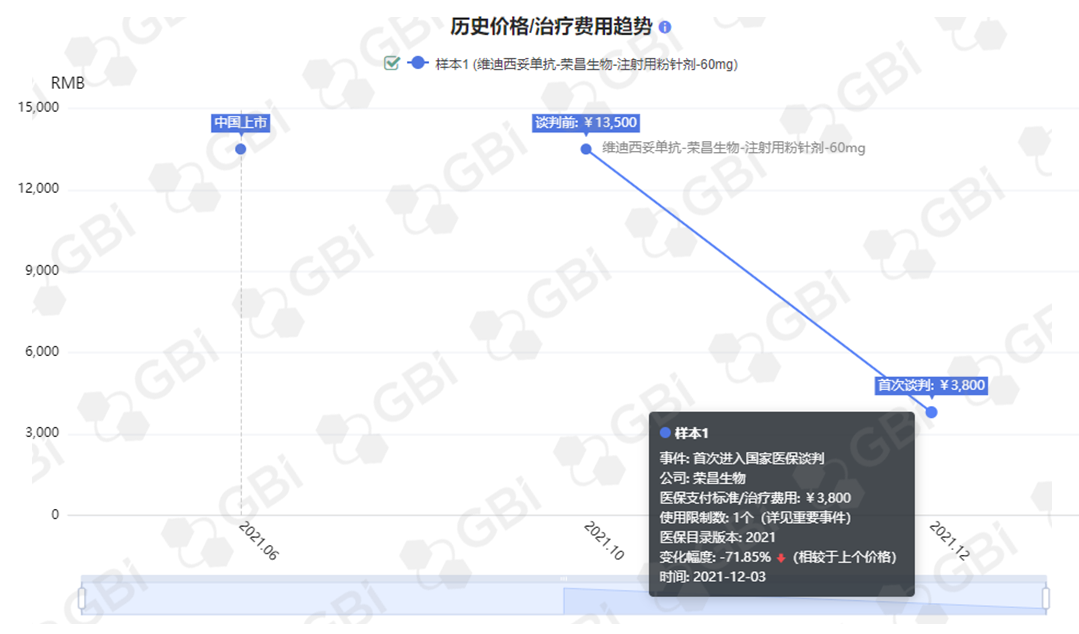
来源:GBI SOURCE全球药品数据库
本次医保谈判维迪西妥单抗拟新增适应证为用于既往接受过含铂化疗且HER2过表达局部晚期或转移性尿路上皮癌的患者,该适应证于2021年12月31日获NMPA附条件批准。

来源:http://www.nhsa.gov.cn/
在美国,维迪西妥单抗已获FDA授予用于治疗局部晚期或转移性尿路上皮癌的突破性疗法及快速通道资格认定。目前荣昌生物还在就维迪西妥单抗针对多项HER2表达癌症适应证进行开发。
罗氏恩美曲妥珠单抗:一年内2次降价
罗氏旗下注射用恩美曲妥珠单抗(商品名:Kadcyla,赫赛莱)于2020年1月获NMPA批准上市,单药适用于接受了紫杉烷类联合曲妥珠单抗为基础的新辅助治疗后仍残存侵袭性病灶的HER2阳性早期乳腺癌患者的辅助治疗,是国内首个获批的ADC。

来源:http://www.nhsa.gov.cn/
据悉,赫赛莱获批上市后的定价为19282元(100mg)以及27633元(160mg)。2020年该药被纳入通过形式审查的药品名单,但未谈判成功。2021年赫赛莱未参与国家医保谈判。然而今年以来,该药两次降低挂网价格,首次在3月,其100mg和160mg规格的价格分别降至9200元和13184元,此后6月又再度降至8340元和11951.63元。
业内有声音认为,罗氏此举是为了积极应战2022年医保谈判。另外值得关注的是,赫赛莱在中国市场的潜在竞争对手——阿斯利康/第一三共的ADC产品德曲妥珠单抗(英文商品名:Enhertu)接连取得积极进展。GBI既往报道,2022年12月,阿斯利康和第一三共联合公布了德曲妥珠单抗与赫赛莱的头对头III期试验DESTINY-Breast03的最新结果。结果显示,在HER2阳性转移性乳腺癌患者中,德曲妥珠单抗显著提高了总体生存率(OS),并且降低了36%的死亡风险,表明该药物有成为乳腺癌治疗新标准的潜力。德曲妥珠单抗已在美国获批五项适应证,虽然尚未在中国获得批准,但目前至少有两种适应证申请正在审查中,包括HER2低表达乳腺癌。若获批上市,将成为赫赛莱在国内市场的强劲对手。
辉瑞奥加伊妥珠单抗:
中国首个且唯一治疗急淋的CD22靶向ADC
辉瑞旗下白血病创新药注射用奥加伊妥珠单抗(商品名:贝博萨)是一种靶向CD22的ADC,于2015年10月被美国FDA授予在ALL治疗上的“突破性治疗”资格,2017年在欧盟和美国获批。2021年12月,贝博萨获NMPA批准,用于治疗R/R B-ALL成年患者,是中国首个且唯一治疗急淋的CD22靶向ADC产品。


来源:http://www.nhsa.gov.cn/
2022年6月27日,辉瑞宣布贝博萨已在全国多个城市开出首批处方,标志着全球首个复发性或难治性前体B细胞ALL(R/R B-ALL)的ADC正式落地,惠及我国ALL患者。
武田维布妥昔单抗:国内第2款ADC
武田旗下注射用维布妥昔单抗(商品名:安适利)是全球唯一获批的靶向CD30 ADC。该药于2020年5月获NMPA批准,用于成人CD30阳性的复发或难治性系统性间变性大细胞淋巴瘤(sALCL)和经典型霍奇金淋巴瘤(cHL)的治疗,成为国内第二款ADC。7月23日,该药在中国开出首张处方正式上市,零售价22075元/盒。2021年4月,维布妥昔单抗获批针对皮肤T细胞淋巴瘤的两项新适应证

来源:http://www.nhsa.gov.cn/
更多2022年医保谈判信息,GBI将持续追踪。
 医改专题
医改专题
 MedTrend医趋势
MedTrend医趋势  2026-03-04
2026-03-04
 32
32

 医改专题
医改专题
 中国医疗保险
中国医疗保险  2026-03-04
2026-03-04
 30
30

 医改专题
医改专题
 村夫日记LatitudeHealth
村夫日记LatitudeHealth  2026-03-03
2026-03-03
 82
82