 产业资讯
产业资讯
 智慧芽新药科讯
智慧芽新药科讯  2023-03-10
2023-03-10
 3973
3973
两个月前,由Biogen与卫材合作开发的Lecanemab获得FDA加速批准,用于治疗阿尔兹海默病,继Aducanumab之后,Biogen与卫材又收获了一款同机制用于治疗阿尔兹海默病的药物。
正是在两年前,FDA宣布批准Aducanumab,作为首个可能改变阿尔茨海默病进程的药物,上市前一众分析师认为其能披荆斩棘朝着千亿蓝海市场奔去,但后面的狗血剧情也几乎引起了FDA历史上最大争议。
众多医生联合起来拒绝处方、医保支付端直接拒绝支付、销售额大跌眼镜、美国国会介入调查、合作伙伴离场,一系列事件几乎宣布了Aducanumab的死刑。
两年后的今天,尽管Lecanemab的临床数据更具有说服力,但在上周,美国医疗保险和医疗补助服务中心(CMS)宣布,仍旧大概率选择将其和Aducanumab一样,可以将Lecanemab纳入医保范围,但附带了一项严苛的限制,即该药物仅用于参与临床试验的患者。
不过Biogen与卫材对Lecanemab还是充满信心,在获得FDA加速批准之后,就在前两天Lecanemab获得了FDA优先审评资格,这也就意味着FDA将在今年7月6日前对其作出是否完全批准的决定,换句话说,也许在不久之后Lecanemab有机会获得CMS认可。
此时恰逢国内新一批医保目录又正式落地,也正是在一年多前,同样具有极大争议的九期一(甘露特钠胶囊)正式被以超过60%的价格纳入医保目录,从895元/盒直接降至296元/盒,如今一年多时间过去,尽管九期一开发者绿谷制药并未公布销售额,但从各个途径不难了解到,进入医保后其完成了快速放量。
图:九期一正式纳入医保(来自绿谷官网)
21世纪以来,在前二十年阿尔茨海默病的药物研发几乎毫无进展,近几年九期一、Aducanumab以及Lecanemab的获批,本该真正的为患者带来曙光,但事实却让人大跌眼镜,从临床数据、药物审批、医保支付甚至是更深层次的因素,均争议不断,我想,这并不是数以亿计的阿尔兹海默病患者真正愿意看到的。
回首过去,直面现在,当讨论阿尔兹海默病药物时,我们究竟在期待什么?
01 两场豪赌
时间倒回到二十年前,绿谷制药在创始人吕松涛带领下,早期以被宣称为“有抗癌功效”的保健品——“中华灵芝宝”为旗下主力,随后又将推向市场,当时得益于产品的销售快速增长,绿谷年产值迅速升至10亿元,2003年更成为上海市工业企业集团50强之一。
但随着接连被爆出中华灵芝宝涉嫌虚假宣传以及双灵固本散数百次被列入国家级违法药品广告公告,绿谷以涉嫌虚假宣传以及假药风波迅速被卷入舆论漩涡,旗下的重点产品管线也几乎被全面叫停。
于是在2009年,绿谷制药与中科院上海药物所签订“GV-971”(“九期一”药品早期研究时使用的代码)全球开发许可合同,总金额达数千万美元,根据后期吕松涛的介绍,绿谷制药对此项目进行了一场豪赌,累计投入30亿元,用于药物研发、临床试验及上市申报等工作,远高于目前国内一款创新药的研发投入,但真实程度还是难以确认。
目光转移到太平洋彼岸的马萨诸塞州,作为一家由两位诺贝尔奖得主创建的公司,Biogen已经在风雨中稳定发展了近二十年时间,随着1996年公司首款重磅产品Avonex(干扰素β-1a)获批上市,2002年成为重磅炸弹之后公司依靠Avonex实现了快速的成长,拥有足够现金后开始对外收购以扩充管线,于是在2007年,Biogen从Neurimmune许可引进阿尔茨海默病药物Aducanumab。
尽管Biogen也没有公开Aducanumab的研发成本,但据医药市场调研机构Evaluate估计, Aducanumab临床试验耗资16.3亿美元,总研发投入可能要高得多,几十亿美金的投入,也是Biogen对自身命运的豪赌。
作为一家由营销商人创建的本土公司,在接连遭受清算之后,绿谷需要为自己的营销行为付出代价,与GV-971的不期而遇,也几乎预示着彼时绿谷的破釜沉舟。
而作为真正意义上由科学家创建的Biotech,Biogen需要为自己成为一家真正意义上的Biopharma甚至是Bigpharma增添一剂猛药,于是双方几乎在同个时间线对阿尔兹海默病发起了冲锋,这一场拉锯战,也持续了数十年。
02 殊途同归
以阿尔兹海默病为代表的神经退行性疾病一大特点就是发病机制很不明确,这也是阿尔兹海默病研发几乎九死一生的重要原因之一,所以药物作用机制也基本围绕着发病假说来进行,九期一以及Aducanumab也不例外,以九期一为代表的脑肠轴假说以及以Aducanumab为代表的淀粉样蛋白假说,也在不同的领地进行着临床验证。
以虚假宣传的正义公司为开发主体,九期一的研发必定一直在闪光灯下,再加上核心研发者被多次质疑学术造假以及临床涉及被广泛质疑,算是buff叠满。但在2019年,国家药品监督管理局仍旧有条件批准其作为国家I类新药上市,顶着一众质疑,九期一完成上市,进入医保,逐渐开始放量。
Aducanumab则没这么好运,遭遇两项临床研究结果矛盾后进行中期数据分析的一波三折,Aducanumab奇迹般也获得FDA的加速批准,于是就发生了迅速的业界震荡,监管机构FDA饱受批评,几位审评员愤而离职。
前文已经提到,众多医生联合起来拒绝处方、医保支付端直接拒绝支付、销售额大跌眼镜、美国国会介入调查、合作伙伴离场,就目前来看Aducanumab大概率已经被直接宣判死刑,Biogen也宣布停止了其真实世界研究。
在国内基本达到预期之后,绿谷在当时也计划布局国际市场,向Aducanumab所在的美国领土也发起冲击,FDA也批准了九期一的Ⅲ期临床试验申请,在安全性上似乎也获得了认可。但后来的故事为人熟知,绿谷表示受脱落率增高、资金等因素影响,目前在研的九期一国际多中心三期临床试验将提前终止,国际化宣布闯关失败,也让九期一是否能通过FDA监管的疑问告一段落。
尽管在Aducanumab上,Biogen遭遇了彻彻底底的失败,但也正因为有在Aducanumab技术以及临床上的沉淀,同靶点药物Lecanemab在今年获得了FDA的加速批准,同时Lecanemab在中国的上市申请拟纳入优先审评,在未来两年将有很大机会和中国患者见面。
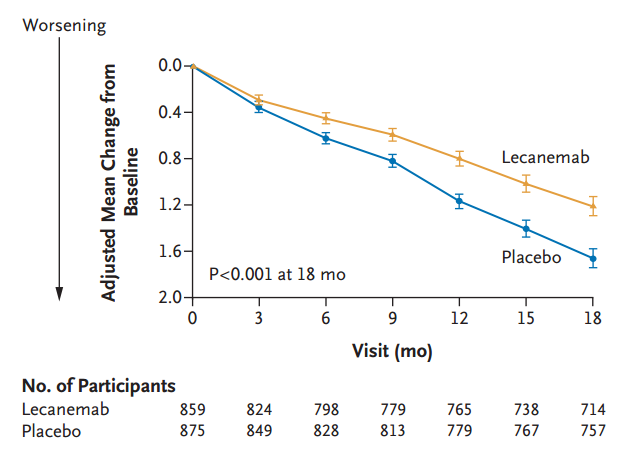
Lecanemab三期临床数据
但值得关注的是,lecanemab在临床试验中出现了第三例死亡案例,一名79岁的妇女在接受lecanemab后出现大面积脑肿胀、出血以及癫痫发作后死亡,多位神经科学家认为,她的死亡很可能由lecanemab引起的,所以后期lecanemab的真实世界研究数据值得所有人关注。
此前Biogen和卫材表示,lecanemab在美国市场的定价为2.65万美元/年,倘若进入中国市场,在美国市场前景都尚不明确的前提下,其在上市后直接进入医保的可能性存疑,再加上其安全性问题,在国内市场短期内的认可度相信也将打上折扣。
03 希望仍在
千头万绪,药物研发还是需要回归到安全性以及有效性之上,尽管发病机制不明确导致了阿尔兹海默病药物不断的失败,但不管怎样还是出现了三款有一定意义的药物,如果三款药物均可以实现完全批准,那么相信从监管方、医保支付、医生以及患者人群上均会实现多方认可,这也是更多患者人群的希望所在。
尽管前面已经经历过太多失败,但除了上述三款药物,目前仍有其他希望。除了Lecanemab,礼来Donanemab在三期临床头对头击败Aducanumab(组织学终点)。此外,Axsome的NMDA受体拮抗剂AXS-05治疗阿尔茨海默病激越症状的Ⅲ期临床成功,SIGMAR1激动剂Anavex治疗阿尔茨海默症认知功能减退的ⅡB/Ⅲ期临床同样获得成功。
根据智慧芽新药情报库,目前关于阿尔兹海默病药物的临床试验也超过5000项,无论是九期一,还是lecanemab,还是正在冲刺的其他药物,大家想看到的都不是见证失败,更不是冷嘲热讽,药物本身就应该去解决未满足的临床需求,这也是我们所期待的。
参考资料:
1.Eisai's Leqembi shunned as CMS keeps strict Alzheimer's drug restrictions in place;
2.Eisai, Biogen's high-stakes Leqembi filing nets FDA priority review—and an AdComm hearing
3.ICER dials up recommended price range for Eisai's Leqembi—but still calls for sizable discount
4.Lecanemab's Rough Progress,Science
5.Lecanemab in Early Alzheimer’s Disease,N Engl J Med 2023; 388:9-21,DOI: 10.1056/NEJMoa2212948
6.美国Biopharma成长启示录-兴业证券
7.各大企业官网以及临床试验登记平台
8.智慧芽新药情报库

 产业资讯
产业资讯
 药通社
药通社  2026-06-06
2026-06-06
 530
530

 产业资讯
产业资讯
 赛柏蓝
赛柏蓝  2026-06-06
2026-06-06
 429
429

 产业资讯
产业资讯
 摩熵医药
摩熵医药  2026-06-06
2026-06-06
 447
447
 热门资讯
热门资讯