 产业资讯
产业资讯
 Insight数据库
Insight数据库  2023-08-24
2023-08-24
 3424
3424
专利战,是企业保护创新成果和争夺市场份额的「利器」,也是跨国制药巨头的「家常便饭」。
近期就有两家 MNC 巨头打响了专利战:GSK 起诉辉瑞的呼吸道合胞病毒(RSV)疫苗 Abrysvo 侵犯了其疫苗产品 Arexvy 的专利。
如果 GSK 胜诉,辉瑞将被永久禁止在美国销售和生产 RSV 疫苗。据分析师预测,RSV 疫苗的市场规模预计到 2030 年会增长到 100 亿美元以上,接近 13 价肺炎疫苗的市场空间。
如此大的蛋糕,辉瑞肯定不会轻易放过。当然,也包括其他海外企业。
只不过,相比如火如荼的海外市场,国产企业在 RSV 疫苗的管线布局上却选择「沉默」。这究竟是为何?
RSV 疫苗研发:高风险下的大机遇
疫苗品种复杂多样,有针对 9-45 岁女性的 HPV 疫苗,也有针对婴幼儿及中老年人群的流感疫苗。
虽然这两种疫苗的接种人群不同,但都有着巨大的市场空间。根据互联网营销圈流传的消费力榜单,女人、小孩和老人均排在前列。
与流感疫苗类似,RSV 疫苗是一款针对 5 岁以下儿童及 65 岁以上老人的疫苗产品。只不过,前者主要是用来预防流行性感冒病毒引起的流行性感冒,后者则针对 RSV(呼吸道合胞病毒)感染。
RSV 是 1956 年从黑猩猩呼吸道分离出来的一种非节段性单股负链 RNA 病毒,属于副黏病毒科的肺病毒属,具有明显季节性(冬春季节为感染的高发期),常在易感人群婴幼儿和老年人中引发严重的肺炎、哮喘和支气管炎,并且可在一生中反复感染。
根据 WHO 估计,全球每年有约 3300 万-6000 万的儿童感染 RSV,以及大约 3%-7% 的 60 岁以上老年人会受到 RSV 感染。
儿童急性呼吸道感染的病因

全球 2019 年 5 岁以下儿童 RSV 相关疾病及死亡统计
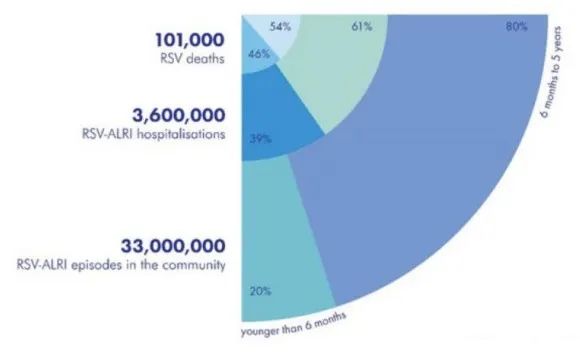
来自:Pediatr Rev,柳叶刀,申万宏源研究
市场上针对 RSV 感染的治疗,主要包括抗体药物和 RSV 疫苗两种。其中,抗体药物主要为帕利珠单抗(Synagis)和 Beyfortus。
不过,帕利珠单抗并不完美:仅限于高危婴幼儿 RSV 预防,患者覆盖面窄,由于中和能力不高,预防效果有限、持续时间较短(保护期仅一个月),而且价格高昂(单剂成本达 1000-3000 美元)。
可即便如此,过去 10 年帕利珠单抗的销售峰值仍达到 16 亿美元。这也从侧面反映出,RSV 疫苗仍存在巨大的未被满足的临床需求,市场仍有大机遇。
阿斯利康和赛诺菲共同开发的 Beyfortus(尼塞维单抗)属于长效性的单抗,专为所有婴儿设计,只需给予单剂量肌肉注射就能提供持续的预防 RSV 疾病作用(药效持续时间约为五个月),能将 RSV 引起的下呼吸道感染发生率降低 74.5%,此前已分别于 2022 年 10 月底、2023 年 7 月获得欧盟、美国 FDA 批准上市,是第一个也是唯一一个针对广泛新生儿和婴儿群体的 RSV 预防方案,极具里程碑意义。
Beyfortus 全球项目开发关键节点
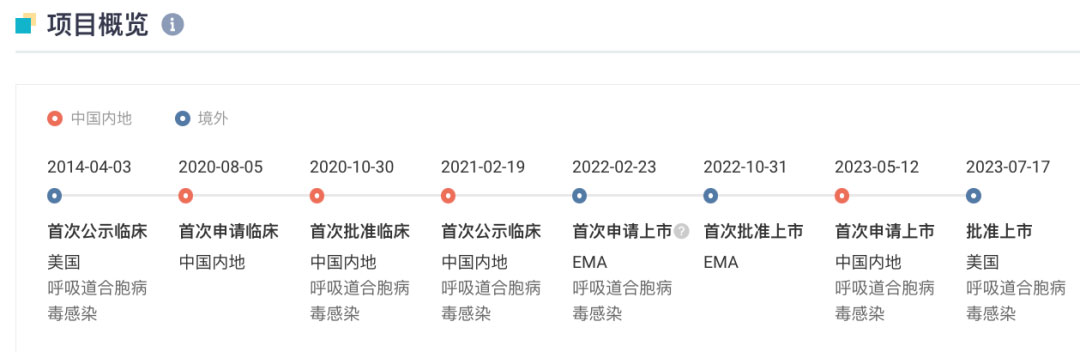
来自:Insight 数据库网页版(下文如无特殊标注,为同一来源)
就 RSV 疫苗而言,早在上世纪 60 年代就已经开始研发,只不过在过去 60 多年的探索中,曾因安全性风险或疗效不足等导致频频失败,一度成为像 AD、NASH 药物般的研发黑洞。
后来经过科学家们研究发现,早期 RSV 疫苗多以失败告终的主要原因是:选用了 Post-F(F 蛋白的融合后结构)作为抗原。
印度有句谚语,「成功是由许多失败积累而成的。」随着科学家们发现选择融合前(Pre-F)蛋白作为抗原,能增加蛋白稳定性,并激发足够强的保护效果,才让 RSV 疫苗的研发进入了快车道。
由此,上述两种治疗手段撑起了百亿美元级别的 RSV 防治市场。根据《Research and Markets》报告表明,2024-2028 年,RSV 疫苗和抗体市场将以 38.9% 的年复合增长率增长,到 2028 年市场将达到 95.3 亿美元,其中疫苗市场将占据大部分市场份额(67.5%)。
尽管 RSV 疫苗研发的风险较高,但在市场的大机遇下,仍有不少企业前赴后继,并冒出了「突围者」。
全球仅 2 款获批,Moderna 上市在即,GSK 保护效力最高
「千淘万漉虽辛苦,吹尽狂沙始到金」。经过 60 多年的探索,RSV 疫苗市场终于盼来了「突围者」。
2023 年 5 月,GSK 开发的 RSVPreF3 疫苗(Arexvy/GSK 3844766A)和辉瑞的 Abrysvo(RSVpreF/PF-06928316)相继获 FDA 批准上市,成为目前全球仅有的两款 RSV 疫苗。
紧随其后的是 mRNA 疫苗巨头 Moderna(莫德纳)研发的 mRNA-1345,此前已于 7 月 5 日递交全球上市申请,包括欧盟、瑞士、澳大利亚和 FDA,将有望摘得全球第三款 RSV 疫苗。
全球处于上市申请以及获批上市阶段的 RSV 疫苗
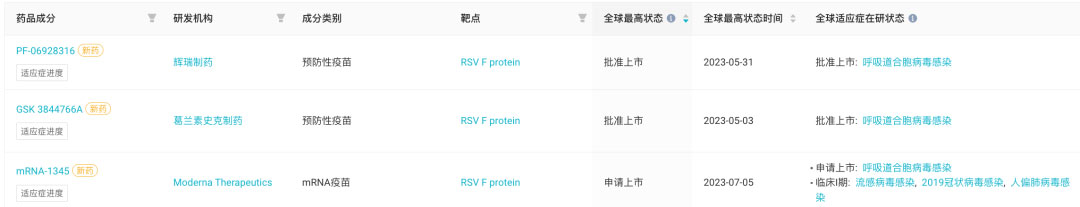
值得一提的是,这三款 RSV 疫苗在技术路线、抗原选择、佐剂、适应人群和保护效力等方面均存在显著差异。
对比来看,GSK 和辉瑞的 RSV 疫苗均采用重组蛋白亚单位技术路线,而 Moderna 采用了其擅长的 mRNA 技术,其中辉瑞使用的是双价抗原(来自 RSV A 与 RSV B 病毒亚型的 Pre-F 蛋白),另两者均选择以 DS-Cav1 为基础的 Pre-F 抗原。
此外,辉瑞和 Moderna 的 RSV 疫苗均未使用佐剂,而 GSK 使用了自主研发的 AS01e 佐剂,增加了体液免疫和细胞免疫这一优势。
一般来说,在疫苗中加入佐剂,可以大幅提高疫苗的免疫原性。GSK 正是在重组带状疱疹疫苗 Shingrix 中应用了 AS01B 佐剂,才大幅提升了预防效力。
因此,在保护效力方面,GSK 的 Arexvy 对于预防 2 种及以上 RSV 相关下呼吸道症状(RVS-LRTD2)的保护率高达 94.1%,而辉瑞和 Moderna 的保护率分别为 66.7% 和 83.7%。
三款 III 期临床成功的 RSV 疫苗对比
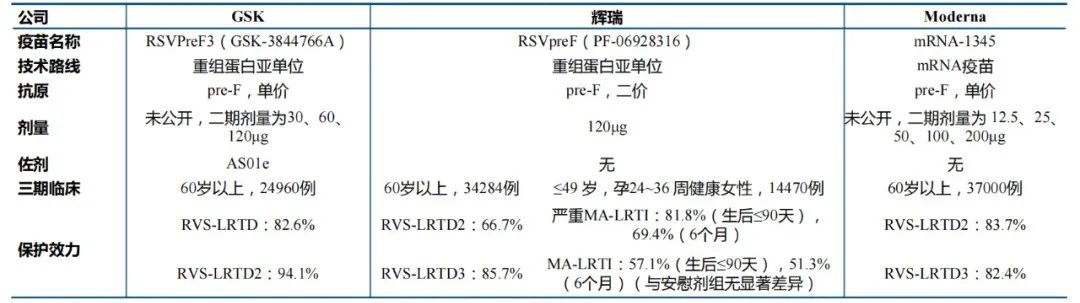
注:RSV-LRTD:RSV 相关下呼吸道症状,后面数字表示症状数量;MA-LRTI:医学护理下呼吸道疾病(数据来源:公司官网,中信建投)
在适应人群方面,这三款 RSV 疫苗获批的适应症都是针对 60 岁以上老年人,而辉瑞的 RSV 疫苗还增加了孕期女性人群,辉瑞刚于昨日宣布 FDA 批准 Abrysvo 扩展用于妊娠 32-36 周孕妇,保护新生儿免受 RSV 感染,成为首款用于孕妇群体的 RSV 疫苗。
根据辉瑞此前公布的 Ⅲ 期临床数据,孕妇接种 Abrysvo 后,婴儿在出生后 90 天和 180 天疫苗对 RSV 引起的严重下呼吸道疾病的保护效力分别为 81.8%、69.4%,6 个月随访期的效力为 69.4%。安全性方面,疫苗耐受性良好,在接种疫苗的孕妇及其新生儿中均未见安全性问题。整体严重不良事件(SAEs)比例为 4.2%。
NCT04424316 试验结果
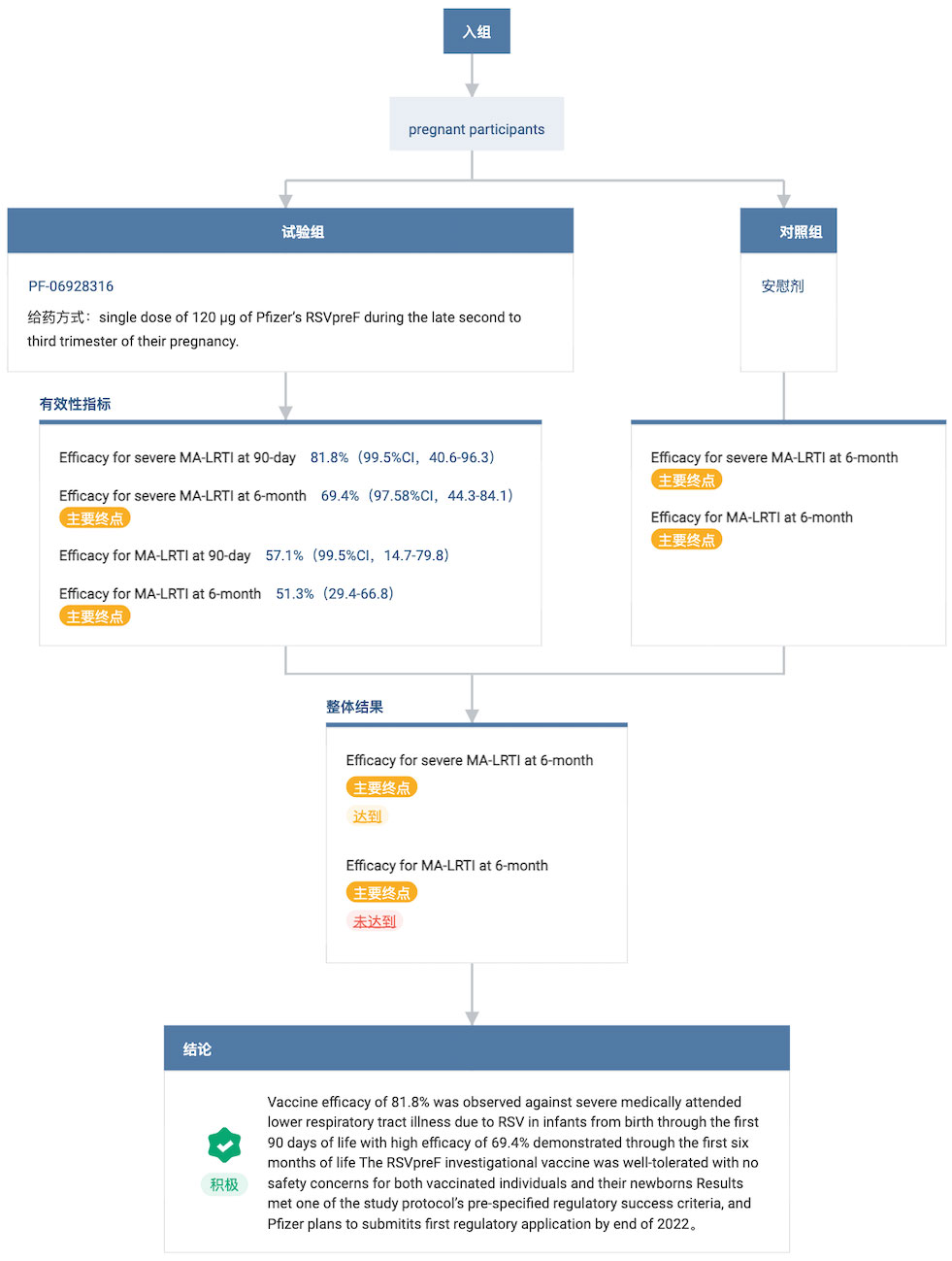
有第三方咨询机构预估,婴幼儿群体的市场空间比老年人更大,婴幼儿群体占 RSV 疫苗市场的比重达到 70%,远高于老年人。
另一边,Moderna 的 mRNA-1345 也在进行一项针对儿童人群全面入组的 Ⅰ 期试验,期待后续数据读出。全球 RSV 疫苗项目(部分)
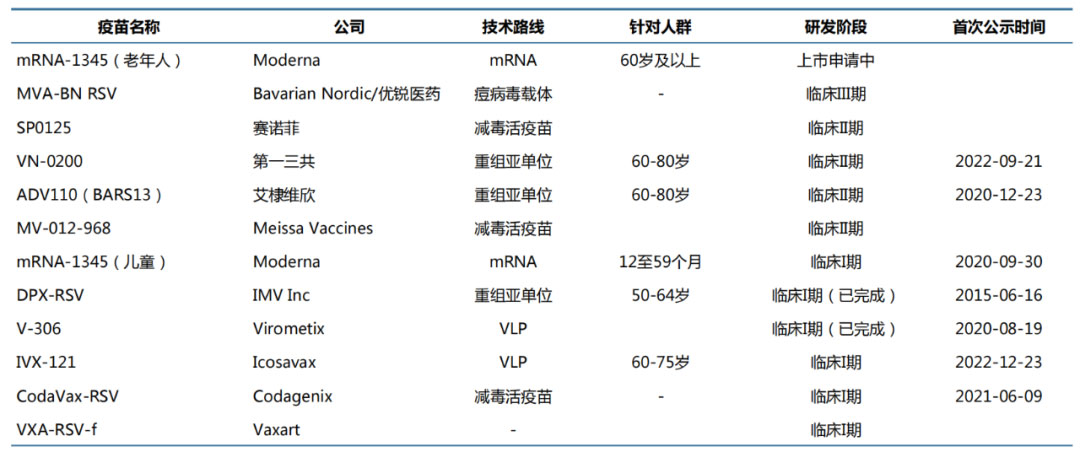
来自:Insight、中信建投
当然,除了上述三款 GSK 疫苗以外,海外企业还有不少同类产品已进入临床阶段,包括赛诺菲的 SP0125(减毒活疫苗技术路线)、Icosavax 的 IVX-121(VLP 技术路线)等,疫苗类型呈现多元化。
国内百亿市场待开拓,但也布满荆棘
现阶段,海外 RSV 疫苗研发正在如火如荼地进行当中。而国产企业却选择了「沉默」,百亿级别市场尚待开拓。
据 Frost&Sullivan 分析,我国由于 RSV 感染引起的急性下呼吸道感染的发病率约为 31‰,随着中国人口老龄化进程加快,未来 RSV 疫苗潜在需求人群持续增长,预计 2030 年潜在需求人群将达到 2968 万人,参考 GSK 给出的 Arexvy 定价范围 60-185 美元测算,2030 年 RSV 疫苗国内潜在市场空间有望达 18-55 亿美元。
事实上,我国在这条赛道上并非没有探索者,只是布满了荆棘。
2022 年,优锐医药就曾以 2.25 亿美元的总交易额向丹麦公司 Bavarian Nordic 引进 RSV 疫苗产品 MVA-BN RSV,而且在中国获批 III 期临床试验时还提振了信心。
MVA-BN RSV 医药交易

只可惜,MVA-BN RSV 的临床试验还是失败了。
7 月 22 日,Bavarian Nordic 宣布 MVA-BN RSV 在三期 VANIR 研究中未能显著降低下呼吸道疾病(LRTD)的发生率,因此决定终止该产品的开发计划,并结束与优锐医药的合作关系。根据最终研究结果显示,MVA-BN RSV 预防至少 2 种 LRTD 症状发生的效力仅有 42.9%,与安慰剂组的数据无显著性差异。
事实上,这已经不是病毒载体 RSV 疫苗第一次倒下。此前的失败者,已经有 GSK、Vaxart 和强生等。
从当前国产企业的研发情况看,进入临床阶段的在研 RSV 疫苗已相当稀少,仅有艾棣维欣自主研发的 ADV110(BARS13)在澳大利亚推进至 II 期临床,可谓是「全村的希望」。尽管沃森生物/蓝鹊生物、艾美疫苗、智飞生物、三叶草生物等,都有在年报中提及 RSV 疫苗管线的布局,但大多数仍处于临床前阶段。
研发机构总部所在地在中国的 RSV 疫苗项目
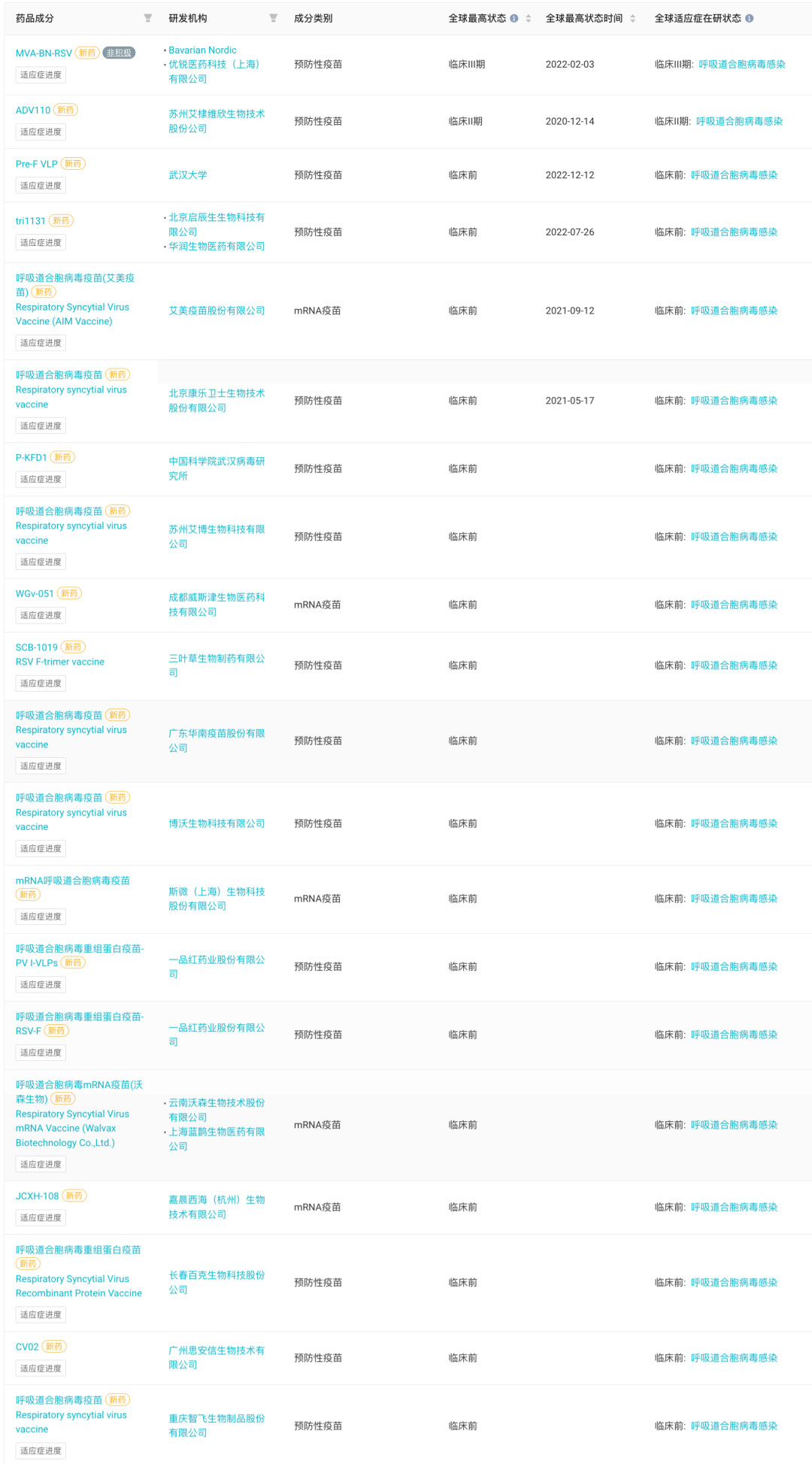
艾棣维欣的 ADV110 属于重组蛋白疫苗技术路线,由纯化的 RSV G 蛋白亚单位作为免疫原性成份与公司开发的佐剂 AE011 组成。
据艾棣维欣首席科学家王宾博士介绍,不同于其他针对 F 蛋白的 RSV 疫苗,ADV110 针对的是 RSV 的 G 蛋白,不仅可以防止病毒感染细胞,还能避免病毒通过细胞间融合感染传播的作用,而产生抗 pre-F 蛋白的疫苗无法避免细胞间的传播,因而 G 蛋白疫苗效果更好。
另外,针对开发 G 蛋白疫苗需要面临的过度激活细胞免疫免疫而产生出肺部炎症的问题和变异问题,艾棣维欣选择在 ADV110 里加入了专有的 AE-011 佐剂,以抑制过强的免疫反应,起到增强中和抗体的水平和提高安全性的作用,同时针对 G 蛋白的 G1 和 G2 两种亚型,开发 2 价疫苗。
根据 Ⅰ 期临床试验结果表明,ADV110 在低剂量、高剂量,以及单次接种和两次接种均具备良好的安全性及耐受性,并且绝大多数受试者表现出显著的抗体应答,低剂量组达到 90%、高剂量组达到了 100%。
不过,这款疫苗尚处于临床前期阶段,能否研发成功还得看后期数据读出。
这也意味着,我国在 RSV 疫苗这条道路上还有很长的路要走。
参考资料:
1.《医药行业重磅疫苗系列深度报告(二):RSV 疫苗,百亿市场待开启》,申万宏源
2.《医药行业深度研究·2023 年 1_6 月疫苗行业纵览:1_6 月批签发同比稳定增长,重磅品种持续放量》,中信建投

 产业资讯
产业资讯
 瞪羚社
瞪羚社  2026-04-01
2026-04-01
 51
51

 产业资讯
产业资讯
 米内网
米内网  2026-04-01
2026-04-01
 56
56

 产业资讯
产业资讯
 药时代
药时代  2026-04-01
2026-04-01
 56
56