 产业资讯
产业资讯
 医药魔方
医药魔方  2023-12-14
2023-12-14
 2762
2762
根据医药魔方数据库,2023年,国内共发生了超170笔license in交易,其中2/3交易的转让方是中国企业,其次是美国企业,还有一些来自日本、英国、瑞士等国家,项目类型以创新药和技术的权益引进为主。(注:数据截至发稿日期,本文统计数据包括国内企业之间的授权许可引进和跨境授权许可引进)与往年相比,2023年license in交易数量有所下降,但总金额与2022年基本持平,这主要得益于百济神州、华东医药等公司的大手笔支出。今年,百济神州先后引进了映恩生物的ADC和ensem therapeutics(昂胜医药)的CDK2抑制剂,两笔交易总额均超10亿美元。华东医药继续大力出奇迹,与科济药业、Scohia、三优生物、Arcutis等8家公司签署合作协议,涉及细胞疗法、GLP-1药物和多款医美产品。
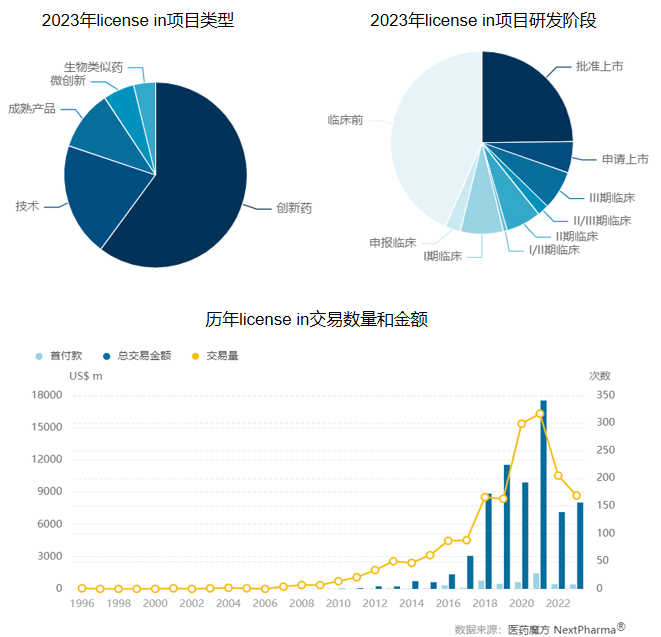
本文按总金额和首付款整理了2023年中国创新药license in交易TOP15,并将按照总金额榜单简单介绍相关交易,供参考。
2023年中国创新药license in交易TOP15 (按总金额计,单位:亿美元)
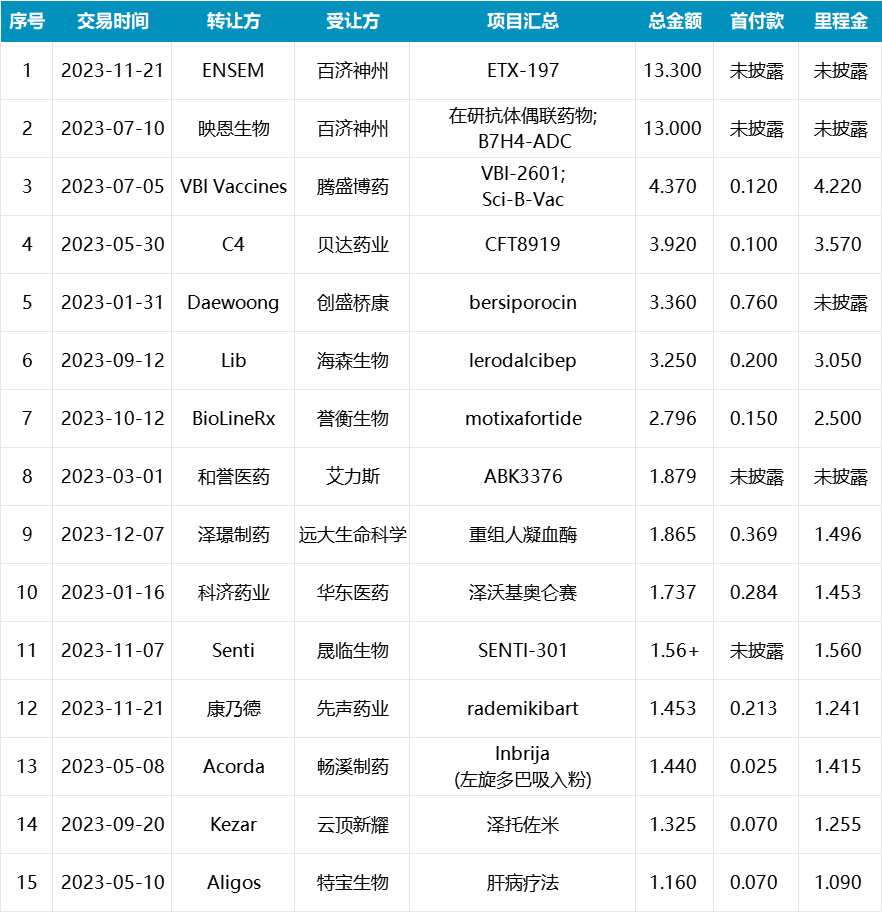
2023年中国创新药license in交易TOP15 (按首付款计,单位:亿美元)
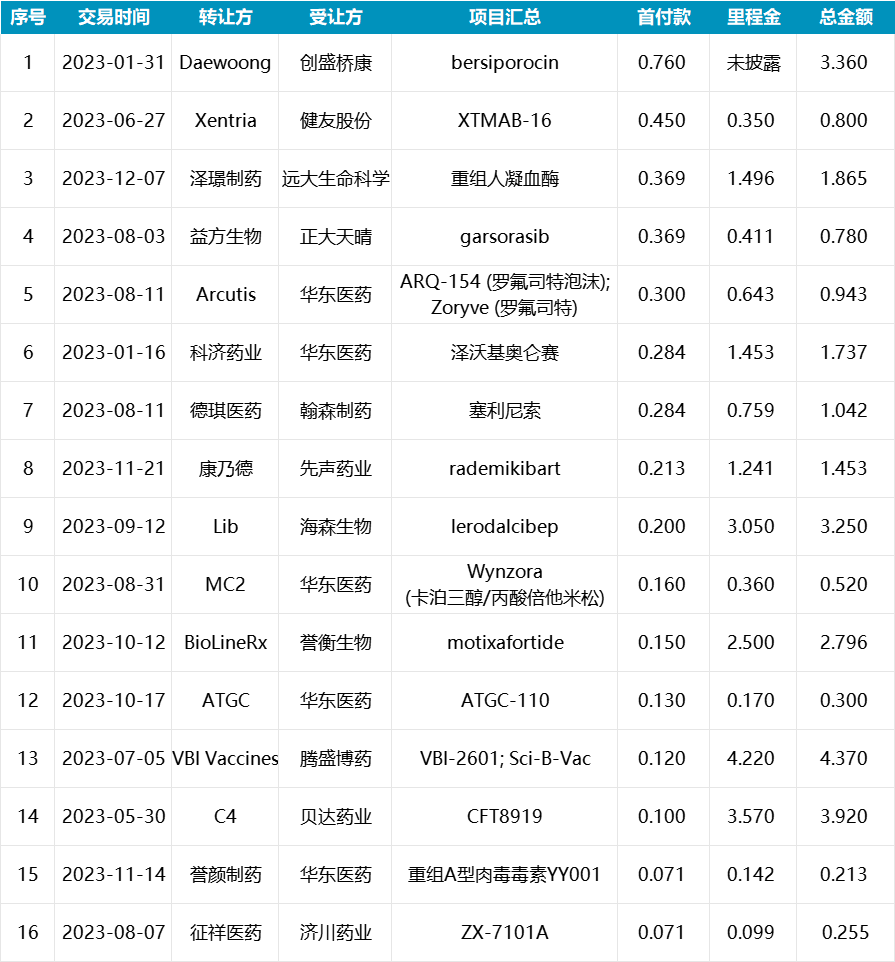
NO.1/2 百济神州断层霸榜前二
11月21日,百济神州宣布,与昂胜医药达成授权合作协议,获得一款在研、即将提交IND申请的口服CDK2抑制剂的全球独家许可权利,交易总金额高达13.3亿美元。该产品将与百济神州的CDK4抑制剂(临床I期)形成补充,有望改善目前CDK4/6抑制剂在特定乳腺癌患者中的治疗效果。
早在今年7月,百济神州还从映恩生物引进了一款在研、临床前ADC药物的全球开发和商业化权利,该药物将用于治疗特定实体瘤患者。根据协议条款,映恩生物将从百济神州获得一笔首付款,并将在百济神州行使选择权后,有权获得选择权付款。此外,映恩生物将有权获得高达13亿美元的里程碑付款,以及分级特许权使用费。
NO.3 腾盛博药扩展HBV产品组合
7月6日,腾盛博药宣布,与VBI达成协议,将持有的BRII-179(VBI-2601)独家许可扩大至全球市场,此外还获得在大中华区及包括澳大利亚、印度尼西亚、马来西亚等亚太国家开发和商业化PreHevbri(Sci-B-Vac)的独家权益。PreHevbri是一款具有临床差异化的三抗原成人HBV预防性疫苗,已在美国、欧盟/欧洲经济区、英国、加拿大和以色列获批上市。
腾盛博药将向VBI支付1500万美元的预付款,其中包括约300万美元的股权投资。此外,VBI还有资格获得高达4.22亿美元的里程碑付款,以及双位数特许权使用费。
NO.4 贝达药业引进EGFR L858R降解剂
5月30日,贝达药业宣布,与美国C4 Therapeutics达成合作,引进后者EGFR L858R降解剂CFT8919在中国(包括香港、澳门和台湾地区)的开发、制造和商业化权益,交易总额为3.92亿美元,包括1000万美元首付款、2500万美元股权投资和最多3.57亿美元里程碑付款。CFT8919是一种具有口服生物利用度的变构BiDAC™降解剂,对携带EGFR L858R突变具有良好的活性和选择性。
NO.5 创盛桥康引进同类首个PRS抑制剂
1月31日,创盛桥康(CSP)与Daewoong Pharmaceutical(大熊制药)达成独家许可协议,在大中华区(包括中国大陆、香港、台湾和澳门)开发和商业推广同类首个PRS抑制剂Bersiporocin(DWN12088 )。
根据协议,CSP被许可用于治疗特发性肺纤维化和其他潜在纤维化适应症的Bersiporocin,总对价高达3.36亿美元,包括高达7600万美元的预付款和开发里程碑付款以及两位数的净销售额分成。
Bersiporocin是大熊制药开发的全球首个口服小分子PRS抑制剂,通过减少影响胶原蛋白生成的PRS蛋白的作用,抑制导致纤维化的胶原蛋白过度生成,有望发挥抗纤维化作用。
NO.6 海森引进第三代长效PCSK9抑制剂
9月12日,海森生物宣布,和Lib Therapeutics达成许可协议,获得Lerodalcibep在大中华区开发和商业化的独家专有权。Lib将获得2000万美元的预付款,并有可能额外获得最高达3.05亿美元的临床、注册和销售里程碑付款,以及特许权使用费。
Lerodalcibep融合蛋白是由Lib开发的第三代长效PCSK9抑制剂,每月一针皮下注射,对解决当前临床降脂治疗中未被满足的需求极具潜力,有望助力更多高脂血症患者实现血脂控制达标,目前正处于III期临床开发阶段。
NO.7 誉衡生物引进CXCR4拮抗剂
10月12日,BioLineRx宣布与誉衡生物达成独家许可协议,授予后者在亚洲开发和商业化Motixafortide的权益,交易总额为2.796亿美元,包括1500万美元的预付款、14602万美元股权投资、5000万美元的潜在开发和监管里程碑付款、2亿美元的潜在商业里程碑付款,以及分级特许权使用费。
Motixafortide是一款新型、高亲和力、选择性环肽类CXCR4拮抗剂,今年9月获得美国FDA 批准上市,联合filgrastim用于多发性骨髓瘤患者自体干细胞移植中的干细胞动员。
NO.8 艾力斯引进新一代EGFR-TKI
3月1日,艾力斯医药宣布,与和誉医药签署许可协议,获得后者新一代小分子表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)ABK3376在中国研究、开发、制造、使用以及销售的独家许可。艾力斯有权在达到行权条件时选择行使海外权益,将授权区域扩大至全球范围。和誉医药将获得最高不超过1.879亿美元的首付款、开发及销售里程碑付款以及相应比例净销售额的许可提成费。
ABK3376是高选择性、可入脑的新一代EGFR口服小分子抑制剂,可高效抑制三代EGFR TKI耐药后产生的C797S突变,目前处于临床前开发阶段。该产品有望与艾力斯已上市的第三代EGFR TKI伏美替尼联用,成为精准治疗伴有EGFR-C797S耐药突变非小细胞肺癌的新一代靶向治疗药物。
NO.9 远大生命科学引进重组人凝血酶
12月7日,泽璟制药宣布与远大生命科学子公司远大辽宁就重组人凝血酶达成独家商业化合作协议,授权后者作为重组人凝血酶在大中华区的独家市场推广服务商。
根据协议约定,远大辽宁将向泽璟制药支付首付款和商业化里程碑款4亿元,其中首付款2.6亿元、首次商业销售满12个月的商业化里程碑款1.4亿元。此外,在达到协议约定的销售里程碑事件后,远大辽宁还将向泽璟制药支付最高不超过9.15亿元的销售里程碑款,同时泽璟制药将根据协议约定向远大辽宁支付市场推广服务费。
重组人凝血酶是基于泽璟制药复杂重组蛋白新药和抗体新药研发及产业化平台开发的一种高度特异性人丝氨酸蛋白酶,是目前国内唯一采用重组基因技术生产的重组人凝血酶开展III期临床试验并获得试验成功的产品。重组人凝血酶技术壁垒高,具有独特优势,全球范围内仅有Recothrom为同类产品已经在境外上市并销售多年。
NO.10 华东医药引进新一代BCMA CAR-T疗法
1月16日,华东医药宣布与科济药业就其BCMA CAR-T细胞产品泽沃基奥仑赛注射液(zevorcabtagene autoleucel,CT053),达成在中国大陆地区的商业化合作。根据协议条款,科济药业将获得2亿人民币的首付款,最高不超过10.25亿人民币的注册及销售里程碑付款。科济药业将继续负责 CT053 在中国大陆地区的开发、注册和生产。
泽沃基奥仑赛是一款用于治疗复发/难治多发性骨髓瘤的自体CAR-T细胞产品,2022年10月已在中国申报上市。NO.11晟临生物引进CAR-NK细胞疗法11月7日,晟临生物宣布与Senti Bio就实体瘤治疗产品SENTI-301A在中国的临床开发达成新的战略合作。晟临生物将在Senti Bio的技术支持下,主导SENTI-301A产品的临床开发、运营和生产。在达到预期结果的前提下,Senti Bio将有资格获得高达1.56亿美元的里程碑付款和分级特许权使用费,其它条款未披露。SENTI-301A是一种现货型健康供体来源的CAR-NK细胞疗法,专为治疗表达GPC3的肿瘤而设计。此外SENTI-301A还融入了校定释放的白介素-15(crIL-15),这是一种多功能免疫刺激有效载荷,旨在同时刺激周围的免疫细胞,促进CAR-NK细胞的扩增、持久性和肿瘤杀伤力。临床前数据显示,SENTI-301A在体外和体内均能有效杀伤相关肿瘤细胞。NO.12 先声药业引进IL-4Rα单抗11月21日,先声药业宣布,已与康乃德生物医药达成协议,获得后者IL-4Rα单抗Rademikibart在大中华地区开发、生产和商业化的独家权益。康乃德生物医药有权获得1.5亿元的预付款、最高8.75亿元里程碑付款,以及高达净销售额两位数百分比的特许权使用费。
Rademikibart(CBP-201)是靶向IL-4Rα(IL-4Rα是IL-4受体和IL-13受体的共同亚基)的全人源单抗,与IL-4Rα结合可以有效阻断IL-4和IL-13功能,进而阻断Th2型炎症通路,从而达到有效治疗特应性皮炎及哮喘等Th2相关炎症性疾病的目的。
NO.13 畅溪制药引进全球首款帕金森病吸入治疗药物
5月8日,畅溪制药宣布与Acorda Therapeutics就Inbrija(左旋多巴吸入粉雾剂)在大中华地区(中国大陆及港澳台地区)的临床应用达成一项合作。根据协议条款,畅溪制药负责推进Inbrija在大中华地区的临床应用,并向Acorda支付250万美元的首期付款,以及后续多至1.41亿美金的潜在里程碑付款。
Inbrija已在美国和欧盟获批上市,用于正在接受左旋多巴-多巴脱羧酶抑制剂治疗的成年帕金森病患者其在“关”期(OFF episodes)的间歇性治疗。
NO.14 云顶新耀引进创新免疫蛋白酶体抑制剂
9月20日,云顶新耀宣布,与Kezar Life Sciences签订合作与授权协议,以在大中华区、韩国和部分东南亚国家进行临床开发和商业化Kezar的首款临床阶段候选药物Zetomipzomib(泽托佐米) ,交易总额为1.325亿美元,包括700万美元预付款和最高1.255 亿美元的临床和商业里程碑付款。
Zetomipzomib是一款同类首创、选择性免疫蛋白酶体抑制剂,用于治疗包括狼疮性肾炎(LN)在内的一系列自身免疫性疾病。
NO.15 特宝生物与Aligos合作开发肝病创新疗法
5月10日,特宝生物宣布与Aligos Therapeutics签署一项利用核酸技术治疗肝炎的研究合作与开发协议,从Aligos获得在中国区域(包括中国大陆、香港特别行政区、澳门特别行政区和台湾地区)对该核酸技术进行开发和商业化的独家选择权。特宝生物与Aligos将对基于治疗肝炎的核酸技术产生的寡核苷酸化合物进行合作研发。
特宝生物将向Aligos支付预付款和研究合作资金700万美元,并分阶段支付基于许可技术的产品开发、上市销售里程碑费用,最高不超过1.09亿美元,以及按净销售额的一定比例计算的特许权使用费。

 产业资讯
产业资讯
 医药财经
医药财经  2025-10-14
2025-10-14
 638
638

 产业资讯
产业资讯
 医药魔方Invest
医药魔方Invest  2025-10-14
2025-10-14
 647
647

 产业资讯
产业资讯
 同写意
同写意  2025-10-14
2025-10-14
 616
616