 产业资讯
产业资讯
 药明康德
药明康德  2024-02-20
2024-02-20
 1710
1710
随着诺和诺德(Novo Nordisk)的司美格鲁肽(semaglutide)与礼来(Eli Lilly and Company)的tirzepatide在2型糖尿病与肥胖症治疗上展现亮眼效果后,许多医疗人员与患者对这类胰高血糖素样肽1(GLP-1)受体激动剂是否同能被应用于其他肥胖相关适应症,以及药物相关副作用是否能获得进一步改善便充满期待。随着业界不断在此领域的持续投入,下一代GLP-1类药物的开发也揭开序幕。近日行业媒体Endpoints News便列出五款备受期待的下一代GLP-1疗法,药明康德内容团队将结合公开资料,向读者介绍这些疗法的“独到之处”。

▲5款潜在重磅下一代GLP-1疗法(图片来源:药明康德内容团队根据参考资料[1]重新整理制表)
在研疗法:danuglipron
开发公司:辉瑞(Pfizer)
辉瑞公司开发的danuglipron是一款小分子GLP-1受体激动剂,与大分子GLP-1类似物不同的是,它们可通过更为简便的口服方式使用,并且不受食物或者服用时间的限制。
去年5月,辉瑞公布danuglipron的2b期临床试验结果。数据显示,在2型糖尿病患者中,danuglipron显著降低患者的糖化血红蛋白(HbA1c)、空腹血糖水平和体重。接受最高剂量danuglipron治疗患者的HbA1c降低1.16个百分点,体重减少4.17公斤。这一结果发表在JAMA Network Open上。目前,不同配方、每日一次的danuglipron正在1期临床试验中受检视,预计在今年5月完成试验。辉瑞首席科学官Mikael Dolsten博士近日指出,若danuglipron在1期试验中的安全性结果表现良好,则可能经一个导入期后直接进入临床3期试验。
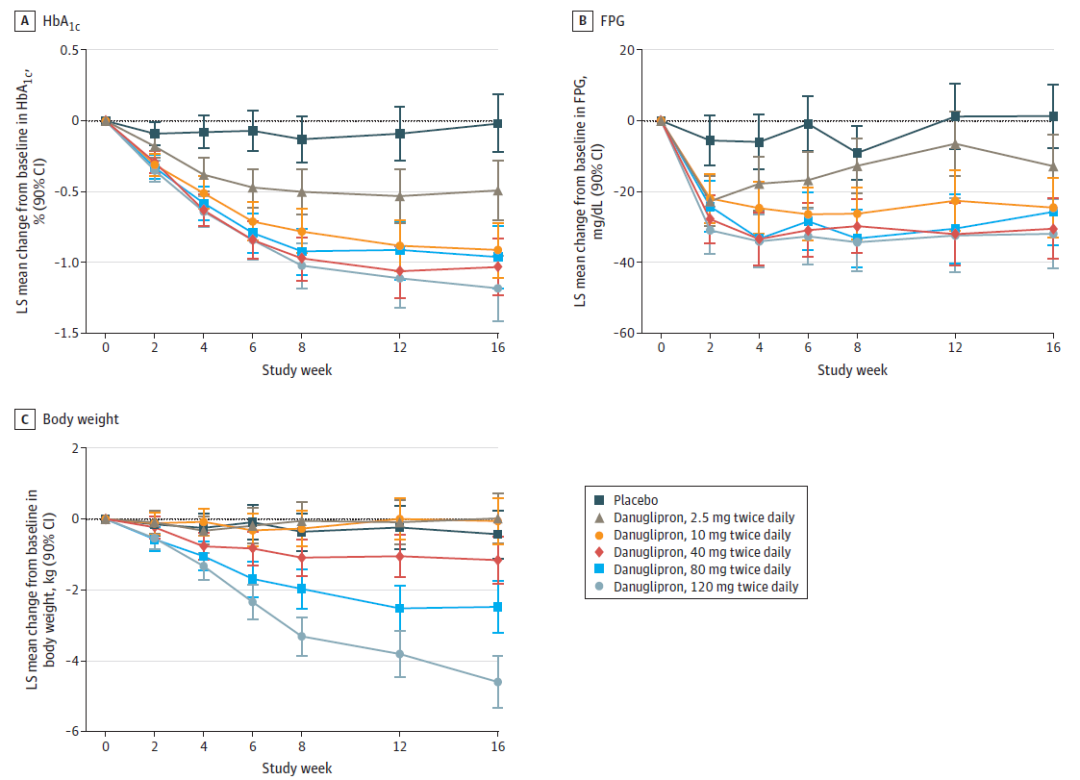
▲Danuglipron的2b期临床试验疗效结果(图片来源:参考资料[3])
在研疗法:AZD5004
开发公司:阿斯利康(AstraZeneca)
阿斯利康在去年11月与诚益生物(Eccogene)达成独家协议,以潜在18.25亿美元的总额获得小分子GLP-1受体激动剂ECC5004(即AZD5004),用于包括肥胖症、2型糖尿病和其他合并症潜在治疗的权益。
AZD5004是一款每日一次、低剂量的小分子GLP-1受体激动剂,该药物在临床前研究中证明具有理想的疗效和安全性。AZD5004目前正在美国进行针对健康受试者和2型糖尿病患者的1期临床试验,初步结果显示,与安慰剂相较,该药物在低剂量10 mg与30 mg展现积极的减重与血糖降低效果,并具有>70%的口服生物利用度以及良好的耐受性。阿斯利康打算在今年晚些时候展开两项AZD5004用于治疗过重与2型糖尿病的2期临床试验。
阿斯利康的生物药物研发执行副总裁Sharon Barr博士指出,阿斯利康的慢性肾病(CKD)和心力衰竭药物Farxiga及其在研口服PCSK9抑制剂可能与该GLP-1受体激动剂作为潜在的治疗组合。
在研疗法:retatrutide
开发公司:礼来
Retatrutide(LY3437943)是礼来的在研靶向葡萄糖依赖性促胰岛素多肽、GLP-1和胰高血糖素受体的三重激动剂,开发用以治疗2型糖尿病与肥胖患者。在去年6月所公布的2期试验临床结果显示,有83%使用12 mg剂量的肥胖或超重成人患者在经过24周的治疗后,达成至少15%的体重下降。根据行业媒体STAT的报道,这是迄今为止达成最高减重幅度的药品。安全性方面,接受retatrutide治疗患者中最常见的不良事件为胃肠道不良事件;这些事件与剂量相关,严重程度大多为轻度至中度,采用较低的起始剂量(2 mg vs 4 mg)可部分缓解所引起的不良事件。
此外,礼来也针对患有膝骨关节炎的肥胖患者以及患有或不患有糖尿病的肥胖患者的3期试验中测试retatrutide,预计2025年会有数据公布。该在研疗法也在一项2期试验中受检视,以观察它是否可以改善患有CKD的超重和肥胖患者的肾功能。
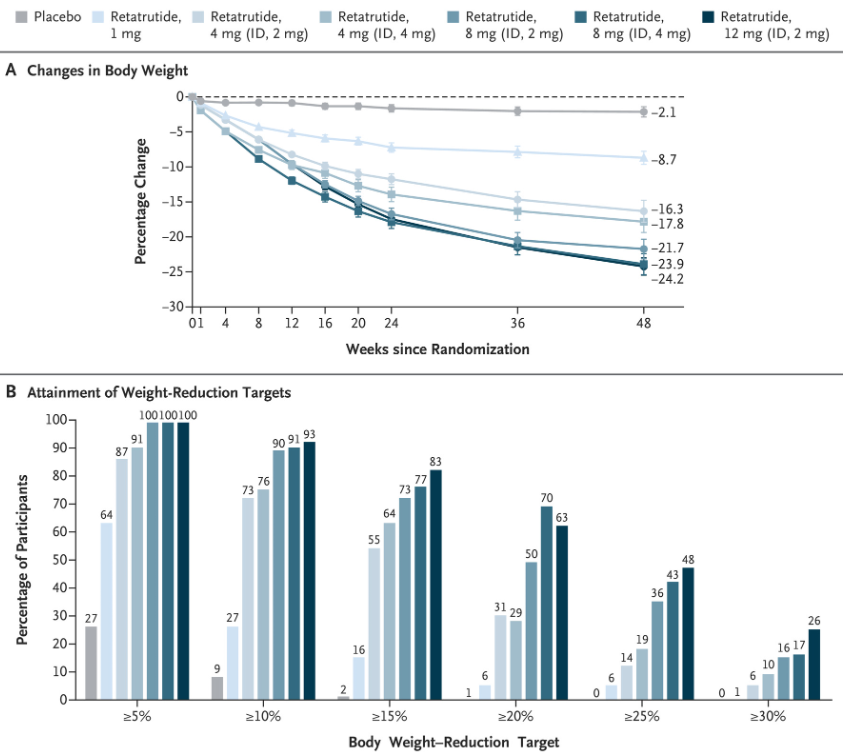
▲Retatrutide试验疗效结果(图片来源:参考资料[4])
在研疗法:survodutide
开发公司:勃林格殷格翰(Boehringer Ingelheim)和Zealand Pharma
Survodutide(曾用名:BI 456906)是一种胰高血糖素/GLP-1受体双重激动剂,可同时激活GLP-1和胰高血糖素受体,这对于控制代谢功能至关重要。在去年6月所公布的一项2期试验结果显示,不患有2型糖尿病的超重或肥胖患者接受每周一次survodutide皮下注射达46周后,有40%使用高达2剂survodutide(最高剂量)的患者,其体重减轻约19%,而此数值在安慰剂组为0%。
Survodutide目前于多项临床试验中受检视,其中备受瞩目的一项2期试验检视了该药物用以治疗非酒精性脂肪性肝炎(NASH)与肝纤维化患者的效果,该试验结果预计在今年上半年公布。此外,两项检视survodutide减重效果的3期试验也已启动,两项试验分别针对患有或不患有2型糖尿病的肥胖/过重患者。
勃林格殷格翰人类医药业务负责人Carinne Brouillon博士在接受Endpoints News专访时指出,她认为survodutide的独特之处在于它有潜力成为“首款降低食欲、同时增加能量消耗并对肝脏产生直接影响的抗肥胖药物”。
图片来源:123RF
在研疗法:MariTide
开发公司:安进(Amgen)
MariTide(AMG133)是一款潜在“first-in-class”的在研抗体多肽偶联药物(antibody-peptide conjugate),在靶向胃抑制肽受体(GIPR)的单克隆抗体的特定位点上偶联了两个GLP-1类似物,在激活GLP-1受体的同时抑制GIPR。激活GLP-1受体可延缓胃排空和抑制食欲,进而达到减重的效果。另一方面,许多遗传流行病学研究显示,不同种族背景人的体重指数(BMI)下降皆与GIPR表达量低有关。
这个月初,安进于《自然》子刊Nature Metabolism上发表了MariTide的临床前研究和1期临床试验结果。临床试验结果显示,肥胖患者只需每月一针,接受高剂量MariTide治疗85天后,体重可降低14.5%(约26斤)。值得一提的是,这些患者在停药后150天,仍可维持体重降低11.2%。安进公司正在开展2期临床试验,探索在使用高剂量的MariTide降低患者体重后,用更低剂量的MariTide或更低频率的用药次数来维持体重下降。
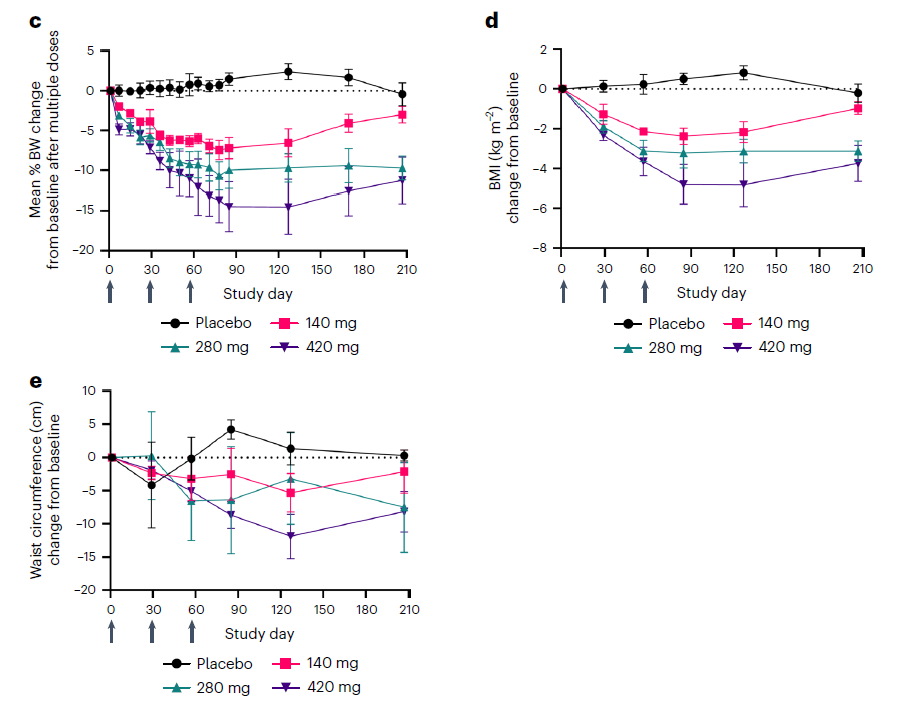
▲在多剂量递增队列中,患者的体重,BMI和腰围均出现剂量依赖性下降(图片来源:参考资料[2])
参考资料:
[1] 'Obesity plus': What’s next for GLP-1s? Retrieved February 16, 2024 from https://endpts.com/obesity-plus-whats-next-for-glp-1s/
[2] JP Morgan Healthcare Conference AstraZeneca. Retrieved February 16, 2024 from https://www.astrazeneca.com/content/dam/az/Investor_Relations/events/AZ-JPM-2024-presentation.pdf
[3] Saxena et al., (2023). Efficacy and Safety of Oral Small Molecule Glucagon-Like Peptide 1 Receptor Agonist Danuglipron for Glycemic Control Among Patients With Type 2 Diabetes A Randomized Clinical Trial. JAMA Network Open, doi:10.1001/jamanetworkopen.2023.14493
[4] Jastreboff AM. et al. “Triple–Hormone-Receptor Agonist Retatrutide for Obesity — A Phase 2 Trial” (2023) N Engl J Med. DOI: 10.1056/NEJMoa2301972

 产业资讯
产业资讯
 Medaverse
Medaverse  2025-12-22
2025-12-22
 54
54

 产业资讯
产业资讯
 医药笔记
医药笔记  2025-12-22
2025-12-22
 56
56

 产业资讯
产业资讯
 CGT分享家
CGT分享家  2025-12-22
2025-12-22
 55
55