 产业资讯
产业资讯
 医药观澜
医药观澜  2024-09-05
2024-09-05
 1327
1327
今日(9月4日),中国国家药监局药品审评中心(CDE)官网刚刚公示,默沙东(MSD)的抗PD-1单抗帕博利珠单抗又一项新适应症提交上市申请并获得受理。在此之前,帕博利珠单抗在中国获批的适应证已经达到14个。
同样在今日,另一则消息传来,默沙东宣布欧盟委员会(EC)已批准帕博利珠单抗与安斯泰来(Astellas)和辉瑞(Pfizer)开发的Nectin-4靶向抗体偶联药物(ADC)Padcev联用,作为一线治疗不可切除或转移性尿路上皮癌成人患者的治疗方案。在中国,这项联合疗法的上市申请已经于2024年3月获CDE受理。
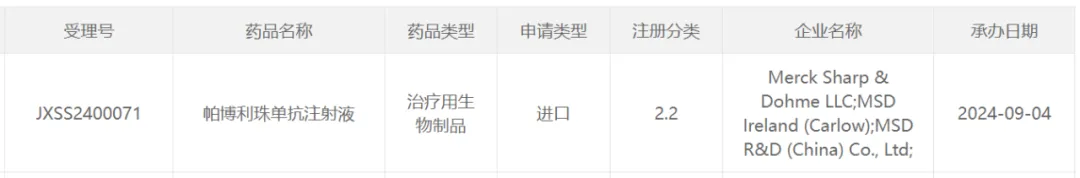
截图来源:CDE官网
帕博利珠单抗是一种人源化的抗PD-1单克隆抗体,可以阻断PD-1与其配体PD-L1、PD-L2的结合,进而激活T淋巴细胞,增强体内免疫系统抵抗癌细胞能力。在全球范围内,帕博利珠单抗自在2014年首次获得美国FDA批准治疗晚期黑色素瘤以来,目前已经获得FDA批准治疗至少16种癌症类型,以及不限癌种的适应症,获批总适应症数量达到40个。今年以来,该产品陆续获批宫颈癌、子宫内膜癌适应症。
在中国,默沙东于今年6月25日宣布帕博利珠单抗在中国获批第14个适应症,用于肿瘤表达PD-L1(CPS≥1)的局部晚期不可切除或转移性HER2阳性胃或胃食管结合部腺癌患者的一线治疗。此前该产品获批的适应症涵盖黑色素瘤、非小细胞肺癌、头颈部鳞状细胞癌、结直肠癌、食管癌、肝癌、胆道癌等。根据CDE官网查询,目前帕博利珠单抗至少还有4项新适应症上市申请正在审评中。
根据中国药物临床试验登记与信息公示平台官网,除了已获批的适应症,还有多项帕博利珠单抗的3期临床研究正在中国开展,适应症涵盖晚期肾透明细胞癌、肝外胆管癌、肝内胆管癌、前列腺癌、肌层浸润性膀胱癌、非肌层浸润性膀胱癌、卵巢上皮癌等。
希望这些临床研究进展顺利,能够早日为更多的患者带来新的治疗选择。
参考资料:
[1]中国国家药监局药品审评中心官网 . Retrieved Sep 4, 2024. From https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d
[2]中国国家药品监督管理局受理默沙东帕博利珠单抗联合enfortumab vedotin一线治疗晚期膀胱癌的新适应证申请 . Retrieved Mar 29, 2024. From https://mp.weixin.qq.com/s/q95e9K0Jq7i7AtDVKIw1vw

 产业资讯
产业资讯
 深蓝观
深蓝观  2026-03-31
2026-03-31
 6
6

 产业资讯
产业资讯
 贝壳社
贝壳社  2026-03-31
2026-03-31
 6
6

 产业资讯
产业资讯
 同写意
同写意  2026-03-31
2026-03-31
 6
6