 产业资讯
产业资讯
 佰傲谷BioValley
佰傲谷BioValley  2024-09-05
2024-09-05
 898
898
近日,根据Biospace报道,Astellas(安斯泰来)公司旗下的Astellas Gene Therapies将关闭其位于旧金山的一家基因治疗工厂,并将基因治疗生产转移至北卡罗来州的另一家工厂。受此影响,将裁员至少17人,影响数十人。根据安斯泰来发言人在一封邮件中所诉,该举动将会影响100名员工。
工厂关闭原因
Astellas Gene Therapies的发言人表示,该工厂正在关闭中,预计将于2025年3月完成。在一份声明中写道,安斯泰来一直在优先考虑资源,并做出简化运营。
在评估了其腺病毒的需求后,该公司决定关闭该设施,并将所有计划和项目转移至Astellas Gene Therapies位于北卡罗来州的另一家工厂。
尽管位于旧金山的工厂关闭、计划转移,但是Astellas Gene Therapies在加利福尼亚州的业务仍然存在。
今年5月,安斯泰来宣布在旧金山开设西海岸创新中心,占地约15万平方英尺,是安斯泰来基因治疗研究和开发业务的中心,包括Astellas Gene Therapies。
为何腺病毒需求下降?
在评估了其腺病毒的需求后,安斯泰来决定关闭一家大型生物制造工厂,说明安斯泰来对于腺病毒的需求下降。
在了解了安斯泰来在AAV基因治疗的失败史后,就明白安斯泰来确实是对腺病毒的需求不高了。安斯泰来开始探足基因治疗可以追溯到2014年与哈佛大学的合作,到正式重点部署AAV基因治疗,是在2019年以30亿美元收购了Audentes公司。
然后,安斯泰来的噩梦就来了。先是X-连锁肌小管性肌病(XLMTM)AAV基因疗法AT132,由于接连的临床死亡事件(在2020年5月、2020年6月、2020年8月、2021年9月累计报告了四例患者死亡严重不良事件),期间遭到FDA两度喊停。
目前,小编还未查到AT132解除临床搁置的消息。2022年4月,安斯泰来终止了来自Audentes的3条杜氏肌营养不良症(DMD)AAV临床前管线,AT702、AT751和AT753。2022年6月,安斯泰来又一款AAV基因疗法AT845临床试验被FDA叫停,原因是一名接受AT845治疗的晚发型庞贝病患者报告了周围感觉神经病不良事件。
该临床搁置于2023年1月解除。
AAV基因治疗的连续失败,以及多款管线的删减,安斯泰来对30亿美元收购Audentes已经进行了资产减值评估。目前,在安斯泰来官网的管线图上,来自Audentes公司的AAV临床管线仅有3条,分别是妾身未明的AT132(临床2期)、身具前科的AT845(临床1/2期)、以及一款新提的弗里德赖希共济失调相关心肌疾病项目ASP2016(临床1期)。其它基因治疗项目还未推进临床。
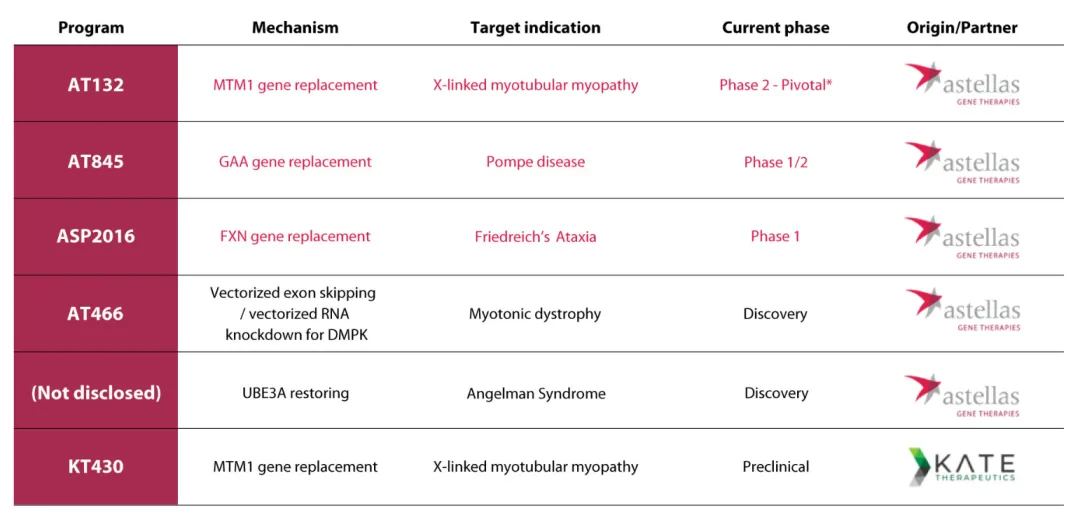
安斯泰来的基因治疗项目(图片来源:参考资料2)
如果除去AT132,也就仅有两款AAV产品需要生产临床制剂,因为都处于早期临床,产量要求也不高,因此,对于腺病毒载体的需求就下降了。
小结
除了AAV基因治疗,细胞治疗也是安斯泰来看好的方向。为了加强自身在细胞治疗领域的地位,安斯泰来于2018年收购了Universal Cells,但是在2023年终止与Adaptimmune公司的合作中,似乎暴露出Universal Cells的干细胞技术平台可能存在问题。
感觉安斯泰来在细胞治疗上,也岌岌可危......
(本文仅代表作者观点,不代表平台立场)
参考资料:
1.https://www.biospace.com/job-trends/astellas-gene-therapies-to-close-biomanufacturing-facility-affecting-about-100-employees
2.https://www.astellas.com/en/innovation/pipeline

 产业资讯
产业资讯
 深蓝观
深蓝观  2026-03-31
2026-03-31
 6
6

 产业资讯
产业资讯
 贝壳社
贝壳社  2026-03-31
2026-03-31
 6
6

 产业资讯
产业资讯
 同写意
同写意  2026-03-31
2026-03-31
 6
6