 产业资讯
产业资讯
 药融圈
药融圈  2024-09-05
2024-09-05
 2748
2748
药融云数据,www.pharnexcloud.com显示,Tarsus Pharmaceuticals是一家商业化阶段的生物制药公司,专注于未满足的需求,从眼部护理开始,应用成熟的科学和新技术,为患者带来革命性疗法。
常见眼科疾病迎来首款疗法
2023年7月,Tarsus Pharmaceuticals开发的XDEMVY(lotilaner滴眼液0.25%,中文名洛替拉纳)获得美国FDA批准用于治疗蠕形螨睑缘炎。据悉,该药物是美国FDA批准的首个也是目前唯一一个直接针对蠕形螨的治疗方法,蠕形螨是蠕形螨睑缘炎的根本原因。

睑缘炎是一种常见的慢性眼部睑缘疾病,可导致或加重眼表疾病,典型体征和症状包括睫毛碎屑、眼睛和眼睑发红、睫毛缺失或方向异常、视力模糊、刺激、眼睑发痒和眼部不适,其治疗具有挑战性,经常复发。睑缘炎可由多种因素引起,包括蠕形螨感染、细菌感染、睑板腺堵塞和脂溢性皮炎。其中,蠕形螨感染是睑缘炎的主要原因,据估计,美国蠕形螨睑缘炎患者数量可能高达约2500万。Tarsus公司认为,虽然该病诊断不足且治疗手段有限,但美国每年新诊断人数约为150万人。蠕形螨睑缘炎是一种进行性疾病,如果不及时治疗,通常表现为更严重的体征和症状,如视力模糊、睫毛缺失、角膜损伤,在极端情况下可能出现失明。
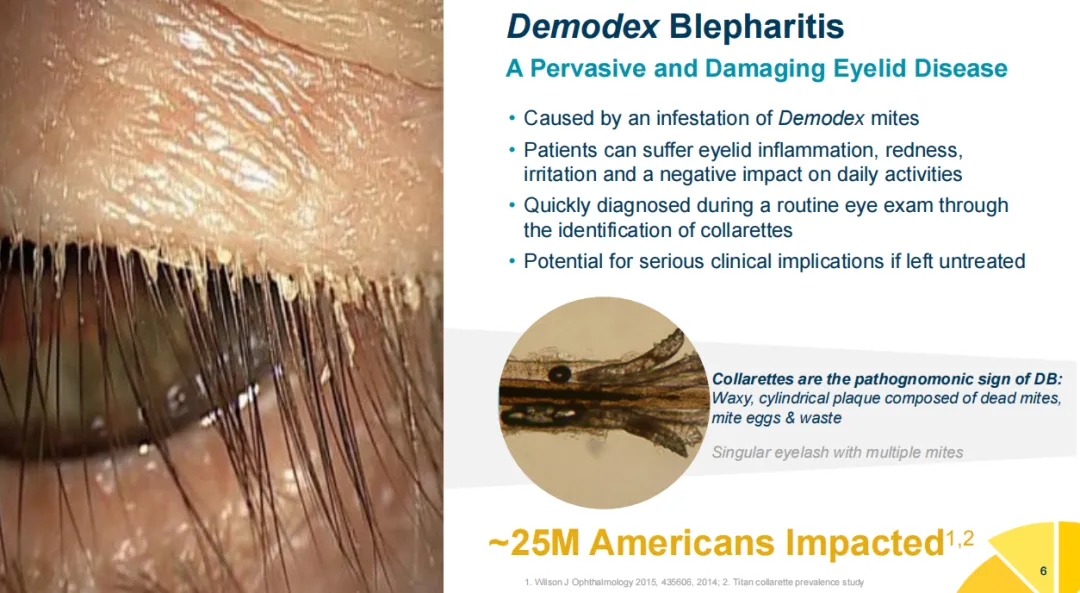
在此之前,蠕形螨睑缘炎通常通过各种非处方药治疗,如茶树油、眼睑湿巾和人工泪液,以及干眼症处方产品的超适应症用药。
XDEMVY(lotilaner滴眼液0.25%)前称为TP-03,属于一种新型抗寄生虫分子异噁唑啉类,其活性成分lotilaner是一种对γ-氨基丁酸门控氯离子通道(GABA-Cl)具有选择性的非竞争性拮抗剂,通过选择性抑制蠕形螨或其他寄生虫体内的GABA-Cl,使虫体麻痹和死亡,从而治愈蠕形螨睑缘炎。
该药物已被证明无法与人类GABA-Cl和其他离子通道(如hERG)结合,因此对人类的神经系统没有影响。另外,lotilaner是一种高度亲脂性分子,这能够促进其在毛囊的油性皮脂中的吸收,这是螨虫栖息的地方。
Lotilaner(TP-03)已在美国完成了两项关键临床研究,均达到了研究的主要终点和次要终点,且耐受性良好。Saturn-2研究招募了412名成人患者,研究显示XDEMVY(lotilaner滴眼液)治疗组有56%的患者实现改善(每个上眼睑袖套状分泌物少于2处)。Saturn-1研究招募了421名成人患者,研究显示XDEMVY(lotilaner滴眼液)治疗组有44%的患者实现改善。
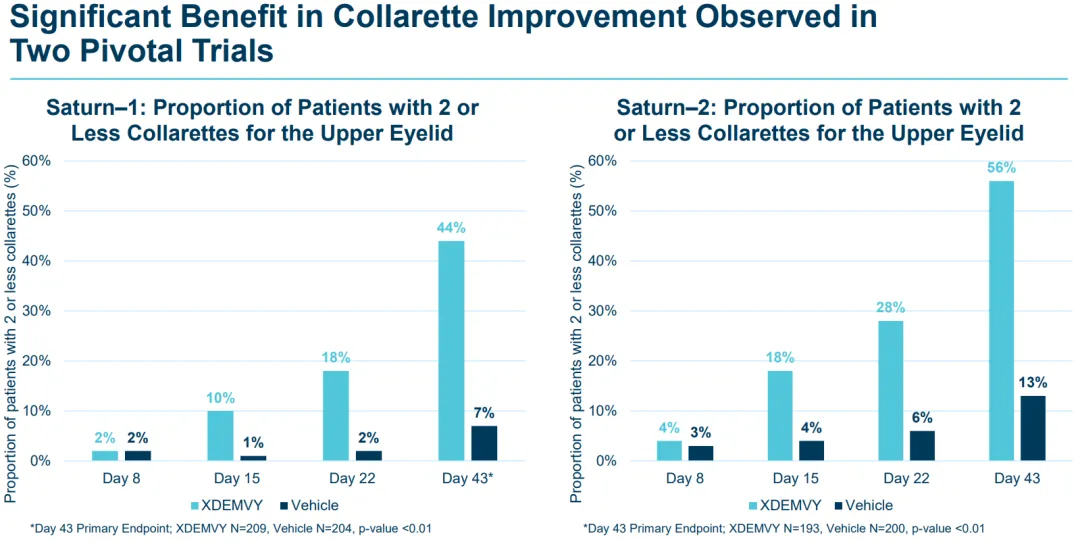
在蠕形螨睑缘炎之外,Tarsus还在开发TP-03用于治疗睑板腺功能障碍(MGD)。MGD是一种睑板腺慢性异常的疾病,睑板腺是眼睑内部的腺体,能够分泌脂质和其他分子,对维持眼睛表面的健康泪膜至关重要。MGD的主要特点是睑板腺体堵塞或破坏,可导致泪膜缺乏,是干眼症的主要原因之一。在美国约有3000~4000万人受到MGD的影响,目前尚无FDA批准的药物治疗MGD。MGD的临床体征已被证明与短蠕形螨感染相关,而TP-03旨在通过根除短蠕形螨和减少由蠕形螨引起的眼睑炎症,来缓解可能导致MGD的一些关键因素。
2023年12月,Tarsus报告了2a期临床试验Ersa的阳性终点结果,该试验评估了TP-03(0.25%),每天2次或每天3次,连续12周,用于治疗伴有蠕形螨感染的MGD患者的疗效,研究表明,与基线相比,TP-03治疗12周后在疾病的两个客观指标中实现了统计学意义和临床意义的改善,即通过睑板腺分泌评分(MGSS)测量液体分泌的存在和质量,以及分泌正常(透明)液体的腺体数量,且耐受性良好。Tarsus计划在2024年底前与FDA讨论并确定潜在的监管路径。
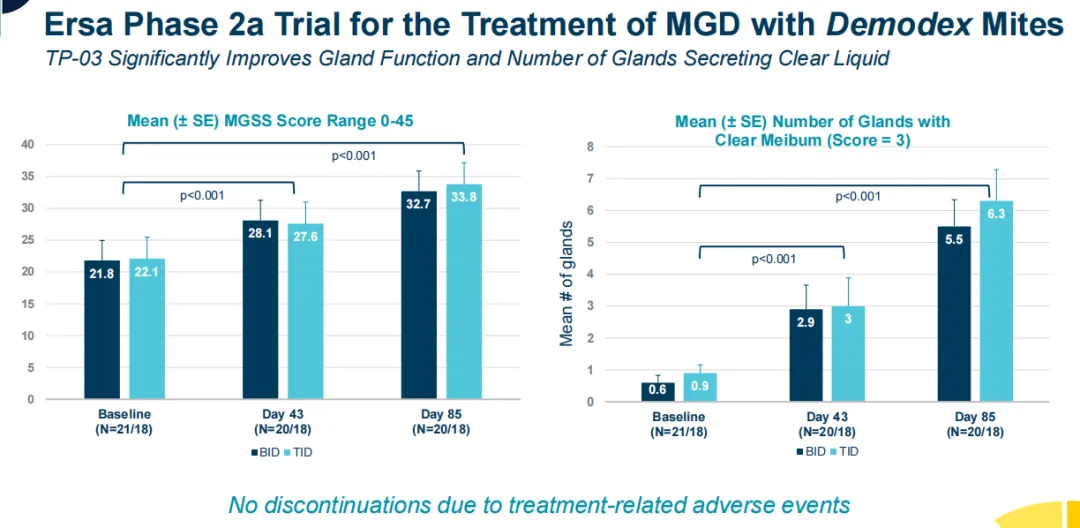
远大医药获得大中华区权益
药融圈早前报道,2021年3月,Tarsus Pharmaceuticals与联拓生物宣布达成战略合作,授予后者在大中华区(中国大陆、中国香港、中国澳门、中国台湾)开发和商业化TP-03的独家权利。据估计,国内约有4000万蠕形螨睑缘炎患者和7000万睑板腺功能障碍(MGD)患者。根据协议条款,Tarsus获得1500万美元的预付款以及高达1.85亿美元的潜在开发和商业化里程碑付款。Tarsus当时还获得了联拓生物的少数股权(已在2024年6月出售)。
2023年10月,联拓生物公布了评估TP-03治疗中国蠕形螨睑缘炎患者的III期临床研究LIBRA的顶线数据结果。该研究的共同主要终点为第43天的螨虫根除率(定义为螨虫密度为0只螨虫/睫毛)以及袖套状分泌物治愈率(0级:定义为每个眼睑0-2根睫毛有袖套状分泌物)。结果显示,与溶媒组相比,TP-03治疗蠕形螨睑缘炎患者的螨虫根除率具有统计学显著性(p<0.001)。袖套状分泌物治愈率也呈现出阳性但无统计学意义的趋势(p=0.15)。TP-03耐受性良好,其安全性特征与其它大规模临床试验中观察到的结果相似,无治疗相关的停药情况。
不过随着联拓生物在今年2月宣布开始关闭业务,TP-03在大中华区的权益再次易主。
2024年3月,远大医药宣布与联拓生物和Tarsus Pharmaceuticals达成产品引进战略合作协议。在相关条件获得满足后,远大医药将以1500万美元的首付款及一定金额的注册里程碑费用为代价,取得用于治疗蠕形螨睑缘炎及蠕形螨导致的睑板腺功能障碍的全球创新眼用制剂TP-03在大中华区(中国大陆、中国香港、中国澳门、中国台湾)的独家开发、生产及商业化权益。本次交易完成后,远大医药将大力推进TP-03在中国的注册落地工作,尽早惠及广大蠕形螨睑缘炎患者。
从滴眼液到凝胶、口服制剂

Tarsus正在推进其产品线,以解决一系列治疗需求未得到满足的疾病,包括眼部护理、皮肤病学和传染病预防。
根据该公司产品管线,Tarsus还在欧洲评估TP-03(lotilaner滴眼液)的无防腐剂配方版本,用于治疗蠕形螨睑缘炎;同时也在积极讨论TP-03(lotilaner滴眼液)在美国境外市场的合作机会。
除了滴眼液,Tarsus围绕lotilaner开发了多种制剂,并应用于不同的适应症,该公司认为lotilaner具有Pipeline in a product的潜力。
Tarsus正在开发的TP-04是lotilaner的凝胶制剂,被开发用于治疗玫瑰痤疮,又称酒渣鼻。
玫瑰痤疮是一种慢性皮肤疾病,其特征是面部发红、炎症性病变、灼热和刺痛,这些症状可能会因某些触发因素(如阳光照射或情绪压力)而爆发。根据美国国家玫瑰痤疮协会的数据,美国约有1600万人受到玫瑰痤疮的影响,另有一项研究估计,玫瑰痤疮的患病率约占全球人口的5.4%。据估计,约有55%的玫瑰痤疮患者是丘疹脓疱型玫瑰痤疮(PPR)。玫瑰痤疮的发病受多种因素影响,越来越多证据表明蠕形螨在发病过程中起重要作用,且研究发现PPR患者皮肤中的蠕形螨密度较高,并可能导致与该病相关的炎症反应。
Tarsus将TP-04开发为局部外用制剂,具有更长的半衰期、更高的亲脂性,以及更大的治疗窗口,最初用于治疗丘疹脓疱型玫瑰痤疮(PPR)。
2024年2月,Tarsus宣布评估TP-04(一种新型lotilaner凝胶制剂)治疗丘疹脓疱型玫瑰痤疮(PPR)的2a期Galatea试验获得积极结果。该试验表明,与安慰剂组相比,TP-04治疗组在第12周时的炎症病变和研究者的整体评估(IGA)评分具有统计学意义上的改善(p<0.05),且总体耐受性良好。该公司计划在2024年底前与FDA讨论并确定潜在的监管路径。
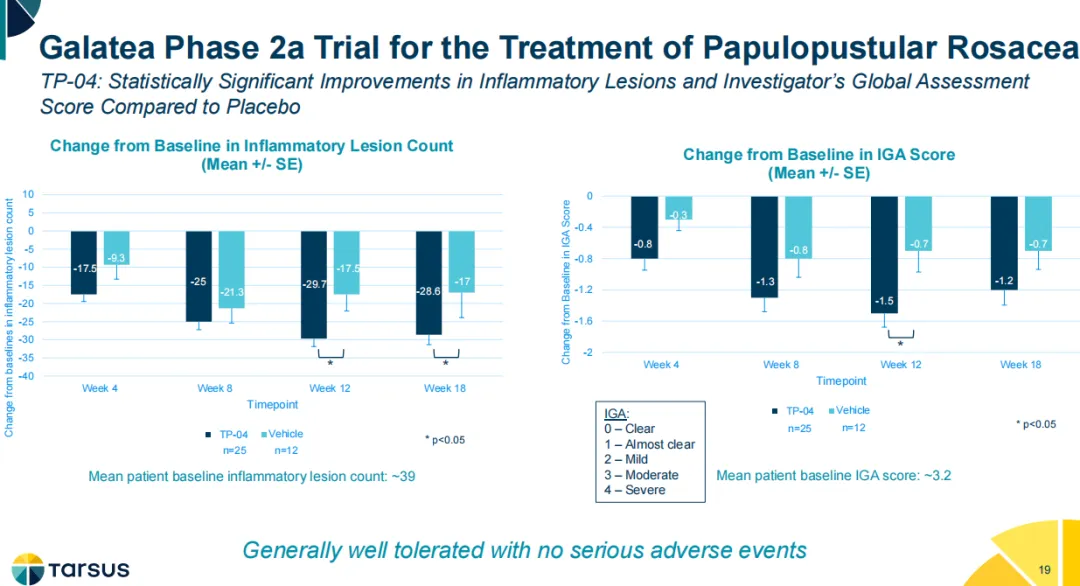
TP-05是lotilaner的口服片剂,正在被开发用于预防莱姆病。莱姆病是美国最常见的病媒传播疾病,由被蜱虫叮咬后疏螺旋体感染引起。该病可能是一种严重的疾病,可影响多个器官,产生广泛的症状。早期症状包括局部皮疹、发烧和疲劳,随着感染的传播,可能会演变为更严重的、有时是慢性的症状,包括发烧、肌肉和关节疼痛、外周和中枢神经功能缺损以及淋巴细胞性脑膜炎。据估计,美国每年莱姆病新发病例约为30万至40万例;美国约有8000万人面临接触莱姆病的风险,其中超过3000万人是中到高风险人群。
TP-05作为一种新型口服制剂,被设计为预防莱姆病的药物,以在蜱虫传播疏螺旋体细菌之前根除蜱虫。2024年2月,Tarsus宣布TP-05(lotilaner)的2a期概念验证研究获得积极顶线结果,这项随机、双盲、安慰剂对照试验评估了TP-05单次治疗(低剂量或高剂量)杀死附着在受试者身上蜱虫的能力。
研究显示,与安慰剂相比,高剂量和低剂量的TP-05在杀死蜱虫方面都显示出统计学意义上的显著益处。具体来说,在给药后第1天蜱虫暴露后,TP-05高剂量和低剂量组的24小时平均蜱虫死亡率分别为97.0%和92.0%,而安慰剂组仅为5.0%;同样,在给药30天后的蜱虫暴露中,TP-05高剂量和低剂量组的24小时平均蜱虫死亡率分别为89.0%和91.0%,而安慰剂组仅为9.0%。两个TP-05治疗组之间在蜱虫死亡率方面未观察到统计学上的显著差异,并且TP-05通常耐受性良好。Tarsus计划在2024年底前与FDA讨论并确定潜在的监管路径。
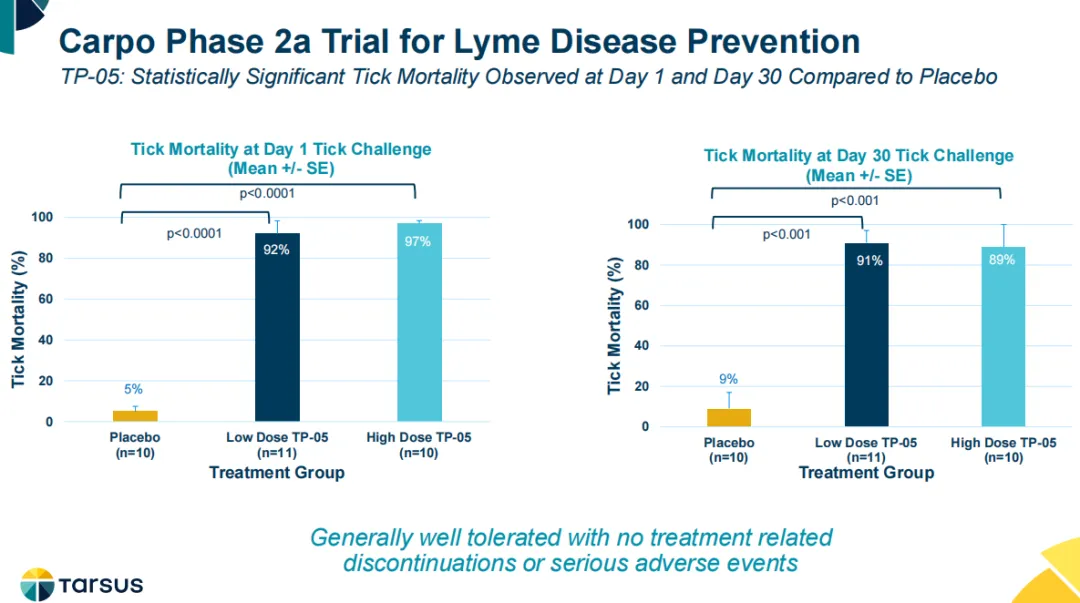
据该公司披露,TP-05是目前正在开发的唯一一种针对蜱虫的非疫苗的预防性药物,因此有可能成为首个和唯一一个长效的,按需口服的莱姆病预防性药物。
另据该公司官网显示,TP-05还可能导致传播疟疾的蚊子死亡。疟疾是世界上尚未得到满足的最严重的公共卫生需求之一,全世界约有2.47亿例病例,并导致60多万人死亡。
财务状况
2023全年,Tarsus Pharmaceuticals总收入1740万美元,其中XDEMVY(lotilaner滴眼液0.25%)产品业绩为1470万美元(8月下旬推出后大约四个月的销售额);全年R&D费用为5030万美元;SG&A费用为1.087亿美元;净亏损为1.359亿美元。自从8月份推出之后,XDEMVY(lotilaner滴眼液0.25%)在整个2023年开出了大约17400张处方。
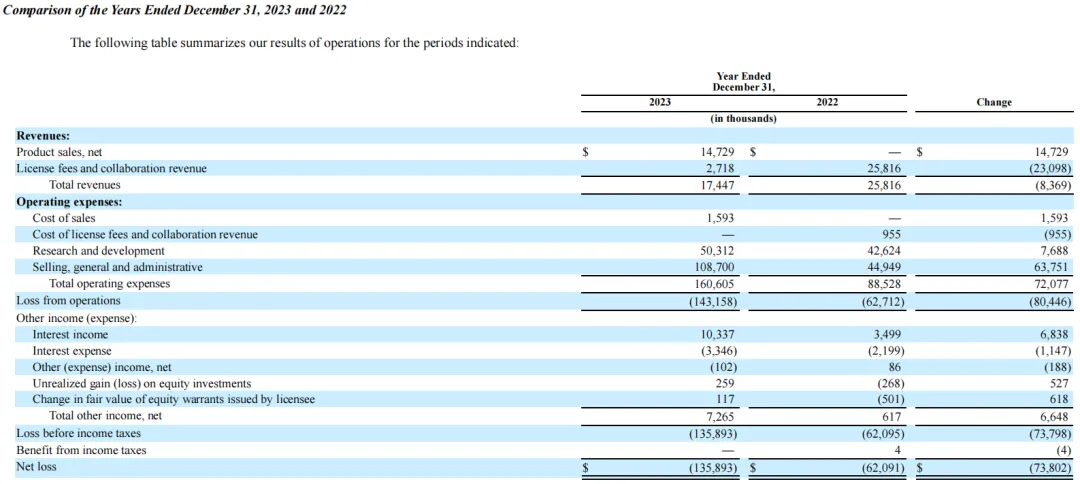
2023年间,Tarsus各项目研发开支如下:

2024年上半年,Tarsus Pharmaceuticals总收入6840万美元,其中XDEMVY(lotilaner滴眼液0.25%)产品业绩为6550万美元(第二季度业绩为4080万美元,比第一季度增长65%);上半年R&D费用为2440万美元;SG&A费用为1.104亿美元;净亏损为6900万美元。上半年该公司卖出XDEMVY(lotilaner滴眼液0.25%)约63000瓶(第二季度37000瓶,单瓶净价格超过1000美元)。
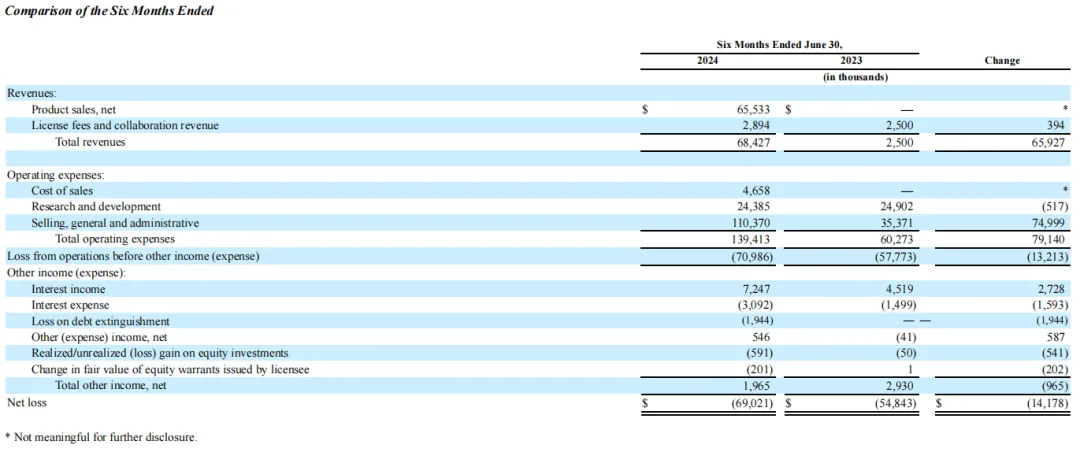
2024年上半年,Tarsus各项目研发开支如下:

截至2024年8月7日,已经有约11000名眼科护理专业人员(ECP)将XDEMVY(lotilaner滴眼液0.25%)作为患者的初始治疗方案,连续处方率超过60%。该公司计划在2024年第三季度末之前再招聘约50名销售人员。
截至2024年6月30日,Tarsus持有现金、现金等价物和有价证券为3.236亿美元。截至8月19日收盘,该公司市值10.08亿美元(约合72.1亿元人民币)。截止发稿前的9月3日收盘,市值约9.96亿美元。
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场,不作任何用药推荐
参考:
NMPA/CDE;
药融云数据www.pharnexcloud.com;
FDA/EMA/PMDA;
相关公司公开披露(正文图片均来自企业官方,除非另有说明);
https://tarsusrx.com/pipeline/;
https://xueqiu.com/S/00512/283800508;
https://investors.lianbio.com/zh-hans/news-releases/news-release-details/liantashengwugongbutp;
https://ir.tarsusrx.com/news-releases/news-release-details/tarsus-announces-positive-topline-results-carpo-phase-2a-proof;等等

 产业资讯
产业资讯
 药智网
药智网  2026-06-10
2026-06-10
 443
443

 产业资讯
产业资讯
 恒瑞医药
恒瑞医药  2026-06-10
2026-06-10
 397
397
 产业资讯
产业资讯
 氨基观察
氨基观察  2026-06-10
2026-06-10
 386
386
 热门资讯
热门资讯