 产业资讯
产业资讯
 Insight数据库
Insight数据库  2025-04-01
2025-04-01
 3327
3327
3 月 31 日,NMPA 官网显示,百时美施贵宝宣布欧狄沃 (纳武利尤单抗注射液) 与逸沃 (伊匹木单抗注射液) 的联合疗法获得中国 NMPA 批准新增适应症,适用于不可切除或晚期肝细胞癌 (HCC) 成人患者的一线治疗,成为中国首个且目前唯一获批的肝细胞癌一线双免疫联合疗法。

截图来源:百时美施贵宝官微
此次获批基于 III 期 CheckMate-9DW 研究的结果,该研究在全球范围内首次证实免疫治疗方案用于肝细胞癌一线治疗,疗效可显著优于两种既往标准治疗药物 (仑伐替尼或索拉非尼)。
CheckMate-9DW 是一项全球多中心、 III 期随机对照研究,评估了欧狄沃联合逸沃方案对比研究者选择的仑伐替尼或索拉非尼,在不可切除的肝细胞癌一线治疗患者中的疗效和安全性,其中 85% 的对照组患者使用了仑伐替尼。
研究主要终点结果显示:
欧狄沃联合逸沃组的中位总生存期 (mOS) 为 23.7 个月 (对照组为 20.6 个月),显著降低 21% 的死亡风险 (HR 0.79,p=0.018)。
次要终点方面,欧狄沃联合逸沃组的客观缓解率 (ORR) 为 36%,相比对照组 (13%) 改善近 3 倍; 中位缓解持续时间 (mDOR) 可达 30.4 个月,较对照组 (12.9 个月) 改善 2 倍以上。
研究中,欧狄沃联合逸沃方案整体安全性可控,未发现新的安全性信号,3/4 级治疗相关不良事件发生率为 41%(对照组 42%)。
CheckMate-9DW 临床结果

截图来自:Insight
数据库网页版CheckMate-9DW 研究 OS 结果
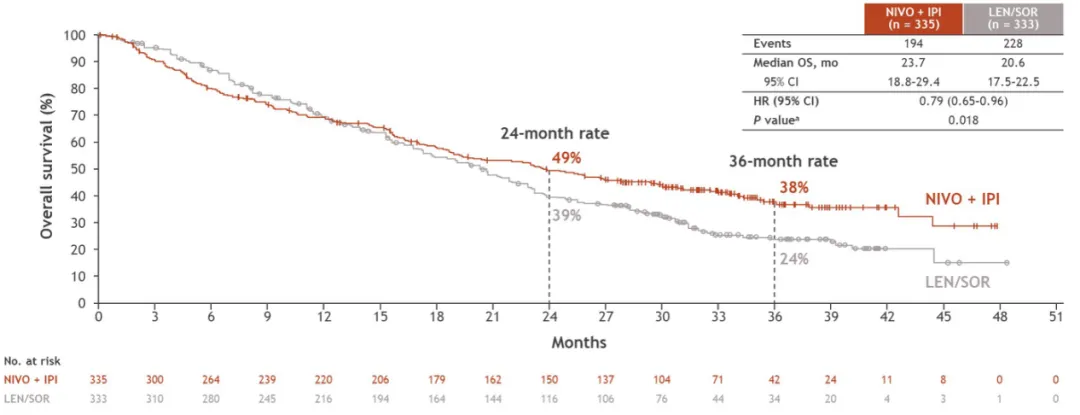
图源:2024 ASCO
在 2025 ASCO GI 中,研究者们又公布了亚洲亚组分析结果。结果显示,在亚洲患者中 O+Y 组(N=133)同样表现出相较于仑伐替尼/索拉非尼组(N=147)的 OS 获益,mOS 分别为 34.0 个月(95%CI,20.5-NE)vs 22.5 个月(95%CI,19.1-30.0),HR=0.75(95%CI,0.54-1.03);24 个月 OS 率分别为 54% 和 47%。
CheckMate-9DW 亚洲亚组数据
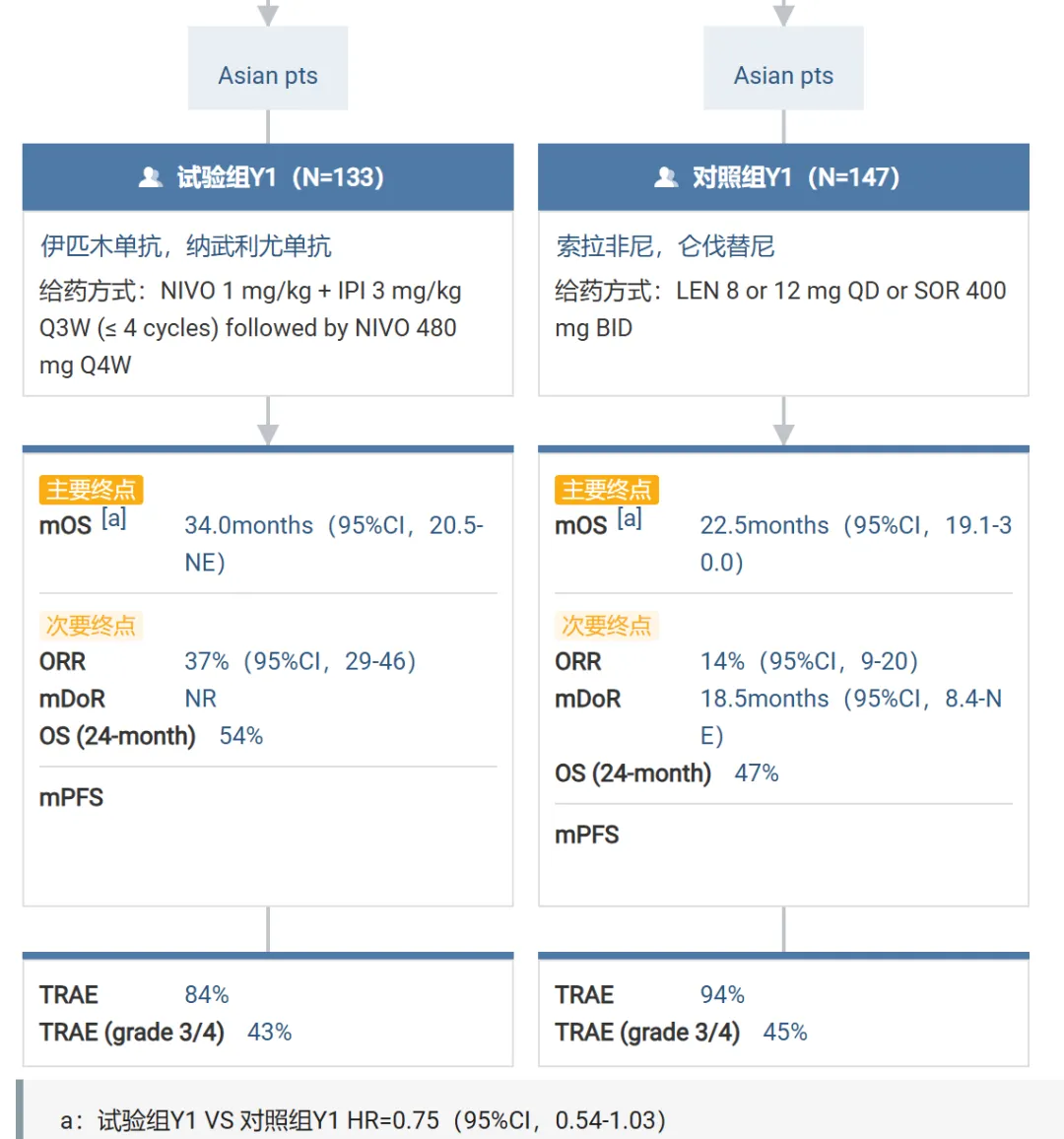
截图来自:Insight 数据库网页版
O 药作为 PD-1 单抗,可通过阻断 PD-1 与 PD-L1 的结合,恢复 T 细胞对肿瘤的识别和杀伤作用;而 Y 药作为 CTLA-4 单抗,对该通路的阻断可增强 T 细胞的活化与增殖。两者通过不同角度激活免疫系统,协同增效。
欧狄沃于 2014 年 7 月获批成为全球首个 PD-1 抑制剂,目前已在超过 65 个国家和地区获批共 12 个瘤种*,涵盖肺癌、头颈癌、胃癌、食管癌、肝细胞癌、肾癌、结直肠癌、尿路上皮癌、黑色素瘤、霍奇金淋巴瘤、胸膜肿瘤、不明原发部位肿瘤。
欧狄沃与逸沃于 2015 年 10 月获批成为全球首个获得监管机构批准的免疫肿瘤药物联合疗法,目前已在全球超过 50 个国家和地区获批共 7 个瘤种,涵盖黑色素瘤、肾癌、结直肠癌、肝癌、肺癌、胸膜肿瘤、食管癌。
欧狄沃是中国首个获批上市的免疫肿瘤药物。欧狄沃联合逸沃是中国首个获批上市的双免疫治疗。目前,以欧狄沃为基础的免疫治疗在中国已获批共 12 项适应症:
1. 欧狄沃适用于治疗表皮生长因子受体 (EGFR) 基因突变阴性和间变性淋巴瘤激酶 (ALK) 阴性、既往接受过含铂方案化疗后疾病进展或不可耐受的局部晚期或转移性非小细胞肺癌 (NSCLC) 成人患者;
2. 欧狄沃适用于治疗接受含铂类方案治疗期间或之后出现疾病进展且肿瘤 PD-L1 表达阳性 (定义为表达 PD-L1 的肿瘤细胞≥1%) 的复发性或转移性头颈部鳞状细胞癌 (SCCHN) 患者;
3. 欧狄沃可用于治疗既往接受过两种或两种以上全身性治疗方案的晚期或复发性胃或胃食管连接部腺癌患者;
4. 欧狄沃联合逸沃用于不可手术切除的、初治的非上皮样恶性胸膜间皮瘤成人患者;
5. 欧狄沃联合含氟尿嘧啶和铂类药物化疗适用于一线治疗晚期或转移性胃癌、胃食管连接部癌或食管腺癌患者;
6. 欧狄沃可用于经新辅助放化疗 (CRT) 及完全手术切除后仍有病理学残留的食管癌或胃食管连接部癌患者的辅助治疗;
7. 欧狄沃联合含氟嘧啶类和铂类化疗用于晚期或转移性食管鳞癌患者的一线治疗;
8. 欧狄沃联合含铂双药化疗适用于新辅助治疗可切除的 (肿瘤直径≥4 cm 或淋巴结阳性) 非小细胞肺癌 (NSCLC) 成人患者;
9. 欧狄沃适用于接受根治性切除术后伴有高复发风险的尿路上皮癌 (UC) 患者的辅助治疗;
10. 欧狄沃联合逸沃适用于不可切除或转移性微卫星高度不稳定性 (MSI-H) 或错配修复缺陷 (dMMR) 结直肠癌 (CRC) 患者的一线治疗;
11. 欧狄沃联合顺铂及吉西他滨用于不可切除或转移性尿路上皮癌成人患者的一线治疗;
12. 欧狄沃联合逸沃适用于不可切除或晚期肝细胞癌 (HCC) 成人患者的一线治疗。

 产业资讯
产业资讯
 药通社
药通社  2026-06-06
2026-06-06
 511
511

 产业资讯
产业资讯
 赛柏蓝
赛柏蓝  2026-06-06
2026-06-06
 411
411

 产业资讯
产业资讯
 摩熵医药
摩熵医药  2026-06-06
2026-06-06
 429
429
 热门资讯
热门资讯