 产业资讯
产业资讯
 潮药Bar
潮药Bar  2025-05-09
2025-05-09
 959
959
免疫检查点抑制剂联合疗法过去曾被市场寄予厚望,但随着CTLA-4应用场景低于预期、TIGIT全球集体折戟,使得市场大幅度降低了对于该方向的预期,而最近LAG3的成功,让免疫检查点抑制剂再重燃“心火”。
5月5日晚, Immutep宣布 TACTI-003 (KEYNOTE-C34) IIb 期试验的队列B结果,该研究评估了LAG-3融合蛋白Eftilagimodalpha(efti)联合K药作为复发/转移性头颈部鳞状细胞癌(1L HNSCC)患者作为一线疗法治疗PD-L1表达低于1(CPS<1)的患者,在31名患者中实现了17.6个月的出色中位总生存期 (OS),该结果显著优于包括“西妥昔单抗+化疗”10.7个月OS,和“PD-1+化疗”11.3个月OS,及PD-1单药治疗7.9个月OS的历史数据。
实际上,除了头颈癌的一线治疗外,efti过去在全人群的一线治疗NSCLC研究中也初步验证强有力的疗效,Immutep的成功将很可能带动新一波的LAG3研发热潮。
LAG3在PD-L1低表达或者阴性人群中优于PD-1的疗效,将是一块巨大的市场蛋糕。
01 | LAG3突破与首个上市单抗Relatlimab
虽然LAG3(淋巴细胞激活基因3)作为免疫检查点之一,学术界对其生物学理解存在知识空白,但目前大多数研究明确了LAG3在抑制T细胞活性促进肿瘤免疫逃逸的机制,其主要通过两种方式:
1)配体结合与泛素化激活:LAG3与配体(如MHC II类分子、FGL1)结合后,胞内结构域发生泛素化修饰并释放原本被膜隔离的信号基序,触发下游抑制信号通路并导致T细胞功能耗竭;
2)肿瘤微环境调控:LAG3在肿瘤微环境中高表达,通过抑制CD8+ T细胞的增殖和细胞毒性,同时促进调节性T细胞和肿瘤相关巨噬细胞的免疫抑制功能,形成免疫逃逸屏障。

(图源:中杉金桥)
显而易见的治疗策略是,研究者可以通过阻断LAG3与配体结合,来解除T细胞的抑制,目前全球开发主要包括单抗、融合蛋白和双抗的形式,全球首个获批的商业化药物便是BMS的LAG-3单抗Relatlimab,而Immutep的efti则是融合蛋白的形式。
Relatlimab首个获批适应症为与O药联用治疗一线转移性或不可切除的黑色素瘤患者,据RELATIVITY-047三期研究数据显示:联用组相比O药单药组在ORR、PFS、OS全面优胜,ORR为43.7% VS 33.7%。,mPFS为10.2个月 VS 4.6个月,mOS为51.9个月 VS 34.1个月;安全性方面,联合组和单药组3-4级不良反应率分别为22%和12%,毒性停药率为18%和10%。
另外Relatlimab在肺癌领域也展现出强大潜力,在治疗IV期或复发性非小细胞肺癌(NSCLC)患者一线疗法的RELATIVITY-104二期研究显示,Relatlimab+O药联合化疗对比O药联合化疗的ORR、mPFS分别为51.3% VS 43.7%、6.7个月 VS 6个月,这样看上去并不显著。但该组合在PD-L1表达≥1%且组织学为非鳞状细胞的患者亚组中展现出惊艳数据,Relatlimab+O药联合化疗组的ORR为58%、mPFS为11.6个月,而对照组的ORR为39.6%、mPFS为6.9个月。
这也进一步展现出LAG-3联用PD-1在PD-L1低表达实体瘤人群的广阔潜力,另外Relatlimab在头颈癌、MSI-H结直肠癌也展现出积极的疗效。
Opdualag(relatlimab+nivolumab)固定剂组在2023年销售额达到了6.27亿美元,而Evaluate分析师预期其未来在2028年有望达到23.5亿美元。
02 | Immutep的efti,创新点和潜力?
Immutep的efti作为一种可溶性LAG-3融合蛋白,其作用机理和BMS的T细胞检查点抑制剂Relatlimab有着显著差异。
efti对抗原呈递细胞(APC)表面的MHC-II分子具有高亲和力,通过APC表面的MHC-II分子激活APC功能,促进T细胞活化和细胞因子释放(有人说其更像是促进DC细胞成熟免疫激活佐剂)。
efti的差异化设计也给自身带来几大好处:1)联合PD-1时efti可通过激活APC间接增强T细胞功能,叠满疗效增强的Buff;2)其作为融合蛋白,分子量小,可采用皮下注射,患者依从性更高;3)潜在安全性好。
除了最新公布的1L HNSCC总生存期数据外,efti目前已经启动全人群1L NSCLC临床III期,旨在探索efti+K药+化疗与K药+化疗+安慰剂组的头对头疗效与安全性的比较,预计将在2026年底到2027年中进行期中分析。
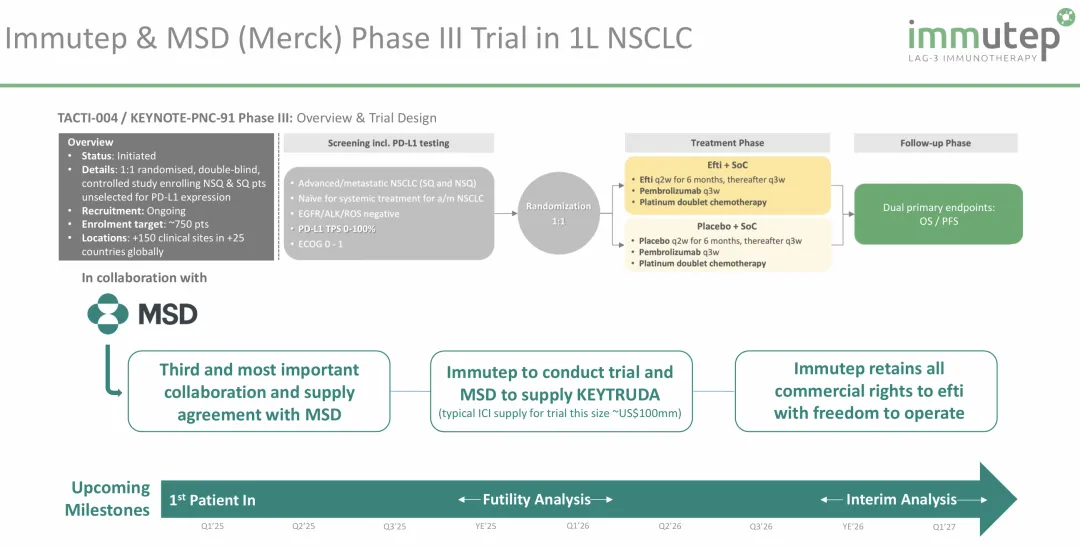
而从efti已披露的治疗1L NSCLC的TACTI-002二期研究中(75%入组患者PD-L1 TPS
<50%,其中包括35%PD-L1为阴性表达;其余25% 患者PD-L1 TPS
≥50%)中,在意向治疗人群中mDoR达到21.6个月,mOS为20.2个月;而在PD-L1 TPS
≥1%的患者中,ORR高达48.3%,mPFS为11.2个月,mOS更是达到35.5个月,并且在所有PD-L1表达组患者均显示出有希望的疗效。
除了肺癌、头颈癌之外,efti在2024 ESMO上公布AIPAC-003临床2/3期试验安全性引导部分结果,接受efti+紫杉醇联合治疗的转移性乳腺癌患者的ORR为50%,DCR为100%,同时公司正在持续探索efti在转移性尿路上皮癌、软组织肉瘤、转移性黑色素瘤和自身免疫性疾病的应用。

从远景来看,efti如若真能兑现在如肺癌、乳腺癌等大癌种一线联用PD-1治疗的潜力
03 | 国内拥有LAG3管线的公司
目前国内拥有LAG-3临床管线的公司并不少,比如恒瑞医药、信达生物、康方生物、复宏汉霖等公司均有相关资产。
不过受制于BMS的LAG-3单抗临床进展,不少国内企业近两年都没有公布过关于LAG-3管线的最新数据。
正大天晴的LAG-3单抗TQB2223是少数公布临床数据的国产分子之一,在拥有21名复发/难治淋巴瘤患者的一期临床中,ORR为52.38%、DCR为80.95%,6个月PFS率为88.54%,6个月DOR率为100%。
更大的看点,其实在于国内LAG-3双抗的发力。

(国内LAG-3管线进展 图源:建投医药)
以康方生物的PD-L1/LAG3双抗AK-129为例,其能够实现单一分子同时阻断PD-1/PD-L1和LAG-3/MHC-II信号通路减少免疫逃逸,临床前研究显示其抗肿瘤活性显著优于BMS的Relatlimab;在适应症布局方面,其选择联合AK-104及化疗治疗HER2阴性胃癌/胃食管结合部腺癌,还有单药或联合AK117治疗PD-1/L1抑制剂治疗失败的复发或难治性经典型霍奇金淋巴瘤、晚期恶性肿瘤等。
泽璟制药的ZGGS15是全球首个LAG-3/TIGIT双抗,一方面可抑制LAG-3与MHC-II等配体的结合,另一方面阻断TIGIT与PVR配体的相互作用,临床前数据显示:在小鼠模型中ZGGS15联合抗PD-1抗体抑制肿瘤生长率达95.8%。适应症布局方面,预计公司进行广谱适应症布局,重点聚焦关注PD-L1低表达及“冷肿瘤”患者的疗效突破。
就如康方生物的AK112去迭代K药、PD-1与VEGF联合疗法一样,在LAG-3已经初见广谱疗效潜力的背景下,LAG-3/“X”将是更迭代的新疗法,冲击更大的实体瘤市场,同时也留下了更多的BD可能性。
Immutep的efti激活了沉寂已久了LAG-3市场,潜在巨大的市场空间值得重视。

 产业资讯
产业资讯
 Innodrugs
Innodrugs  2026-03-23
2026-03-23
 27
27

 产业资讯
产业资讯
 药渡
药渡  2026-03-23
2026-03-23
 23
23

 产业资讯
产业资讯
 药融圈
药融圈  2026-03-23
2026-03-23
 21
21