 产业资讯
产业资讯
 药智网
药智网  2025-05-14
2025-05-14
 1232
1232
4月,CDE共将6个品种纳入了优先审评名单,其中5个化药品种,1个生物制品品种,中药未有品种纳入优先审评(详见文末表3)。
1.申报情况
4月CDE共受理新的药品注册申请1168个品种(受理号1521个)。按药品类型统计,化药722个品种,中药283个品种,生物制品163个品种。以审评任务类型统计,受理新药临床试验申请(以下简称IND)174个品种;新药上市许可申请(以下简称NDA)38个品种;同名同方药、仿制药、生物类似药上市许可申请(以下简称ANDA)312个品种;仿制药质量和疗效一致性评价注册申请(该注册申请类别以下简称一致性评价申请)19个品种。
以注册分类统计,1类创新药受理147个品种,同比增长23.53%,IND申请136个品种,NDA申请11个品种。化药创新药上市申请4个品种,分别是礼来申报的Imlunestrant片、诺诚健华医药科技申报的卓乐替尼片、南京征祥医药和江苏宣泰药业共同申报的玛硒洛沙韦片,以及百济神州的索托克拉片;中药创新药上市申请4个品种,分别是以岭药业的芪桂络痹通片、浙江宝仁堂药业和北京亚东生物共同申报的三贝苎鼾胶囊、成都百裕制药的银杏总内酯滴丸及其原料药;生物制品创新药上市申请3个品种,分别是默沙东的Clesrovimab注射液、康乐卫士(昆明)的重组三价人乳头瘤病毒(16/18/58型)疫苗(大肠杆菌),以及强生制药的尼卡利单抗注射液。
2类改良型新药注册申请受理43个品种,化药申请27个品种,中药申请3个品种,生物制品申请13个品种。其中2.2类申报最多,有24个品种;其次是2.4类,10个品种。
表1 2025年4月创新药与改良型新药注册申请受理情况
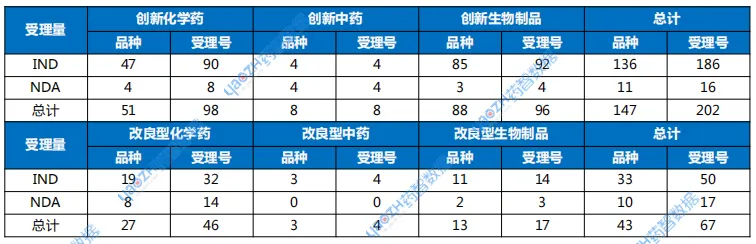
中药3类经典名方注册申请受理2个品种,为浙江维康药业的二冬汤颗粒,以及安徽华润金蟾药业的开心散。
3类化学仿制药注册申请受理122个品种,验证性临床申请6个品种,上市申请116个品种。4类化学仿制药受理209个品种。中药同名同方药受理1个品种,为宁波卓仑医药和宁波立华制药共同申报的西帕依固龈液。生物制品3.3类生物类似药受理7个品种,其中预防用生物制品2个品种,治疗用生物制品5个品种。
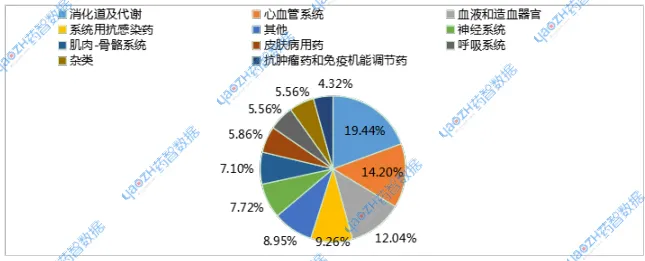
图1 2025年4月化学仿制药申报品种ATC分布情况
2.完成审批情况
4月NMPA完成审批1131个品种(受理号1508个),其中化药735个品种,中药171个品种,生物制品225个品种。以审评任务类型统计,IND申请完成审批192个品种,NDA申请35个品种,ANDA申请295个品种,一致性评价品种50个品种。按药智审评结论统计,批准临床257个品种,批准生产276个品种,批准进口25个品种,未被批准96个品种。
以注册分类统计,1类创新型新药完成审批150个品种,IND申请完成审批143个品种,NDA申请7个品种,批准率均为100%。2类改良型新药完成审批57个品种,IND申请完成审批44个品种,NDA申请完成审批13个品种,批准率均达100%。中药3类经典名方完成审批4个品种,批准率为75%。
3类化学仿制药申请完成审批155个品种,批准临床21个品种,批准生产118个品种,未被批准16个品种。4类化学仿制药申请完成审批152个品种,批准临床2个品种,批准生产140个品种,未被批准10个品种。生物制品3.3类生物类似药完成审批3个品种,批准临床1个品种,批准生产2个品种。
表2 2025年4月新药上市申请审评结论情况
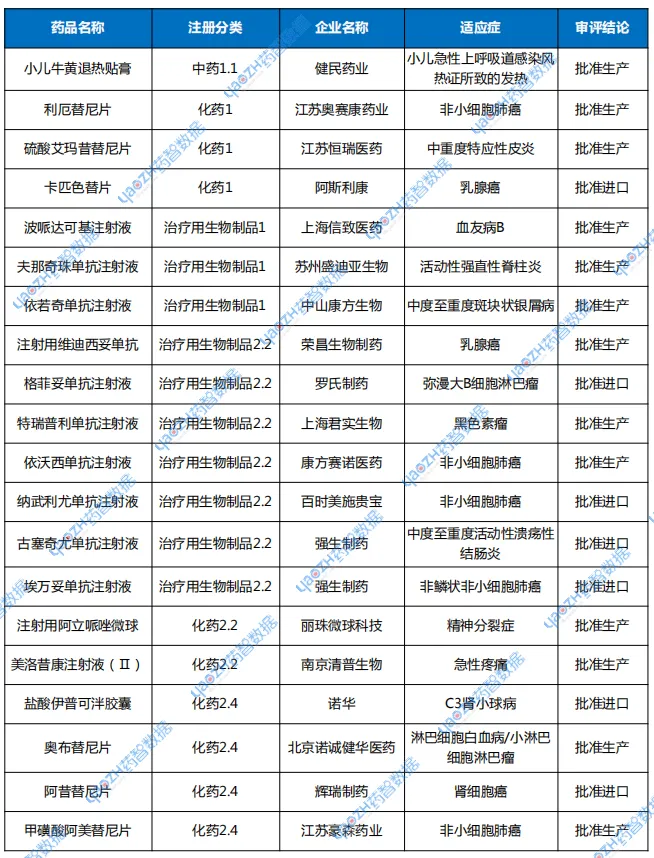
注:数据统计至2025年5月12日。
3.优先审评与突破性治疗品种
4月CDE共将6个品种纳入了优先审评名单,其中5个化药品种,1个生物制品品种,中药未有品种纳入优先审评。纳入优先审评理由涉及“儿童用药”“附条件批准”等。
突破性治疗品种名单有10个品种,4个化药品种,6个生物制品。涉及非小细胞肺癌、实体瘤等适应症。
表3 2025年4月优先审评与突破性治疗品种名单
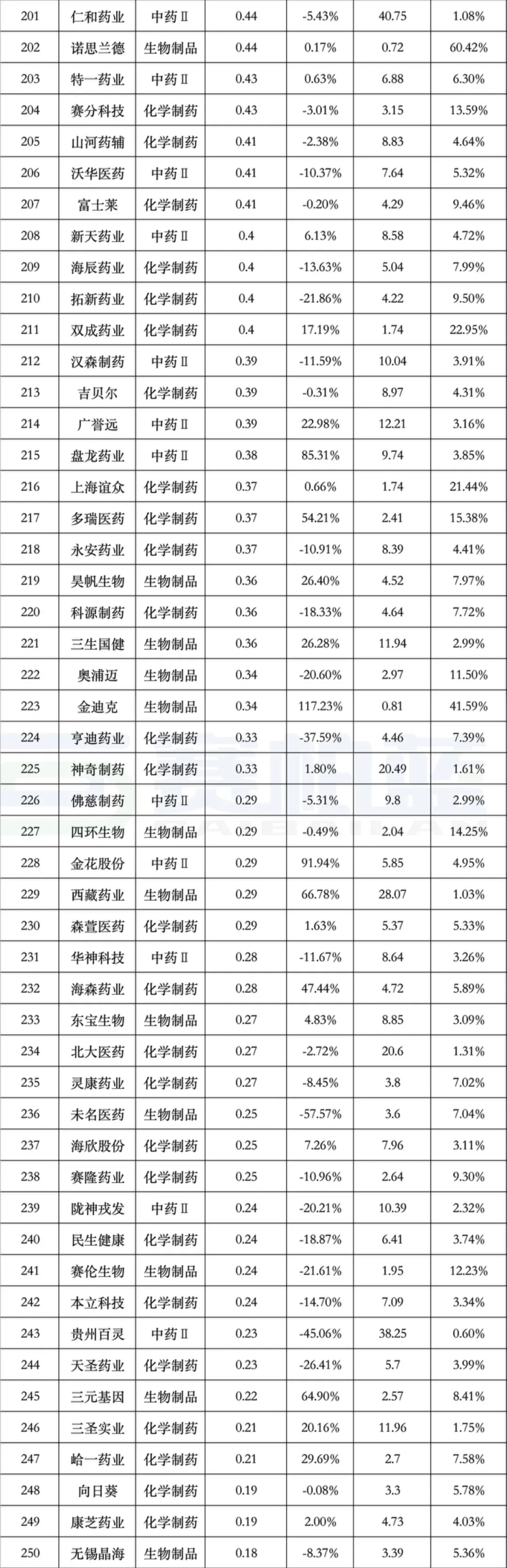
注:数据按公示日期进行统计。

 产业资讯
产业资讯
 Innodrugs
Innodrugs  2026-03-23
2026-03-23
 14
14

 产业资讯
产业资讯
 药渡
药渡  2026-03-23
2026-03-23
 12
12

 产业资讯
产业资讯
 药融圈
药融圈  2026-03-23
2026-03-23
 12
12