 产业资讯
产业资讯
 药时空
药时空  2025-05-26
2025-05-26
 1161
1161
5月22日,据行业知名媒体Fierce Biotech报道,吉利德支付1000万美元以获得与Hookipa Pharma公司长期合作开发的针对乙型肝炎(HBV)和艾滋病毒(HIV)的沙粒病毒免疫疗法的全部所有权。
Hookipa Pharma成立于2011年,总部位于纽约和维也纳,是一家专注于开发免疫疗法的生物技术公司。公司自主研发的沙粒病毒平台,通过“重新编程”免疫系统,帮助人体识别并清除病毒或肿瘤细胞,应用领域涵盖传染病与肿瘤治疗。
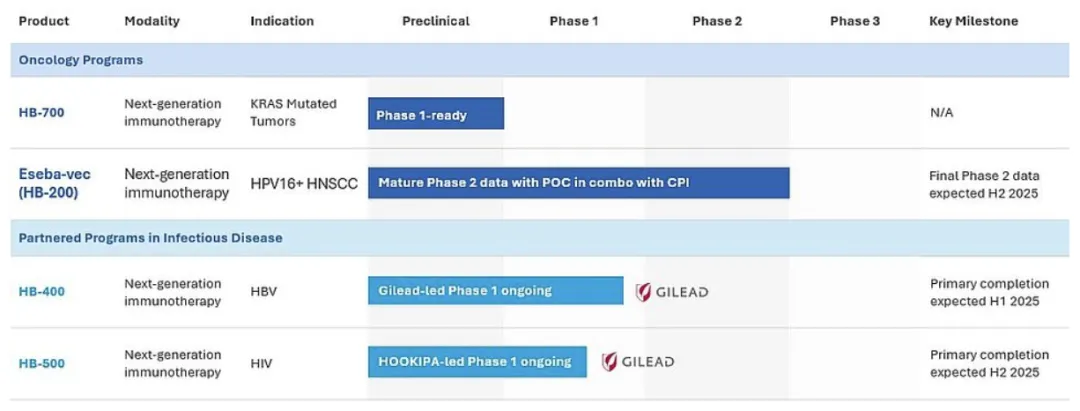
图1:Hookipa Pharma的在研管线
本次交易涉及的两款治疗性疫苗分别为:
1、HB-400
一种针对慢性HBV的沙粒病毒治疗性疫苗。GS-2829 + GS-6779是两种基于病毒载体的疫苗成分,是基于Hookipa的非复制性沙粒病毒载体(arenavirus vector)疫苗接种技术平台开发,分别使用了淋巴细胞性脉络丛脑膜炎病毒(LCMV)和水疱性口炎病毒(VSV)载体。这些载体经过改造,能够表达HBV抗原,从而激活宿主的免疫反应。
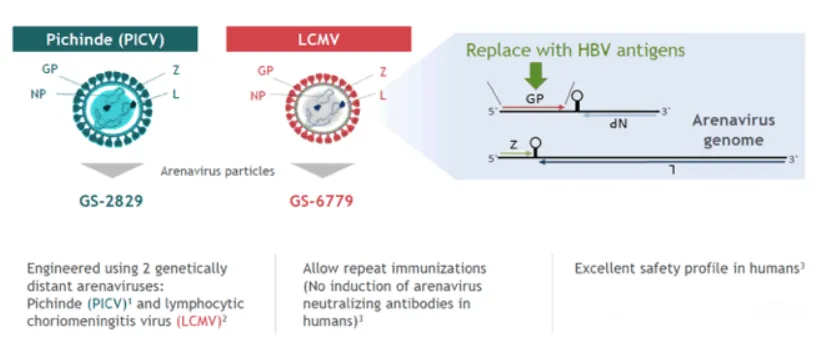
图2:HB-400
早在2023年,Hookipa便启动了HB-400的1a/1b期试验。在荷兰阿姆斯特丹举办的2025年欧洲肝病年会(EASL2025)上,研究人员公布了GS-2829 + GS-6779这两款治疗性疫苗正在进行的旨在评估药物安全性、耐受性和免疫原性的1a期研究(NCT05770895)结果。
结果显示,单次和交替的病毒载体给药均安全且耐受良好。疫苗引发的免疫反应与剂量相关;在几名参与者(C8)中,第5和第6剂的增加进一步提高了T细胞反应的幅度。参与者对所有疫苗编码的HBV抗原产生了HBV特异性T细胞且伴随持续高幅度的抗HBsAg。
2、HB-500
一种针对HIV的沙粒病毒治疗性疫苗。该疫苗利用基于沙粒病毒Pichinde病毒和淋巴细胞性脑膜炎病毒的两个复制载体。这些载体递送来自HIV-1蛋白免疫原区域的HIV抗原,这些区域在HIV-1 B型变体中高度保守。免疫原之间的氨基酸序列不同,允许覆盖超过80%的循环HIV-1病毒变体。
2025年1月,Hookipa宣布完成其评估HB-500治疗HIV的Ib期临床试验的招募。该试验涉及30名参与者,预计将在2025年下半年完成主要终点。根据近日签署的交易协议,将涉及Hookipa逐步结束HB-500的1期研究,而不是由吉利德接手推进。
吉利德与Hookipa的合作关系可以追溯到2018年,当时该公司首次授权使用沙粒病毒免疫技术对抗HBV和HIV。2021年,吉利德决定不将由此产生的HIV免疫疗法推进到临床阶段,但在2022年重新考虑后更新了合作。
当时,吉利德支付了1500万美元的预付款以及500万美元的股权投资。该原始协议的条款包括吉利德可能支付1000万美元的项目完成费,并附带另外1.625亿美元的开发里程碑付款以及高达6500万美元的商业化里程碑付款。
现在,吉利德决定将这2款候选疫苗完全掌控在自己手中。根据5月22日提交给美国证券交易委员会的一份文件,吉利德将为此总共支付1000万美元,其中300万美元将在交易结束时支付,剩余的700万美元将分三阶段支付,对应技术转移计划的推进步骤。
去年,吉利德在艾滋病病毒相关产品中的销售额总计达到196亿美元,其中以抗逆转录病毒药物必妥维(Biktarvy)和抗病毒药物德斯科维(Descovy)为主力产品。虽然该公司尚未将治疗性疫苗推向市场,但随着公司准备将其已获批的HIV长效预防用药Lenacapavir投入暴露前预防(PrEP)市场,这种情况似乎将在未来几周内发生变化。
在HBV方面,吉利德已经在销售抗病毒药物Vemlidy,而HB-400治疗性疫苗或将为公司在该领域上再次加码,提供替代产品。今年到目前为止,Vir Biotechnology和GSK都放弃了针对该病毒的拟议“功能性治疗方法”,尽管GSK仍在开发另一种药物。
值得注意的是,最近几个月,Hookipa接连传出坏消息:2月取消了与Poolbeg Pharma的合并计划,此前其还经历了艰难的2024年,其中包括在罗氏退出其KRAS突变癌症HB-700项目的合作后进行裁员30%。在这种情况下,吉利德选择购买HB-400和HB-500的所有权,可见其对于Hookipa的这两款治疗性疫苗项目的看好。
原文链接:

 产业资讯
产业资讯
 2026-03-20
2026-03-20
 38
38

 产业资讯
产业资讯
 BiG生物创新社
BiG生物创新社  2026-03-20
2026-03-20
 37
37

 产业资讯
产业资讯
 医麦创新药
医麦创新药  2026-03-20
2026-03-20
 35
35