 产业资讯
产业资讯
 生物制药小编
生物制药小编  2025-06-11
2025-06-11
 1128
1128
随着生物制药行业的逐步发展,癌症疫苗已经不是新鲜的概念,不过你有听过高血压疫苗吗?
近日,根据CDE官网公布的6月7日消息,武汉华纪元生物已经向NMPA提交了HJY-ATRQβ-001注射液的新药临床申请。
根据公开渠道消息可知,HJY-ATRQβ-001注射液是一款用于预防高血压的疫苗,本文将就高血压疫苗管线的发展历史进行简单介绍。
肾素疫苗
在上世纪有人尝试使用肾素作为高血压疫苗,肾素是由肾脏球旁细胞产生和分泌的一种蛋白水解酶,能够催化血管紧张素原(AGT)转化为血管紧张素I(Ang I)。
血管紧张素I在血管紧张素转换酶(ACE)的作用下进一步转化为血管紧张素II(Ang II)。而血管紧张素II是强效的血管收缩剂,可导致血压升高,同时促进醛固酮分泌,增加水钠潴留,进一步升高血压。(这也是为什么血管紧张素Ⅱ受体阻滞剂在心血管领域中得到大规模应用)理论上,抑制其活性可从源头阻断高血压的关键病理通路。
然而,实践中却发现,通过注射外源性肾素来诱导肾素抗体针对人体肾素的操作很容易会让人体换上自免疾病。患者的血压确实有降低,但是因此患上了自免肾病。
因此安全性问题让人们对于肾素疫苗开发望而却步。
Ang I疫苗
后来的尝试则试图通过肾素以外的通路入手,如英国Protherics公司试图开发一款针对Ang I的疫苗PMD-3117,旨在通过诱导机体产生针对Ang I的抗体,阻断肾素-血管紧张素系统(RAAS)的激活,从而降低血压。
然而,实际临床中发现降压效果并不明显。
原因可能包括抗体滴度不足以显著降低血压,以及Ang I抗体主要存在于血浆中,无法有效阻止组织中的Ang I转化为Ang II。
为了提高疫苗效果,研究人员尝试将PMD-3117的佐剂调整为“CoVaccine HTTM”(水包油佐剂),该佐剂能刺激疫苗中的抗原成分产生更强的B细胞免疫反应,提高抗原相关免疫球蛋白G抗体的形成。然而,自从2008年出现了相关严重剂量相关性不良反应,II期临床最终于2010年终止。
同济大学附属医学院的Fang Hong等人将内源性 AngⅠ与牛血清白蛋白共价结合,以氢氧化铝作为佐剂,研制出血管紧张素肽(angiotensin peptides, Ang I-R)。在小鼠模型中成功降低了血压,不过未见后续临床。
Ang II疫苗
瑞士Cytos公司研制的针对血管紧张素II的CYT006-AngQb疫苗曾经被认为是极有希望的降压疫苗。其具体机制在于疫苗本身含有与Ang II结构相似的抗原表位。当疫苗被注射到体内后,抗原呈递细胞(如树突状细胞)会摄取并处理这些抗原,将其呈递给T细胞和B细胞。
B细胞在抗原刺激和T细胞辅助下,会分化为浆细胞并产生特异性抗体。这些抗体能够识别并结合Ang II,从而中和其活性。
在后续临床试验中,与安慰剂组相比,该疫苗的高剂量组将受试者的日间平均动态血压从基线水平下调-9/-4mm Hg,可惜的是,这一降压幅度还不能完全满足临床实际要求。而且该疫苗的降压效果可能因个体差异而异,部分患者可能对疫苗无应答。这可能和疫苗产生的抗体亲和力太低有关系,抑或是针对血管紧张素II疫苗免疫会诱导肾素-血管紧张素系统反馈激活有关,这可能在一定程度上削弱了疫苗的降压效应。
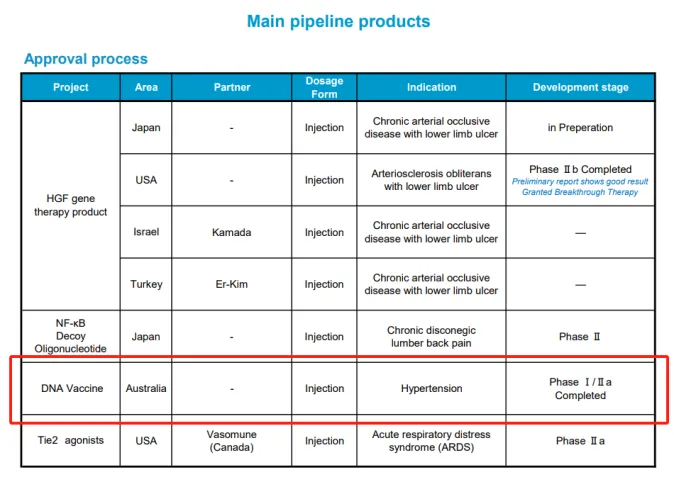
另外,大阪大学的Nakagami团队及大阪大学发起的风投制药公司AnGes共同开发了多款Ang II疫苗,每一款都在原有基础上进行改进和迭代,根据公司官网消息和公开渠道,该Ang II疫苗似乎几年前就在澳大利亚完成了II期临床,但是未见下文。
Ang II1R疫苗
Ang II通过两种受体亚型发挥作用:AT1R和AT2R。AT1R介导了Ang II的绝大多数病理生理效应,包括血管收缩、血压升高、心肌肥厚、纤维化及炎症反应等。相比之下,AT2R的作用尚不完全明确,但可能与血管扩张、抗增殖及组织修复相关。
靶向AT1R被认为是规避肾素-血管紧张素系统(RAS)的反馈激活机制的一种方法。
2006年武汉华纪元生物的创始人廖玉华及其团队开发一款AngⅡ受体疫苗ATR-12181。它由鼠源性AT1R的抗原短肽、TT和弗氏佐剂组成。
后续在2013年廖玉华团队开发了ATRQβ-001,这是一款从人AT1R的胞外第二环中选取线性表位ATR-001与Qβ噬菌体VLP 结合制成 ATRQβ-001疫苗。ATRQβ-001疫苗具有更长的抗体半衰期(14.4天)
在ATRQβ-001疫苗组中,也未观察到循环或局部肾素-血管紧张素系统(RAS)的明显反馈激活。同年华纪元生物成立。
2017年,廖玉华团队还开发人血管平滑肌细胞L型钙通道和血管紧张素1型受体的嵌合型二价降压疫苗,这是在现有疫苗开发针对单一靶点的情况下进行的优化设计。
团队找到一段来源于L型CaV1.2钙通道的线性表位,它能诱导针对L型钙通道的特异性抗体,并且降低高血压动物模型的血压,因此可以作为另一个新的治疗性高血压疫苗靶点。
东京大学的Tatsuhiko Azegami团队开发了一款血管紧张素II型受体-肺炎球菌表面蛋白A (AT1R-PspA)疫苗。该AT1R部分肽与PspA和环二胍盐一磷酸佐剂缀合,可通过鼻内给予自发性高血压大鼠(SHR)。用AT1R-PspA疫苗进行鼻内免疫具有同时减弱高血压发展和保护免于致死性肺炎球菌感染的潜力。

 产业资讯
产业资讯
 2026-03-20
2026-03-20
 16
16

 产业资讯
产业资讯
 BiG生物创新社
BiG生物创新社  2026-03-20
2026-03-20
 16
16

 产业资讯
产业资讯
 医麦创新药
医麦创新药  2026-03-20
2026-03-20
 15
15