 产业资讯
产业资讯
 瞪羚社
瞪羚社  2025-08-09
2025-08-09
 525
525
8月6日夜间,一项收购预告点燃了大家对一个新兴治疗领域的热情,据金融时报消息称:诺华计划收购Avidity Biosciences;受消息影响,公司当天股价大涨26%,市值达到58亿美元。
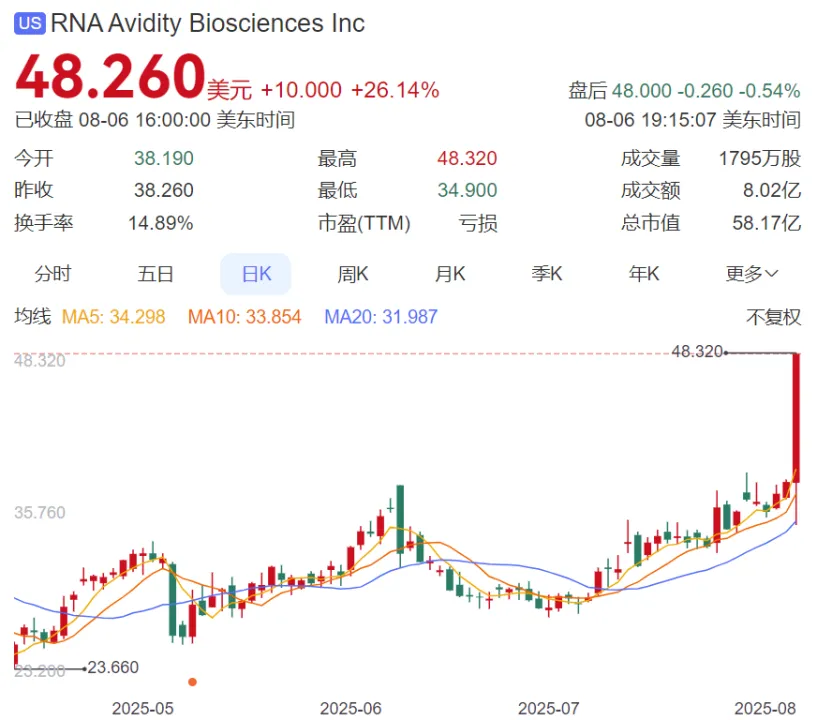
Avidity
Biosciences作为抗体偶联小核酸(AOC)的先驱Biotech,这次收购可以看做是MNC对该类技术的一次强烈的认可,同时也告诉国内投资者要开始重视起AOC技术,说不定未来国内的AOC研发biotech也有机会和MNC发生大规模的BD交易了。
01
AOC技术机制
AOC技术是典型的偶联技术,我们可以回顾一下ADC这一技术的结构:用来定向的抗体,用来连接抗体和毒素的连接子,以及用来杀伤的毒素。那么AOC呢?它的其它结构也类似,只是把毒素换成了寡核苷酸。ADC 成功的基础上,AOC作为一种新型融合物应运而生,它将siRNA和ASO的精确性与抗体的靶向递送能力相结合。
核酸疗法因其利用核苷酸序列在基因水平上调节细胞功能的能力而备受关注。通过引入外源核酸来纠正基因缺陷,这些疗法可以为遗传性疾病和获得性疾病(例如遗传疾病、癌症、病毒感染和神经系统疾病)提供高度针对性和持久的治疗效果。寡核苷酸是核酸疗法的一个子类,因其体积小、易于合成、特异性高、靶点广泛和毒性低而著称
,用它作为payload,是ADC基础上下一代偶联物的一大重要探索。
抗体上没有太多可说的,虽然mAb仍然是目前最为主流的选择,但是抗体片段由于体积更小、耐受性更好、激活免疫系统的风险更低,作为替代递送载体已引起人们的关注。这些片段,如Fab、单链可变片段(scFv) 或纳米抗体(源自骆驼科动物的VHH),保留了全尺寸IgG的结合特性,同时具有独特的优势。例如,纳米抗体对抗原表现出亚纳摩尔亲和力、更短的血清半衰期和增强的组织穿透性,使它们能够进入细胞并将功能分子递送到细胞质。
寡核苷酸选择上,有ASO和miRNA等。ASO上有比较典型的临床前治疗案例:Satake等人通过将MXD3 ASO与抗CD22抗体(αCD22抗体)结合,开发出一种新型白血病靶向剂,用于治疗前体B细胞淋巴细胞白血病(pre-B ALL),并证明了显著的体外和体内治疗效果。以所检查的最小剂量施用结合物,显著延长了Reh(中位生存时间从20.5天增加到 42.5天,p < 0.001)和原发性preB ALL(中位生存时间从29.3天增加到63天,p < 0.001)异种移植模型中小鼠的寿命 。
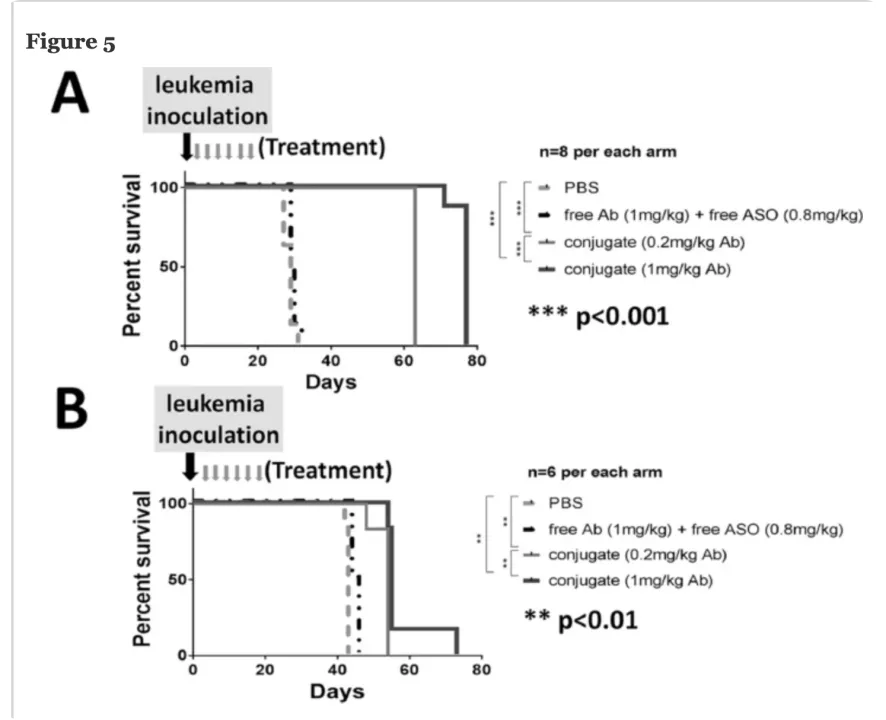
(图源:Novel Targeted Therapy for Precursor B-Cell Acute Lymphoblastic Leukemia:
Anti-CD22 Antibody-MXD3 Antisense Oligonucleotide Conjugate)
miRNA上,Yamayoshi等人开发了ExomiR-Tracker,一种抗外泌体抗体-抗miRNA受体复合物,通过外泌体将抗mirna递送至受体细胞。ExomiR-Tracker与外泌体结合并在体外和体内抑制miRNA功能。划痕试验显示,ExomiR-Tracker可有效将细胞生长降低至32%。
linker上,和ADC对linker的要求是类似的,目前不同类型的已经公开的linker如图所示。半胱氨酸和赖氨酸残基通常用作AOC的结合位点。半胱氨酸残基中的硫醇基团可与寡核苷酸上的硫醇反应性官能团(例如马来酰亚胺或硫醇修饰的连接体)发生反应,而赖氨酸中的伯胺基团则可作为寡核苷酸的直接结合位点,例如使用琥珀酰亚胺酯或N-羟基琥珀酰亚胺官能化的二苯并环辛炔连接体。具有天然反应性赖氨酸残基的抗体可通过分子内酰胺键促进位点特异性siRNA的连接。

(图源:Overcoming limitations and advancing the therapeutic potential of
antibody-oligonucleotide conjugates (AOCs): Current status and future
perspectives)
结构拆解大致如此。
02
Avidity——AOC老将
说Avidity是AOC概念第一股并不过分,它成立于2012年,IPO于2020年,也历经了十几年的岁月的洗礼。笔者认为该公司在对于小核酸的理解上,有着非常独到的一点:发明了一种独到的递送方式——肌肉递送。因为RNA递送一直以来都是老大难的问题,要么是技术瓶颈,要么是专利被卡,而Avidity算是走出了一条属于自己的路。在平台之上,才是Avidity的管线。

其目前首当其冲的管线是Del-zota,主要适应症是杜氏肌营养不良症(DMD)
。该病也是罕见病中的经典病种,其发病机理是由于患者体内编码抗肌萎缩蛋白(dystrophin)的基因发生变异,导致抗肌萎缩蛋白的缺失或功能缺陷。在临床表现上,患者会出现全身肌肉渐进式退化和运动功能减退,同时也会影响心脏功能与呼吸系统。患病人数上,全球每5,000名活产男婴中约有1名患有此病,每年全球约有20,000例新诊断病例。虽然全球确切的患病率各不相同,但估计有全球有超过300,000人患有DMD,其中美国患病人数约为1万5千例。
而Del-zota旨在将磷二酰胺吗啉寡聚体 (PMO) 递送至骨骼肌和心脏组织,以特异性地跳跃抗肌萎缩蛋白基因的第44号外显子,从而使携带可进行第44号外显子跳跃突变的杜氏肌营养不良症 (DMD44) 患者能够产生抗肌萎缩蛋白。目前Del-zota已经完成了该适应症的I/II期临床试验。
阿肯色医科大学和阿肯色儿童医院儿科副教授Aravindhan Veerapandiyan医学博士表示:“Del-zota在多项指标上均显示出显著改善,包括显著增加肌营养不良蛋白的生成,以及仅服用三次后血清肌酸激酶水平显著降低至接近正常水平。如此短的时间内取得如此一致的疗效,加上良好的安全性和耐受性,凸显了Del-zota有望成为携带可进行44号外显子跳跃治疗的DMD患者的突破性疗法。”
如图所示,肌营养不良蛋白的产生量显著增加,比正常值高出约25%,肌营养不良蛋白总量恢复至正常值的58%;肌酸激酶水平降低至接近正常水平,与基线相比降低超过80%。
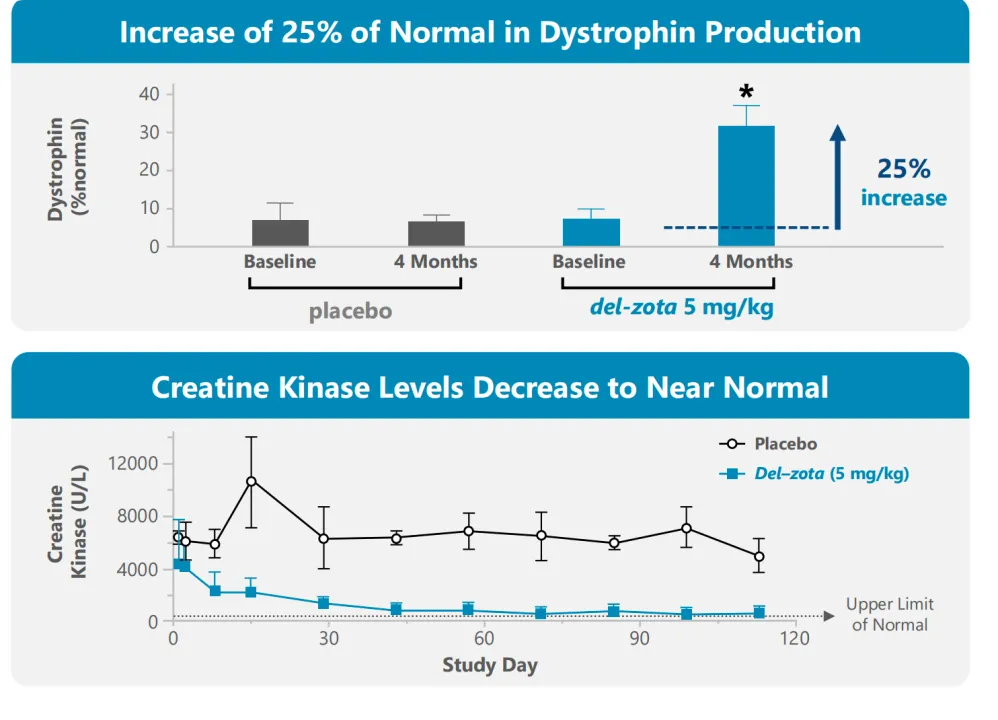
目前该药已经获得了FDA和EMA的孤儿药认证。
其次值得关注的药物是Del-desiran。这是一种用于治疗1型强直性肌营养不良症(DM1) 的管线,该适应症的全球患病率估计约为每2,100到3,000人中有1人。该药目前正进入到了三期临床阶段。DM1是由DMPK基因突变引起的,会导致产生异常长的信使RNA。超长的mRNA会在细胞中形成有毒的团块,造成肌肉损伤,进而引发肌强直(即肌肉在收缩后无法放松)以及其他疾病症状。
Del-desiran旨在通过降低DMPK相关的mRNA水平来解决DM1的根本原因。
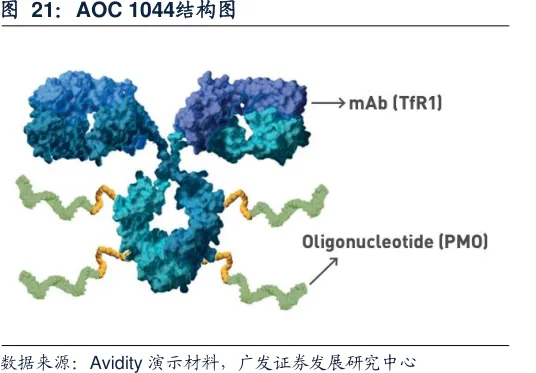
Del-desiran由一种与转铁蛋白受体1 (TfR1)结合的专有单克隆抗体与靶向DMPK mRNA的siRNA结合而成。在临床前研究中,del-desiran成功地将siRNA递送至肌肉细胞,从而在包括骨骼肌、心肌和平滑肌在内的多种肌肉中实现了持久、剂量依赖性的DMPK RNA降低。
从MARINA-OLE试验来看,患者获得了持久的疗效。
03
国内映射
AOC作为一个非常前沿的领域,国内大多数公司管线的进展仍然非常早期,相信在Avidity被收购后研发进度会有一个质的飞跃。
国内药物上,AOC药物的先驱是迦进生物,其先导产品CGB1001是针对1型强直性肌营养不良症(DM1)的抗体-SiRNA偶联药物,目前正在进行新药临床研究审批(IND)相关工作。该企业采用的是“定点偶联”工艺。
公司的ARC(Antibody-siRNA Conjugate)平台基于一款公司自主研发的高亲和力,高选择性TfR1专利抗体,对标Avidity Bio的13E4抗体,主要用于靶向肌肉递送小核酸药物。公司的管线CGB1001是一款ARC平台+ DMPK siRNA的抗体-siRNA偶联药物,用于治疗DM1,有机会成为国内首款针对DM1的疾病修饰疗法。此外公司还开发了CGB1003(ARC平台+ MSTN/ACVR2 siRNA用于增肌)及CGB1004(ARC平台 + DUX4 siRNA用于面肩肱型肌营养不良FSHD)等创新药管线,在国内都处于领先地位。
除此之外,2024年10月,盛世君联与成都先导宣布达成合作协议,共同推动AOC药物研发服务。成都先导在核酸药物研发领域有一定技术积累,此次合作旨在整合双方资源,加速AOC药物的研发进程。
结语:本次的收购对于Avidity是收获期,代表了它常年在一个垂直领域的深耕获得了MNC的认可。但之后AOC的临床和商业化之路道阻且长,能否闯过临床三期最后一关进入市场,就看未来Avidity的表现了。

 产业资讯
产业资讯
 药视声Medispace
药视声Medispace  2026-03-16
2026-03-16
 25
25
 产业资讯
产业资讯
 药时空
药时空  2026-03-16
2026-03-16
 21
21

 产业资讯
产业资讯
 MedTrend医趋势
MedTrend医趋势  2026-03-16
2026-03-16
 24
24