 产业资讯
产业资讯
 药智网
药智网  2025-08-28
2025-08-28
 1593
1593
创新药的周期像一条螺旋上升的曲线——政策、资本、技术、需求四股力量时而错位,时而共振。
过去几年,行业在估值低谷中完成了一次残酷的供给侧改革:管线同质化公司出清,资金与人才向真正具备“源头创新+国际化”能力的头部企业集中。
几年后的今天,当政策端暖风频吹、BD交易金额屡创新高、一级融资回暖、二级股价大涨之时,市场猛然发现,创新药板块已经重新站上风口。
这其中,君实生物凭借密集的全球里程碑事件与创新管线催化,再次成为市场情绪的锚点。在研发节奏、技术平台和国际化布局上,君实生物把每一步都踩在了节拍上。
近日,君实生物发布了2025年中期业绩报告,实现营收11.68亿元,同比增长49%;归母净亏损4.13亿元,较2024年同期下降36%,亏损大幅缩窄。
一直以来,君实生物凭借卓越的战略眼光,精准布局了较多优势管线,为其未来发展筑牢了根基。同时,在降本增效的大前提下君实生物继续加大研发投入,推动技术创新,为其竞争力的提升注入强劲动力。
01
“全链条+多领域”布局
细看君实生物的研发版图,已从单抗药物类型扩展为横跨单克隆抗体、双特异性及多特异性抗体、抗体药物偶联物(ADC)、融合蛋白、小分子抑制剂、核酸类药物与疫苗等多元技术形态的综合平台。目前,创新领域覆盖恶性肿瘤、自身免疫、代谢性疾病、神经系统及感染性疾病五大治疗方向,形成了“全链条+多领域”的完整布局。
截至公告日期,君实生物有4款药品(拓益®、君迈康®、民得维®以及君适达®)正在商业化中,近30个在研药物处于临床试验阶段;另有20余个候选分子处于临床前开发阶段,为公司未来3–5年的持续产出提供充足储备。
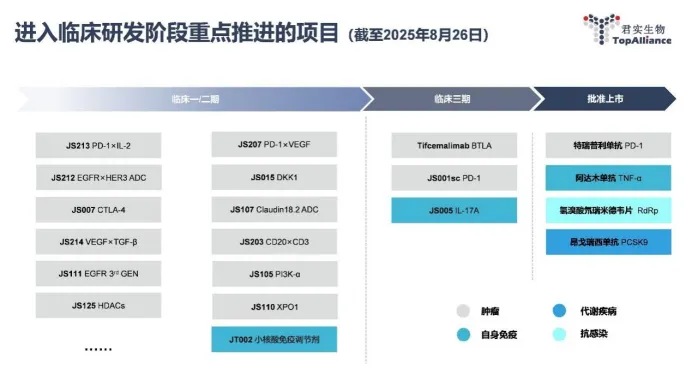
君实生物研发管线
图片来源:君实生物半年报
已上市产品方面,君实生物特瑞普利单抗(拓益®)已经从一个“国产首款PD-1”成长为真正的全球品种。截至报告期末,它在中国内地获批12项适应症,其中10项被纳入国家医保目录,是目前医保中唯一覆盖黑色素瘤、非小细胞肺癌围手术期、肾细胞癌和三阴性乳腺癌的PD-1单抗。
与此同时,君实生物通过“自营+合作”双轮驱动,把拓益推向全球:已在40个国家和地区获批上市,并向巴西、加拿大、马来西亚等12国递交上市申请;与Coherus、Hikma、Dr.Reddy’s、利奥制药等伙伴达成80余国的商业化合作,形成“中国智造,全球销售”的市场格局。2025年上半年,特瑞普利单抗先后在澳大利亚、新加坡、阿联酋和科威特获批,标志着其国际化进入收获期,也为后续双抗、ADC等管线出海打通了监管与渠道路径。
PCSK9单抗(君适达®,昂戈瑞西单抗)则是国内降脂市场中首个切中“他汀不耐受”这一人群的国产PCSK9单抗。2025年5月,两项新增适应症正式获批:杂合子型家族性高胆固醇血症(HeFH)及他汀类药物不耐受人群的高胆固醇血症。两项III期临床数据显示,150 mg Q2W皮下注射12周即可使患者LDL-C下降66.2%,且疗效持续至第52周,安全谱与安慰剂相当;研究结果连续发表于欧洲动脉粥样硬化学会官方杂志《动脉粥样硬化》(Atherosclerosis),强化了循证品牌力。预计2025年下半年开始放量,与特瑞普利单抗形成“肿瘤+慢病”双现金支柱。
从整体商业化布局看,君实生物已搭建“1+N”销售体系:通过肿瘤、心血管、自免、感染四条产品线的交叉部署了不同的销售渠道及方式,公司既能摊薄销售费用,又能提升单医院产出,为后续管线上市预留了成熟的商业化接口。
国际化方面,特瑞普利单抗已在全球40个国家和地区获得上市批准,实现“临床同步、法规同步、市场同步”的全球一体化推进。通过“现金流品种—注册梯队—重点孵化”的三级火箭模式,公司把已上市产品的商业化收益迅速转化为后续项目的研发燃料,确保创新引擎持续高转速运转。
02
组合舰队出击
站在公司“中期—后期”衔接的十字路口,JS207、JS212与JS213三条管线正把君实生物从“单品种驱动”带向“组合舰队”阶段。它们共同的关键词是“双靶”与“全球同步”,但各自切中的临床痛点、技术路径与时间节点又互为补充,构成一条清晰的迭代曲线。
>>JS207(PD-1/VEGF双抗)
——让“免疫+抗血管”组合成为王炸。JS207是具有IgG4κ亚型的IgG-VHH四价结构的新型双特性抗体,由全长抗PD-1 IgG抗体(即特瑞普利单抗)和靶向VEGFA的重链可变区(VHH)组成,VEGFA单域抗体通过柔性连接子融合到铰链区。
临床前数据显示,在MC38结肠癌模型中4.5 mg/kg组的肿瘤抑制率(TGI)达到84.4%,优于PD-1单药或PD-1+VEGF双药联合。II期正在非小细胞肺癌、结直肠癌、三阴乳腺癌与肝癌四大瘤种中开展与化疗、ADC等不同方案联合研究,截至今年8月22日,II期临床研究共入组172名受试者,临床提速明显。此前,在I期临床研究阶段,JS207共入组近100名受试者。
>>JS212(EGFR/HER3双特异ADC)
——把耐药人群重新拉回治疗窗。JS212有望实现“双靶点+细胞毒”的三重杀伤。与单一靶点ADC药物相比,JS212能够通过与EGFR或HER3结合发挥肿瘤抑制作用,与同类药物相比具有独特的payload和linker,有望对更广泛的肿瘤有效,同时有望克服耐药性问题。目前,JS212正在I期研究中验证其在晚期实体瘤中的安全性与初步疗效。
>>JS213(PD-1/IL-2融合蛋白)
——把“冷肿瘤”烧成“热战场”。IL-2曾因毒性大而束之高阁,而JS213通过PD-1的靶向作用,更有效地将IL-2引导至PD-1高表达的T细胞,激活那些处于抑制状态的耗竭性T细胞,恢复其抗肿瘤功能,同时通过IL-2信号增强这些T细胞的增殖和效应功能,提高了IL-2的局部浓度和活性,减少其在外周其他部位的不必要激活,减少系统性毒性。此外,JS213的平均半衰期约4.5天,通过延长给药间隔进一步降低毒性。海外FIH I期已完成16例剂量递增(0.3–1 mg/kg Q2W),2例PR(胸腺癌、胸腺瘤各1例)、6例SD,安全性以1–2级皮疹、甲减为主;国内I期也已开组,聚焦在非小细胞肺癌、黑色素瘤、结直肠癌等瘤种。
综合来看,JS207解决的是“联合用药复杂”的问题,JS212解决的是“靶向耐药”的问题,JS213则瞄准“免疫不应答”的空白。三条管线在时间上呈阶梯递进,在空间上共享全球多中心体系,一旦形成梯队上市,将让君实生物真正走向“多引擎”时代。
03
向星辰大海启航
君实生物的其他重点管线更像一座“预装多弹头的弹仓”,通过差异化的靶点选择与多技术平台并行,把未来三到五年的潜在爆款提前锁定。
首先,CD20×CD3双抗JS203瞄准血液瘤未被满足的复发/难治需求。该分子利用双特异桥接机制,通过对淋巴瘤细胞(结合CD20)和T细胞(结合CD3)的联结和活化,有效促进T细胞杀伤淋巴瘤细胞。I/II期数据显示,经利妥昔单抗预处理后30 mg阶梯给药组的弥漫大B细胞淋巴瘤(DLBCL)ORR达到80%,完全缓解率40%。公司计划2026年启动关键注册研究,有望为恶性淋巴瘤患者提供一种潜在的治疗新选择。
其次,DKK1单抗JS015在实体瘤调控上另辟蹊径。DKK1通过调节Wnt和CKAP4-PI3K/Akt通路、诱导免疫抑制和血管生成促进肿瘤发生发展。JS015能以高亲和力结合DKK1,通过阻断上述路径发挥肿瘤抑制作用。2025年AACR上首次公布的一项Ib/II期与两项研究者发起研究(IIT)汇总数据显示:JS015联合贝伐珠单抗和化疗用于二线结直肠癌ORR 31.6%,贝伐未经治的ORR达80%,一线联合方案ORR高达100%;胃癌一线三药联合ORR 66.7%。目前这几项研究正在继续随访中。
Claudin18.2 ADC JS107则把“精准制导”与“旁观者杀伤”结合,使用vc-MMAE的连接子-毒素,对抗胃肠道肿瘤高异质性。2025年AACR首次公布了I期剂量扩展和1线胃癌数据,1L联合特瑞普利和化疗治疗晚期胃/胃食管结合部腺癌ORR达81%。公司预计2025年内启动III期研究。
整体来看,上述重点管线以“差异化靶点+多技术平台+快速迭代”为核心逻辑:血液瘤、实体瘤并重,抗体、ADC、小分子、融合蛋白交叉互补。
随着资金与临床资源的持续注入,这些管线有望在未来三到五年陆续进入后期开发,为君实生物下一轮的业绩爆发提供充足弹药。
04
结语
回望君实生物的管线版图,一条清晰的“成长螺旋”已经成形:已上市品种用现金流为创新持续输血,重点管线则加速冲刺,将差异化靶点与技术平台提前锁位。资本、政策、技术与临床需求四股力量,如今终于在君实的节奏里同频共振。
未来三到五年,随着这些管线梯队持续兑现,君实有望完成从“星星之火”到“矩阵舰队”的蝶变。

 产业资讯
产业资讯
 医药魔方
医药魔方  2026-03-14
2026-03-14
 107
107
 产业资讯
产业资讯
 会会药咖
会会药咖  2026-03-14
2026-03-14
 107
107

 产业资讯
产业资讯
 氨基观察
氨基观察  2026-03-14
2026-03-14
 108
108