 产业资讯
产业资讯
 医药魔方
医药魔方  2025-08-29
2025-08-29
 862
862
2025年,中国创新药在经历了三年低谷后,似乎又行了。
年初至今,多重利好政策催化下,港股生物医药股普遍迎来了暴涨。在此过程中,一大逻辑主线是中国创新药在历经十年发展后迎来了拐点,开始从本土研发、商业化走向全球化,以BD出海为核心引擎,拉动了生物医药板块持续向好。
值得一提的是,当下的BD浪潮中,已有少数中国原创新药在美国等海外市场实现亮眼的销售成绩,成为这波浪潮中的领军者,呋喹替尼便是其中之一。
而有赖于其显露的创新价值,呋喹替尼更是于本月26日斩获“2024年度上海市科学技术奖”中的“上海市科技进步奖”一等奖,标志着创新药企同样能成为推动科学研究突破的核心力量。
对此,和黄医药执行副总裁崔昳昤认为,2023年新修订的《上海市科学技术奖励规定实施细则》对科学奖励鼓励创新转化的导向给与了进一步的明确,从而更激发了企业参与科技创新的信心。
可以说,呋喹替尼的创新价值不言而喻。但作为上海首个成功叩开美国、欧盟、日本三大全球标杆市场,以及一度刷新小分子BD出海记录的原创新药,它之于和黄医药的意义远不止于获奖和创收——其12年的研发历程,为和黄医药沉淀了宝贵的经验,这都将为后续管线2.0的全球开发筑牢根基,也为其业绩和股价攀升铺垫好了道路。
20年前,如何做出全球新?
单看药物本身,2025年上半年,呋喹替尼以2.058亿美元的全球销售额彰显实力,其中海外市场同比增长25%。这一表现,不仅印证了这款药物的市场穿透力,更让和黄医药稳稳立身于Biopharma阵营。
而当不少创新药企还在“创新如何做”“国际化道路又该怎么走”的迷思中摸索时,相较于直观的数字,呋喹替尼从实验室到全球市场的开发历程,才真正隐藏着破题的答案,这恰是和黄医药一路成长的核心密码。
呋喹替尼诞生于一个仿制药的时代,在近日的一场媒体对话里,和黄医药高级副总裁范颂华就回忆称:“2006年之前,国内的肿瘤创新药或者靶向药可以说非常少,中国创新靶向药物完全依赖国外引进,上市时间要比国外市场滞后4-5年。”
即便是十年之后,呋喹替尼在国内上市的2018年,国产创新药的发展也才刚开始不久。医药魔方数据显示,2016年在中国首次获批的国产新药仅有4款,进口新药2款;2017年则是进口新药的天下,共有41款,远不是今日模样。
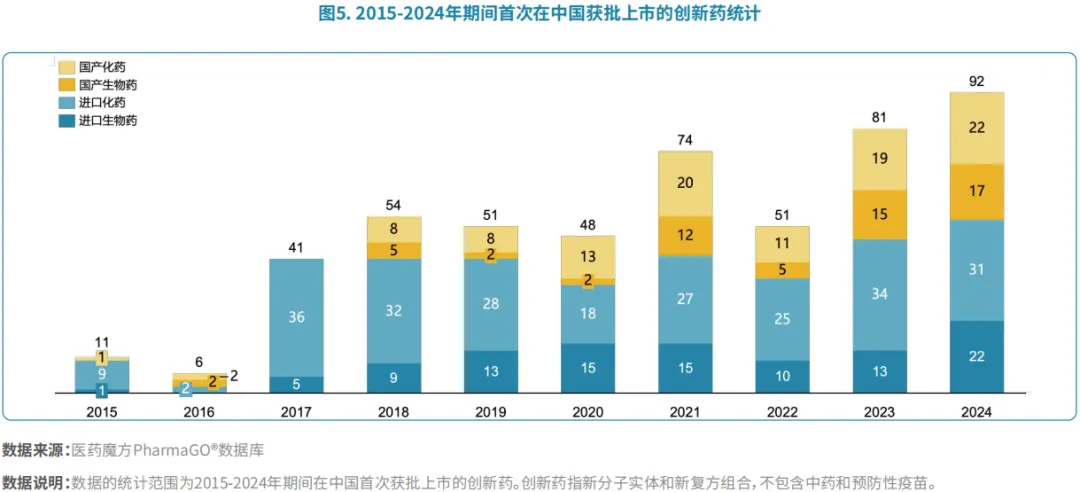
来源:全球视野下的中国创新药产业:十年回顾与展望
在那个年代,做创新药是需要初心和魄力的。彼时,罗氏一款针对肠癌的贝伐珠单抗注射液,启发了和黄医药的创新之路,成为其踏足原研药领域的起点。“我们想做出一款口服药,能替代静脉注射,实实在在帮到患者。”范颂华的话道出了和黄医药最初的信念。
2005年,和黄医药首席科学官苏慰国在一家咖啡馆里,在“信手拈来”的一张餐巾纸上画下了一串分子式,其中一个就是呋喹替尼。尽管故事的开端有些戏剧性,但后续的开发却是实打实的硬仗。
选择打造一款Best-in-Class(同类最佳),用“巧劲”率先打开口子虽然更为务实,但稳扎稳打的策略并不意味着和黄医药降低标准。相反,“在体系构建的初期,我们就确立了清晰的国际化战略。”苏慰国如此说道,比如在药物开发上,搭建与国际接轨的临床前筛选平台,再比如搭建国际化团队。
2011年,呋喹替尼首次在人体中使用,开始迎接更大的挑战——临床开发。和黄医药高级副总裁戴广袖坦言,当时要开发一款媲美贝伐珠单抗的原创新药,面临两大挑战是资金和不确定性。换言之便是高风险高投入,这是其它行业少有的特点。
她回忆道:“2017年三期结果揭盲前,全公司都非常紧张,没人敢拍胸脯保证结果一定理想。”即便到了2022年,该药在美国的三期临床结果即将公布时,和黄医药依旧不敢打包票。“这种不确定性,是我们创新药企永远要面对的问题。”她如此说道。
与此同时,呋喹替尼开发初期,中国投资创新药的资本寥寥无几,这意味着彼时的和黄医药在资金方面也承受着压力。
即便如此,和黄医药依旧保持前瞻视野和恪守创新标准。苏慰国曾如此总结呋喹替尼的成功,那就是“要按照要求脚踏实地地布局,该投入的地方要舍得投入”。
最鲜明的例证是,早在2013年,和黄医药就在国内前瞻性设计了一个随机对照、剂量优化的临床方案,来确定呋喹替尼的临床推荐剂量,早于FDA推出“随机对照试验剂量优化方法”指导原则9年。与此同时,和黄医药敏锐洞悉了FDA的新要求,提前开展了呋喹替尼全球多中心临床研究(MRCT)。
正是这份最初的坚守和先行探索,为呋喹替尼后来的出海之路埋下伏笔,使其成为国内最早一批踏上美国市场的原创新药。
与时代共振,和黄加速奔跑
放眼今日,中国创新药的集体崛起,离不开时代环境的托举。而呋喹替尼的成长轨迹,亦始终与时代同频共振。
无论是借力国家重大新药创制专项的政策东风,再到后来借势MAH制度试点加速上市,还是在国产新药掀起出海浪潮时叩开国际市场大门,呋喹替尼的成功可以说是时代机遇与企业韧性的双向成就。
2015年起至今,中国迎来了创新药发展的黄金期,根据医药魔方InvestGo数据库的统计,期间中国创新药从一二级市场筹集到的资金总额达到1.23万亿元。重金投入,政策扶持,让中国成功诞生了一批原创新药。
2023年年底,3款国产创新药相继在美国上市,成为中国医药创新的标志性突破。而早就布局全球多中心临床试验,瞄准临床痛点的呋喹替尼,也跻身其中,成为第二个登陆美国市场的本土小分子创新药。
围绕呋喹替尼在海外的商业化,和黄医药不是没有想过自建美国商业化团队,但这样的投入在当前的国际局势下可能并非明智之举。也因此,在BD浪潮掀起之时,务实的和黄医药基于自身情况,选择了携手武田打开国际市场,打造百亿级品种。
从2025年上半年的销售数据来看,呋喹替尼已在海外市场快速放量,在超过30个国家获批上市,其中2025年新增了10多个市场。在国内市场,市占率第一的呋喹替尼即便销售额有所下滑,但韧性仍在——苏慰国就透露基于市场策略的调整,二季度的下半段以及7月份已看到呋喹替尼在肠癌市场的快速反弹。
于市场而言,和黄医药历来是基本盘扎实的代表。成长至今日,它并非只有呋喹替尼挑大梁。过去20年里,赛沃替尼、索凡替尼相继诞生,与呋喹替尼共同构成“替尼三将”的商业化基本盘。
不过,竞品冲击与单品天花板是“替尼三将”眼下有待破解的难题。和黄医药拿出的策略是扩展适应症,以及联合用药来破局。
近期来看,呋喹替尼将在中国市场获批用于二线治疗子宫内膜癌,和黄医药正备战今年的医保目录谈判。同时,武田也为其定下2025财年海外市场增长20%以上的目标。
赛沃替尼与奥希替尼的联合疗法则刚获国家药监局批准上市。索乐匹尼布的中国新药上市申请则已获国家药监局受理,正在审批中。医药魔方NextPharma数据库显示,该药的开发进度处于中国第一,全球第二。如此种种,无疑都将持续拓展和黄医药的价值空间。
眼下,和黄医药已陆续剥离中药资产,全面押注创新。显然,尽管短期面临阵痛,但和黄医药还在加速奔跑。
进场ADC打造管线2.0,拼什么?
而它的新一站,正是当下如火如荼的ADC赛道。
这不免让人好奇,ADC赛道并不乏开发者,刚入局的和黄医药有何底气?何况无论是前述已获批产品,还是后续在研的靶向FGFR 1/2/3的抑制剂、IDH1/2双重抑制剂等,外界对它的印象始终是深耕小分子领域。
在此前的对话中,和黄医药给出了它的答案。“我们一直在不断根据行业变化,调整我们的方向,精准押注。”崔昳昤如此说道。它的新蓝图,便是“借助之前小分子领域的优势和特长,进军大分子领域,开发具有高度差异化的创新产品。”此话恰恰点明了它搅动ADC赛道风云的玄机所在。
因ADC药物的“工程性”特质,医药魔方数据显示,中国在活跃ADC管线数量上位于全球前列,贡献了全球57%的ADC产品。尽管在研管线众多,但市场仍存在机会——国内市场上,84%仍处于早期研发阶段(I期-II期),只有3款国产ADC产品获批上市。
围绕双抗/多抗ADC、多载荷ADC等创新形式的开发,正成为行业差异化竞争的突破口。
细究和黄医药的ADC布局,过去三年里,其自主研发了新一代抗体靶向偶联药物(ATTC)技术平台。该平台的一大亮点是联动小分子管线资源,使用靶向小分子取代传统以毒素为基础的有效载荷,而非另起炉灶。这一做法的好处是能够充分发挥现有资源的优势,同时突破天花板。
而从技术上来看,ATTC平台的另一个优势在于可进一步优化小分子药物的效力,避免因狭窄的治疗窗口带来的限制。
通过降低对肿瘤以外组织毒性或脱靶毒性,和黄医药的平台旨在将高效浓度的小分子抑制剂通过抗体引导精准送达目标组织。这有可能在大量有着未被满足需求的适应症中发挥疗效,并使长期用药成为可能。更广泛而言,ATTC平台有潜力整合高分子量的药物作为有效载荷,例如蛋白降解靶向嵌合体(PROTAC)和蛋白互作抑制剂(PPI)。
另外,不同于传统的ADC,全新的ATTC平台还具有与化疗或其他靶向药物联合用药的潜力,这使得这一新的疗法有潜力在更早的治疗线中应用,面向更广阔的患者群体。
值得一提的是,当下ADC出海浪潮中,和黄医药的ATTC平台已显露出孕育更多BD 机会的潜力。依托该ATTC平台搭建的管线2.0,其临床开发策略直指全球化,并在中美同步开展临床——这与管线1.0时代的开发路径形成了鲜明差异。
“得益于此前开发呋喹替尼等药物所沉淀的开发经验。现在我们已经知道如何去开展全球多中心临床。”范颂华说。事实上,全球多中心临床试验是创新药出海的重要门槛之一,往往意味着人力、物力和财力的大量投入,并非所有创新药企都能做到。
而中美同步申报的情况下,范颂华表示:“未来在I期临床研究中,我们就会纳入中国以及中国以外的人群,这有利于开拓更广阔的全球市场。”
可以说,前期积累的全球开发经验、打造的国际化团队以及资金投入,都成为了有力推手,让和黄医药在开发管线2.0时更显从容老练。它已预计,到2025年年底将有1-2个新分子中美同步申报,进入临床开发。
眼下,据半年报披露,和黄医药上海工厂已完成首款ATTC候选药物的生产,并已完成生产全球临床供药的首批药品。
创新齿轮加速下,和黄医药已在逆风上扬的路上,市场对它的认知,也有望在此过程中被重塑。

 产业资讯
产业资讯
 医药魔方
医药魔方  2026-03-14
2026-03-14
 106
106
 产业资讯
产业资讯
 会会药咖
会会药咖  2026-03-14
2026-03-14
 106
106

 产业资讯
产业资讯
 氨基观察
氨基观察  2026-03-14
2026-03-14
 107
107