 产业资讯
产业资讯
 医药魔方
医药魔方  2025-08-30
2025-08-30
 917
917
随着各大药企2025年半年报的发布,BTK抑制剂赛道各玩家销售成绩单也开始刷新。
第一代BTK抑制剂强生/艾伯维的伊布替尼2025年上半年销售额不足30亿美元,同比下滑9%。
与此相对的是新一代BTK抑制剂各玩家的增长:百济神州的泽布替尼2025年上半年销售额达17.42亿美元,同比增长54.7%;阿斯利康的阿可替尼2025年上半年销售额16.34亿美元,同比增长9%;礼来的匹妥布替尼2025年上半年销售额为2.15亿美元,同比增长51.4%;诺诚健华的奥布替尼2025年上半年销售额达6.37亿元(约0.89亿美元),同比增长52.84%。
目前全球范围内共有6款BTK抑制剂获批上市,不过仅有伊布替尼和泽布替尼上榜了2025上半年全球药品销售额TOP50榜单。伊布替尼从2024全年度的22位降至今年上半年的26位;泽布替尼则从2024全年度的第70名越迁至今年上半年的第50位。
泽布替尼作为百济神州的第一个“重磅炸弹”药物,自2019年11月在美国上市以来,销售额持续增长:2022年其全球销售额达38.29亿元,同比增长159%;2023年,泽布替尼全球销售额就已突破10亿美元大关,达13亿美元,快速跻身“重磅炸弹”药物行列。2024年其全球销售额达26.44亿美元,占百济神州产品收入的近70%。
从上市3年即成为“重磅炸弹”药品到上榜全球畅销药TOP50榜单,泽布替尼在商业化上的成功如同其在研发上取得的成就一样值得创新药企参考。在泽布替尼上市5周年之际,我们试图对其商业化成功的原因进行解析。
长生存期打造差异化优势
时间回到2022年12月14日,这一天,百济神州在第64届美国血液学会(ASH)年会上公布了全球3期ALPINE试验的最终分析数据,结果显示泽布替尼在复发/难治性(R/R)慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者中,无进展生存期(PFS)和总缓解率(ORR)均优于伊布替尼。
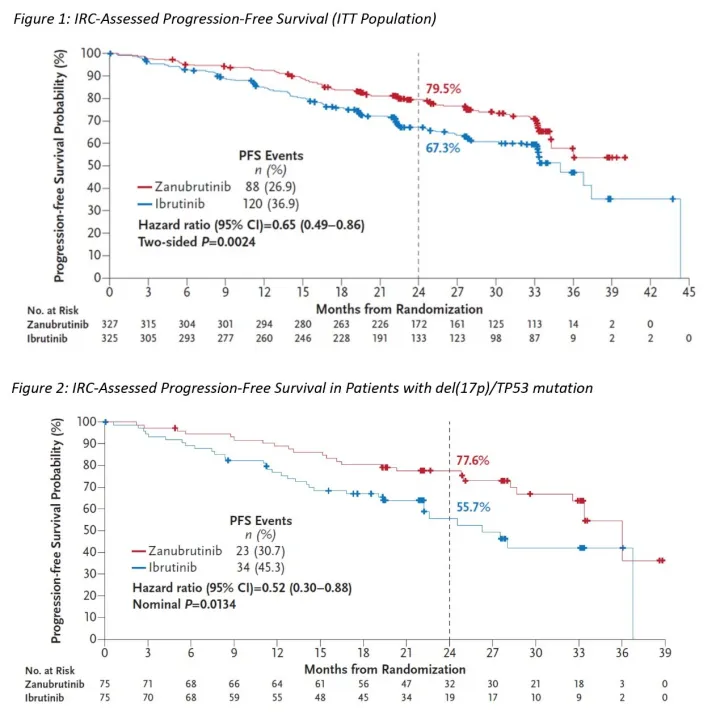
图片来源:2022年ASH年会摘要#LBA-6
在此之前,阿可替尼的ELEVATE-RR研究是CLL/SLL领域首个BTK抑制剂“头对头”临床试验。结果显示,阿可替尼对于既往至少接受过一次治疗的高危CLL患者在改善PFS方面非劣效于伊布替尼。在安全性方面,阿可替尼的房颤/房扑发生率、不良事件导致的停药和死亡均低于伊布替尼。
今年7月,礼来公布了BRUIN CLL-314研究的积极顶线结果。在这又一个与伊布替尼“头对头”对比研究中,匹妥布替尼对于CLL/SLL患者治疗在ORR方面非劣于后者,PFS在本次分析中尚未成熟。
可以看到的是,同样是与伊布替尼的“头对头”研究,阿可替尼提高了安全性,但并未取得PFS获益;匹妥布替尼取得了ORR获益,但同样在PFS获益上还未完全清晰;而泽布替尼则成为全球首个且目前唯一在CLL/SLL“头对头”研究中在PFS与ORR上均取得优效性的新一代BTK抑制剂。
更值得注意的是,泽布替尼在PFS上正持续不断创造出更优异的成绩。
ALPINE研究显示,泽布替尼治疗R/R CLL患者的PFS获益和心脏安全性显著优于一代BTK抑制剂,36个月PFS率分别为泽布替尼67.4%VS伊布替尼56.3%。
在今年的ASCO会议上,SEQUOIA研究C组5年随访数据显示,泽布替尼治疗初治伴17p缺失的CLL/SLL患者中显示出持久的疗效,5年PFS率达到72.2%。
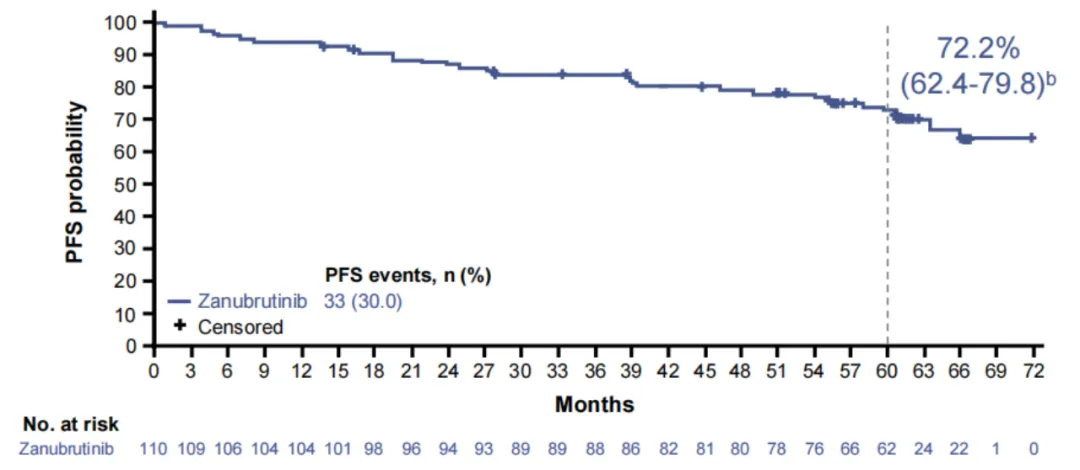
图片来源:2025 ASCO摘要 #7011
长期随访数据显示,泽布替尼针对初治不伴高危因素的CLL患者的5年PFS率高达76%。这意味着,患者获得长生存期且不复发的概率很大,或可提高患者的长期生活质量。
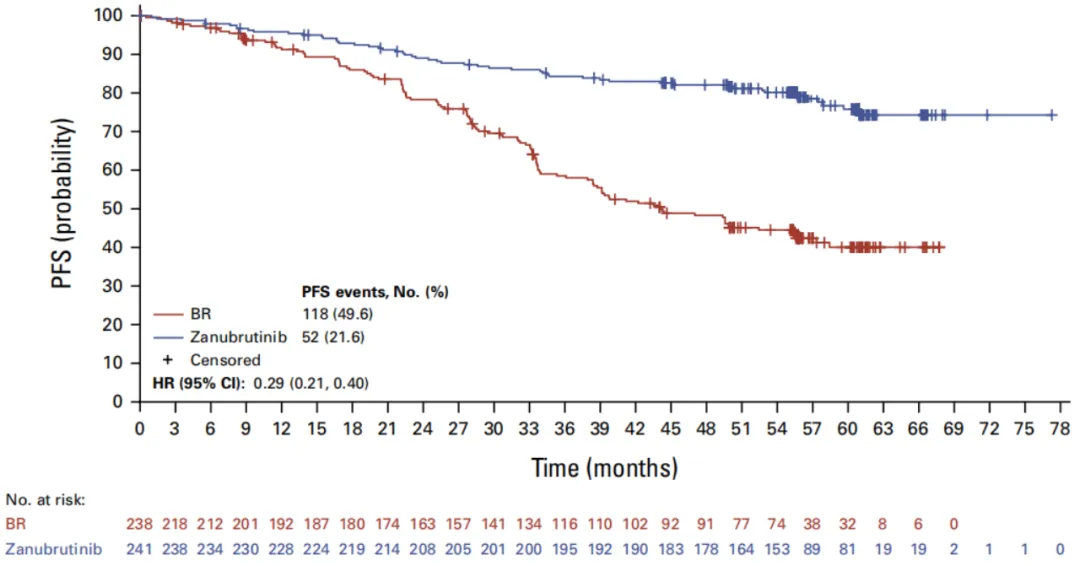
图片来源:2025 ASCO 摘要 #7011
长生存期获益既是泽布替尼突出BTK抑制剂重围的“关键武器”,更是对于患者而言至关重要的临床需求。通过更好、更全面地满足临床需求,是一款创新药从诞生到销售大爆的必经之路。
基于头对头研究及长随访数据,泽布替尼获CSCO和NCCN指南优先推荐,作为基石药物推动淋巴瘤进入“无化疗”和“有限周期治疗”时代。
在差异化优势——长生存期加持的同时,百济神州正源源不断地拓展泽布替尼适应症范围。
截止目前,泽布替尼在中国已获批针对治疗CLL/SLL、华氏巨球蛋白血症(WM)、R/R套细胞淋巴瘤(MCL)、R/R滤泡性淋巴瘤(FL)4项适应症,且4项适应症均已被纳入国家医保目录。泽布替尼也成为在中国市场获批和纳入医保适应症最多的BTK抑制剂。
进入医保是泽布替尼在中国市场提高可及性的重要一步。更为关键的是,泽布替尼在进入医保后不断让利于患者。经过多次降价后,泽布替尼在中国市场的价格约是在美国市场定价的1/10。
而在欧美市场,百济神州则从便利性角度出发,提供更贴心的治疗选择。今年上半年,泽布替尼新的薄膜包衣片剂剂型先后在美国和欧盟获得批准,用于所有当地已获批适应症。对于患者而言,片剂剂型简化了用药方式,让用药的便利性和依从性可进一步获得提升;对于医生而言,片剂剂型可一分为二,更方便完善治疗方案。
从患者和医生角度出发去满足临床需求,从需求点差异化角度出发去填补市场空缺,或许是泽布替尼成功的最底层逻辑。
巩固全球地位
凭借着在疗效和安全性上同类最优的产品硬实力,泽布替尼在BTK抑制剂市场的领先地位被持续巩固。
2025年8月,百济神州发布2025年第二季度报告:实现GAAP净利润为9400万美元,较去年同期亏损相比增加2.15亿美元。至此,百济神州迈入“盈利元年”。
让百济神州收入大幅增长乃至实现扭亏为盈的“头号功臣”非泽布替尼莫属。2025年第二季度,百济神州产品收入为13亿美元,同比增长42%。其中,泽布替尼全球收入达9.5亿美元,占收入超73%。
百济神州也在报告中表示,收入的增长主要得益于泽布替尼销售额增长。而泽布替尼在全球化上的成功更是其销售额大增的主要原因。
在美国市场,泽布替尼2025年第二季度销售额为6.84亿美元,同比增长43%,占到泽布替尼全球收入的72%;在欧洲市场,泽布替尼2025年第二季度销售额为1.50亿美元,同比增长85%。这主要得益于在所有欧洲主要市场的市场份额提升,包括德国、意大利、西班牙、法国和英国。
全球化之路对于任何一款创新药来说都是不容易的,百济神州更是早在泽布替尼立项之初就已开始布局全球化,才有了泽布替尼的现在。
而广泛的适应症且所有适应症领域强劲的需求增长,以及净定价带来的适度利好,让本就拥有差异化优势和同类最佳临床特征的泽布替尼在BTK抑制剂赛道继续保持市场份额的领先地位。
在2024第四季度首次以8.28亿美元的销售额超过了阿可替尼的8.08亿美元后,泽布替尼乘胜追击,进一步扩大领先优势:两款新型BTK抑制剂销售额差距也从2025年第一季度的3000万美元拉开至第二季度的7800万美元。
如今,泽布替尼已在全球75个市场获批,今年第二季度在5个市场新增纳入或扩大报销范围。随着BTK抑制剂市场的持续扩大和新适应症的拓展,泽布替尼未来是否会成为BTK抑制剂赛道“新晋药王”,值得期待。
基石产品引领血液肿瘤领域
泽布替尼作为全球畅销药之一,是百济神州产品组合中的“定海神针”,反映着百济神州在血液肿瘤领域的表现。而百济神州在血液肿瘤领域布局的一举一动也备受行业关注。
具体而言,在血液肿瘤领域百济神州找准了锚点:聚焦细分市场大、增长快的CLL疾病市场并选择持续深耕。从其2025年第二季度业绩报告中可以看出,在血液肿瘤领域有两款在研产品颇受百济神州重视:索托克拉(BCL2抑制剂)和BGB-16673(BTK CDAC)。
以BTK抑制剂泽布替尼为基石产品,加上BCL-2抑制剂索托克拉和BTK CDAC产品BGB-16673,百济神州也因此成为了唯一一家在3个CLL基础作用机制中均拥有潜在BIC产品的药企。
索托克拉是新一代BCL2抑制剂,旨在阻断可帮助肿瘤细胞存活的BCL2蛋白。研究表明,BCL2抑制剂能特异性地结合并抑制BCL-2蛋白,重新激活癌细胞的凋亡程序,诱导癌细胞死亡,或将为患者带来更多创新选择。
索托克拉用于治疗MCL和CLL的2期试验预计进行数据读出,并有望提交全球加速上市申请,目前用于治疗CLL/SLL和MCL的上市申请在中国已获受理,并被纳入优先审评;索托克拉用于初治CLL患者的全球3期研究也已完成患者入组,联合抗CD20抗体用于治疗R/R CLL的全球3期试验完成首例受试者入组。
BGB-16673是一种口服、靶向BTK的嵌合式降解激活化合物,也是一款在研、潜在同类首创BTK降解剂,旨在解决B细胞恶性肿瘤患者耐药性问题并改善治疗效果。
目前,BGB-16673获得欧洲药品管理局授予的优先药物(PRIME)认定,用于治疗既往接受过BTK抑制剂治疗的华氏巨球蛋白血症(WM)患者;用于治疗R/R CLL的全球3期BGB-16673-302试验已完成首例受试者入组;用于治疗R/R CLL的中国3期BGB-16673-303试验已完成首例受试者入组;用于治疗R/R WM的潜在注册性2期研究已启动患者入组。
据百济神州透露,预计将于今年下半年启动BGB-16673对比礼来的匹妥布替尼用于治疗R/R CLL患者的3期头对头试验。
泽布替尼引航,索托克拉、BGB-16673续力,百济神州在筑起产品护城河的同时,或将构建出血液肿瘤领域治疗新生态。

 产业资讯
产业资讯
 医药魔方
医药魔方  2026-03-14
2026-03-14
 104
104
 产业资讯
产业资讯
 会会药咖
会会药咖  2026-03-14
2026-03-14
 103
103

 产业资讯
产业资讯
 氨基观察
氨基观察  2026-03-14
2026-03-14
 105
105