 产业资讯
产业资讯
 同写意
同写意  2025-09-17
2025-09-17
 3013
3013
若论真正推动中国创新药站上国际舞台的药物,ADC和双抗无疑是其中的核心力量。
从2021年荣昌生物维迪西妥单抗以26亿美元成功出海,到2022年科伦博泰与默沙东达成超百亿美元的ADC大单,再到康方生物依沃西单抗在头对头研究中击败K药,中国创新药凭借ADC和双抗,吸引全球巨头纷纷前来“扫货”。仅2025年上半年,ADC和双抗就占据中国创新药BD交易总金额的近60%,其中ADC交易额达172.72亿美元,双抗也突破114亿美元。
然而,随着赛道从蓝海转向红海,靶点同质化、研发瓶颈等问题逐渐显现,部分企业甚至被迫砍掉ADC管线。在这一背景下,双抗ADC作为ADC的升级形态,融合了双抗与ADC的双重优势,正成为肿瘤治疗领域最具竞争力的新方向。其不仅有望接棒成为中国创新药BD交易新热点,更可能再次引爆中国创新药。
TONACEA
01
“魔法子弹”升级版
ADC药物是通过抗体特异性识别肿瘤表面抗原,在癌细胞内释放强效细胞毒素,从而达到高效低毒的治疗效果,被誉为肿瘤治疗的“魔法子弹”。
然而,随着临床应用深入,传统ADC的局限逐渐暴露:单一靶点识别难以应对肿瘤的复杂性。若目标抗原丢失或表达不均,就容易出现靶向失效,导致药物无法精准定位或杀伤不足,进而引发耐药;此外,受限于肿瘤微环境的免疫抑制状态,传统ADC主要依靠直接杀伤作用,难以有效激活机体免疫响应,治疗效果面临瓶颈。
而双抗ADC(BsADC)作为ADC技术的进阶形态,延续了“抗体-连接子-毒素”的基本架构,关键突破在于将传统单抗“导航”升级为双特异性抗体,它能同时结合两个不同靶点,如同为“子弹”加装双重制导系统,显著提升识别精准度并拓展应用场景。
根据靶向策略的不同,双抗ADC主要分为两类:一类是针对同一抗原上不同表位的双表位ADC,可增强受体聚集与内吞效率;另一类为同时靶向两个不同抗原的双靶点ADC,能够协同抑制多个信号通路,实现更高效的抗肿瘤效应。
具体而言,双抗ADC通过其双特异性抗体同时识别两个不同靶点,显著增强了药物对肿瘤细胞的选择性和结合能力。例如,部分HER2阳性乳腺癌细胞可能丢失HER2抗原,导致传统HER2 ADC无法识别,而双抗ADC若同时靶向HER2与另一个在肿瘤细胞上稳定表达的抗原(如CD46),即便部分细胞丢失HER2,仍能通过 CD46实现精准结合,从而有效克服单靶点ADC常见的抗原逃逸所致耐药问题。
同时,双靶点协同结合可诱导更强的受体聚集效应,加速药物内吞,提升毒素在胞内的释放效率,增强杀伤效果。研究表明,双抗ADC的内吞速率可达单抗ADC的2-3倍,显著提升毒素进入肿瘤细胞的效率。
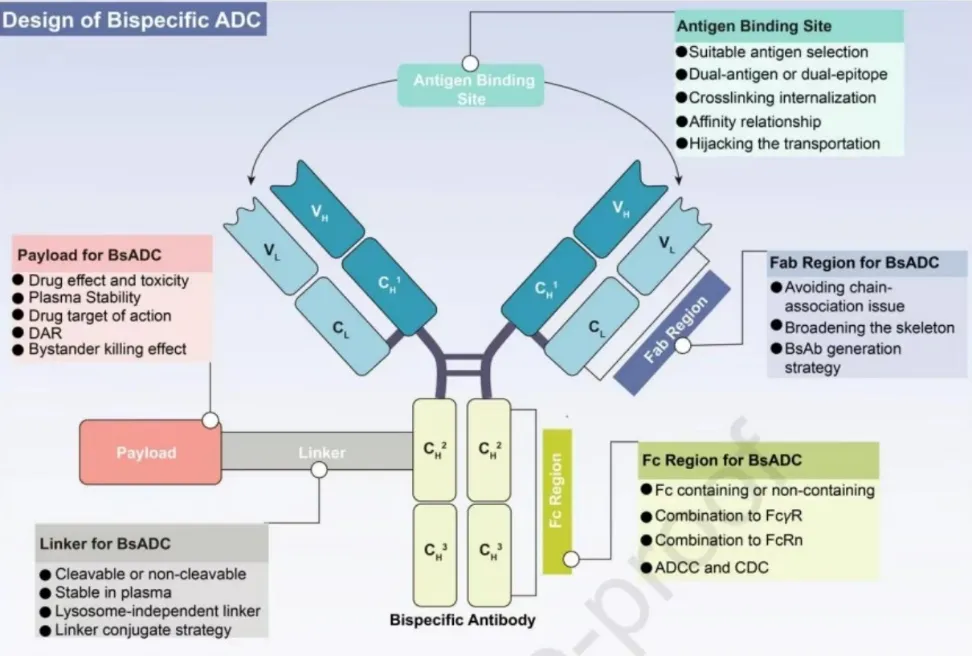
双抗ADC机制 图片来源:参考资料1
与传统单抗ADC相比,双抗ADC的另一重要优势在于其协同杀伤效应。除了靶向肿瘤细胞表面两种抗原,它还可被设计为同时结合肿瘤细胞与免疫细胞(如T细胞表面的CD3),从而不仅直接杀伤肿瘤,还可募集并激活免疫细胞,重塑肿瘤微环境,实现免疫调节与化学杀伤的协同效应。
此外,双抗ADC通过提高肿瘤特异性结合强度,有助于减少脱靶毒性及在正常组织中的非特异性分布,从而有望拓宽治疗窗口,降低系统暴露带来的不良反应。目前,双抗ADC技术已在多种实体瘤和血液肿瘤模型中展现出令人鼓舞的治疗潜力,并逐步推动临床转化,成为各大创新药企争相布局的方向。
TONACEA
02
中国药企冲击第一梯队
随着双抗ADC的技术路线日益明朗,全球药企竞相投入研发,其中中国企业更是跻身全球双抗 ADC 研发的第一梯队。不完全统计,目前全球进入临床阶段的双抗ADC有19款,其中只有3款处于临床III期,全部来自中国企业,分别是百利天恒BL-B01D1、康宁杰瑞JSKN-003和正大天晴TQB2102。
百利天恒的BL-B01D1是全球首款进入III期临床的 EGFR/HER3 双抗ADC。其III期鼻咽癌研究已达成主要终点,并在非小细胞肺癌、小细胞肺癌等10项III期临床中同步推进。该药物早期便凭借I期数据与BMS达成84亿美元的出海交易,创下中国单药License-out金额纪录。在2025年世界肺癌大会(WCLC)上,BL-B01D1联合奥希替尼一线治疗EGFR突变非小细胞肺癌的最新临床结果显示,在接受2.5mg/kg剂量的40名患者中,ORR达到了惊人的100%,为后续商业化奠定基础。
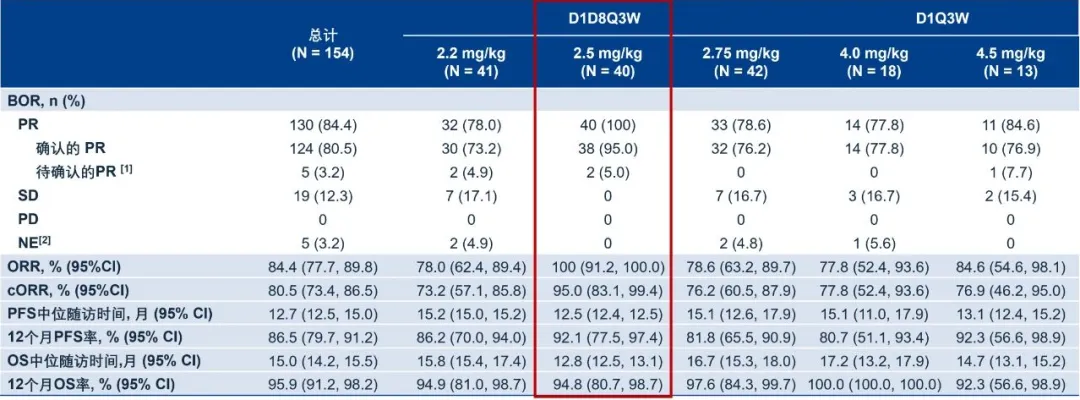
BL-B01D1联合奥希替尼II期研究主要疗效结果
图片来源:参考资料2
康宁杰瑞的JSKN-003是一款HER2双表位ADC,其治疗HER2低表达乳腺癌、铂耐药卵巢癌、HER2阳性乳腺癌适应症已在国内进入III期临床阶段。2024年9月,石药集团与康宁杰瑞达成合作,以最高超30亿元获得JSKN-003的内地独家权益,并成为内地唯一上市许可持有人。
正大天晴的TQB2102也是一款HER2双表位ADC,其用于治疗乳腺癌、胃癌等多种HER2阳性肿瘤的多项关键研究正在同步推进。2025年在WCLC公布的非小细胞肺癌II期研究数据显示,该药在HER2突变患者中ORR达61.1%,在HER2/EGFR双突变患者中ORR高达100%,凸显双靶点设计对耐药突变的突破潜力。
除了上述第一梯队的领先产品,其他药企也纷纷布局这一前沿领域。
映恩生物依托四大ADC技术平台(DITAC、DIBAC等),布局12款ADC候选药物,其中双抗ADC管线包括DB-1418(EGFR/HER3)和DB-1419(B7-H3/PD-L1)。DB-1418于2025年初以最高达12亿美元的金额授权给Avenzo Therapeutics,管线价值通过国际合作持续释放。
信达生物聚焦“双抗ADC+双载荷ADC”技术,已有多款双抗ADC进入临床阶段,包括IBI3001(EGFR/B7H3)、IBI3005(EGFR/HER3)以及全球首个进入临床的PD-L1/TROP2双抗ADC IBI3014,展现了其快速推进的研发能力。
百奥赛图则通过“千鼠万抗”计划构建超百万条全人抗体库,结合RenLite全人抗体平台和BLD1102 Linker-Payload技术,高效开发双抗ADC候选分子。其平台已支持Radiance、IDEAYA等企业开发靶向HER2/TROP2、B7H3/PTK7等组合的双抗ADC。
科伦博泰与默沙东联合推进SKB571(双抗ADC),被开发用于治疗肺癌、消化道肿瘤等多种实体瘤,在默沙东的全力推动下,正在开展I期临床研究。
此外,在今年的AACR年会上,恒瑞医药E-cM-Topi(EGFR/c-Met)、EM-TOPi(EGFR/MUC1)首次公开亮相,信达生物、康宁杰瑞、映恩生物、金赛药业、康方生物、多禧生物、橙帆医药、启德医药也都在会上展示了双抗ADC的早期研究结果。
TONACEA
03
挑战与未来方向
中国创新药企的不断探索取得突破,尤其是百利天恒BL-B01D1鼻咽癌III期研究达成主要终点,标志着双抗ADC的临床价值首次通过中国企业自主研发的领先管线获得验证。
双抗ADC针对性解决了传统ADC耐药、杀伤不彻底等瓶颈,无论是通过双靶点设计覆盖抗原丢失的肿瘤细胞,还是结合免疫激活机制重塑肿瘤微环境,都为HER2低表达乳腺癌、Claudin 18.2阳性胰腺癌等难治性肿瘤提供了新的治疗思路,并推动肿瘤治疗从“单一药物”向“精准联合疗法”升级,比如双抗ADC与PD-1抑制剂的联用,已在临床前研究中展现出卓越的协同效果。
跨国巨头也已敏锐察觉到双抗ADC的价值。阿斯利康、辉瑞等通过收购或自研积极布局双抗ADC;默沙东则与科伦博泰就SKB571等ADC管线开展全球合作,并行使相关选择权;第一三共、基因泰克等传统ADC强者也纷纷公开双抗ADC开发计划。这些动态不仅印证了技术方向的可信度,也预示着未来全球竞争将愈发激烈。
然而,双抗ADC要从理论优势转化为临床价值,仍面临多重挑战,其成功的关键在于能否真正实现“1+1>2”的协同效应。并非任意两个靶点组合都能发挥协同效应,“双靶点协同”的假设需在临床中谨慎验证。例如HER2/CD46的组合,是因CD46在HER2阳性肿瘤中稳定表达且与耐药相关,能弥补HER2抗原丢失的缺陷。若靶点组合缺乏临床逻辑,比如选择两个无协同作用的抗原,反而可能因双抗亲和力失衡导致靶向效率下降,甚至增加脱靶风险。
同时,双抗的复杂结构让分子设计复杂度大幅提升,双抗的链间错配、聚集性、稳定性等难题尚未完全解决,附加毒性载荷后更易引发不可预期的免疫原性反应或药代动力学变化。此外,相比传统单抗ADC,其生产工艺开发、质量控制和规模化生产难度更高,对药企的CMC能力提出严峻考验。
尽管挑战仍在,双抗ADC无疑正在深刻重塑肿瘤治疗的研发格局,成为中国创新药实现“从并跑到领跑”跨越的重要机遇,为中国创新药出海开辟新路径。但需警惕的是,再创新的技术路线,一旦陷入同质化竞争,也难免终将造成临床资源的浪费,同时稀释其商业价值。
未来真正具备竞争力的,必是那些深耕生物学机制、拥有差异化临床策略,并率先突破关键技术平台的企业。唯有始终以临床价值为导向,理性推进研发与转化,双抗ADC才有望真正承载起引领中国创新药未来的期待。

 产业资讯
产业资讯
 GBIHealth
GBIHealth  2026-05-15
2026-05-15
 411
411

 产业资讯
产业资讯
 药渡
药渡  2026-05-15
2026-05-15
 356
356
 产业资讯
产业资讯
 丁香园Insight数据库
丁香园Insight数据库  2026-05-15
2026-05-15
 462
462
 热门资讯
热门资讯