 产业资讯
产业资讯
 2015-11-05
2015-11-05
 3497
3497
来源:药智网 2015-11-05
看点:
Ÿ1.由广西慧宝源申报的1.1类新药注射用曲沙他滨及其制剂,2015年10月12日获得药审中心承办。
2.太景医药研发(北京)申报的伏拉瑞韦及其制剂,用于治疗丙肝,是NS3-4A蛋白酶抑制剂,2015年10月13日进入药审中心,目前未查到排队信息。
3.本月集中审评见成效,临床批件出现井喷。
10月份,集中审评继续发威,据药智数据库统计,国庆放假之后至10月31日,状态由“在审评”变更为“在审批”的受理号就达到了1300+个,而本月新承办的数量持续走低,根据最新统计,2015年10月份CDE共承办新的药品注册申请以受理号计有541个(复审除外,下同)。
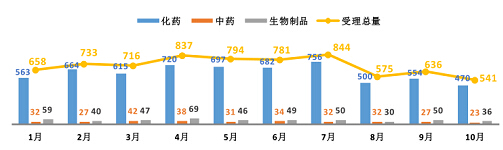
图一 2015年1-10月CDE药品受理情况
2015年10月,受理总量环比下降14.9%。其中化药470个,中药23个,生物制品36个,药用辅料11个,体外诊断试剂1个。化药、中药、生物制品的受理数量较上月都有减少。以下让我们分析一下化药、中药、生物制品的注册受理及审评情况。
一.化药
10月份CDE共承办新的化药注册申请以受理号计有470个,环比下降15.2%。
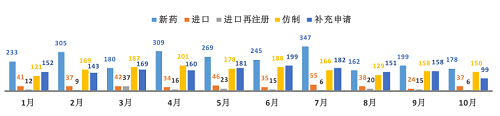
图二 2015年1-10月CDE化药各申请类型受理情况
以下对2015年10月CDE化药受理情况进行详细分析。
1.新药
10月新的化药新药申报数量为178个,占到了化药申报数量的37.9%。
1)1.1类新药
本月CDE受理化药1.1类共计17个受理号,涉及8个品种。下图为10月新承办的1.1类新药。
表一 2015年10月新承办的1.1类新药
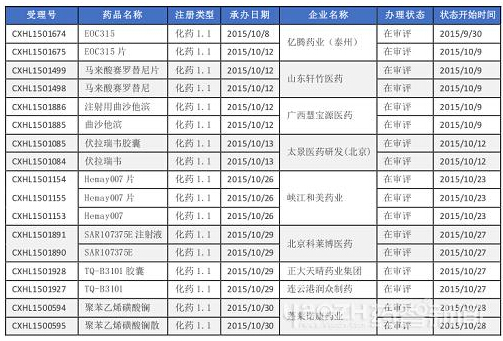
广西慧宝源申报注射用曲沙他滨及其制剂,于2015年10月12日获得药审中心承办,该品种为抗肿瘤胞苷类似物,治疗癌症,shire公司曾经开发,后来放弃。
太景医药研发(北京)申报的伏拉瑞韦及其制剂,用于治疗丙肝,是NS3-4A蛋白酶抑制剂,据了解,该药在美国已进入II期临床,2015年10月13日进入药审中心,目前未查到排队信息。
北京科莱博申报的SAR107375E及注射液是与赛诺菲合作开发的项目,属于凝血酶和Xa因子抑制剂,用于抗凝血治疗,SAR107375E可能是一种酒石酸盐。
聚苯乙烯磺酸镧用于治疗慢性肾功能衰竭(chronic renal failure,CRF)高磷血症。
2)3.1类新药
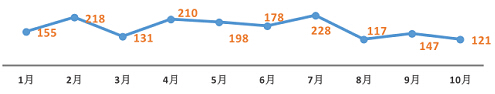
图三 2015年1-10月化药3.1类新药受理数量情况
从8月开始,化药3.1类的申报数量开始减少,临床自查等相关公告的发布对企业确实造成了很大的影响。
3)仿制药
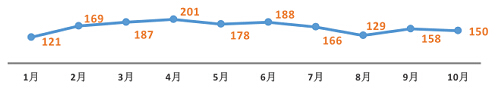
图四 2015年1-10月化药仿制药受理数量情况
在今年十二届全国人大常委会第十七次会议上,《关于授权国务院开展药品上市许可持有人制度试点和药品注册分类改革试点工作的决定(草案)》引起广泛关注。草案建议:第一,参考美国、欧盟等国家和地区的做法,实行药品上市许可持有人制度,允许药品注册人即药品上市许可持有人与生产企业相分离,此方案有利用调动研发人员的积极性,有效的避免低水平的重复;第二,授权国务院在化学药品领域组织开展药品注册分类改革试点,暂时将药品管理法规定的“已有国家标准的药品”调整为“与原研药品质量和疗效一致的药品”,切实的提高仿制药的准入门槛。药品上市许可持有人制度试点和药品注册分类改革试点的期限为二年,对药企乃至整个医药研发圈都是一个极大的挑战。
二.中药
10月份CDE承办新的中药注册申请受理号共计23个,其中新药5个,补充申请17个。
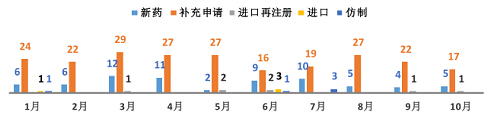
图五 2015年1-10月CDE中药受理情况
三.生物制品
10月份CDE承办新的生物制品注册申请受理号共计36个,新药9个,补充申请24个。
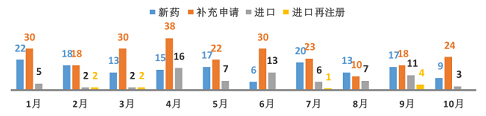
图六 2015年1-10月CDE生物制品受理情况
本月生物制品新药申请有所减少,其中有2个1类生物制品项目获得承办。
表二 2015年10月新承办的1类生物制品品种

注:排队序号截止至2015年11月3日。
四.CDE审评完成情况
本月,集中审评来势汹汹,根据药智注册与受理数据库最新统计,2015年1-10月份(状态开始时间从2015年1月1日至2015年10月31日)审结受理号数量共计6669个。
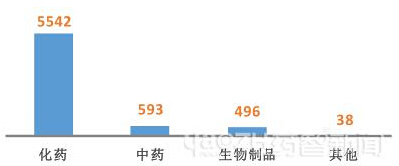
图七 2015年1-10月CDE各药品类型审结数量情况
可以看到,2015年截止到目前,审结完成的主要集中在化药上,占到了83.1%。其中其他类型指体外诊断试剂和辅料。
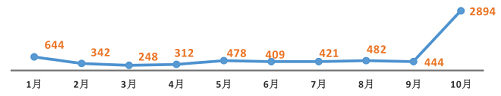
图八 2015年1-10月每月CDE审结数量情况
从7月开始,CDE开始了集中审评,至10月31日,CDE审评完结的受理号达到了2894个,出现了大幅增加,较9月环比增长551.8%。尤其是在临床批件的获批方面,往年,一个药企平均一年拿一到两个临床批件,而最近一到两个星期一次性拿五、六个,甚至十几个临床批件,详细情况可查看往期报告《临床批件呈井喷》。
数据来源:药智注册与受理数据库

 产业资讯
产业资讯
 Medaverse
Medaverse  2025-12-22
2025-12-22
 137
137

 产业资讯
产业资讯
 医药笔记
医药笔记  2025-12-22
2025-12-22
 138
138

 产业资讯
产业资讯
 CGT分享家
CGT分享家  2025-12-22
2025-12-22
 139
139