 研发追踪
研发追踪
 医药魔方
医药魔方
 2022.02.28
2022.02.28
 1796
1796
2月21日,阿斯利康/第一三共宣布关键III期DESTINY-Breast04临床试验获得高水平积极结果。在HER2低表达不可切除和/或转移性乳腺癌患者中,与化疗相比,Enhertu(trastuzumab deruxtecan)在无进展生存期(PFS)和总生存期(OS)方面均有统计学意义和临床意义的改善,无论患者激素受体(HR)状态如何。该项结果是首个针对HER2低表达转移性乳腺癌患者的HER2靶向治疗的III期试验结果。

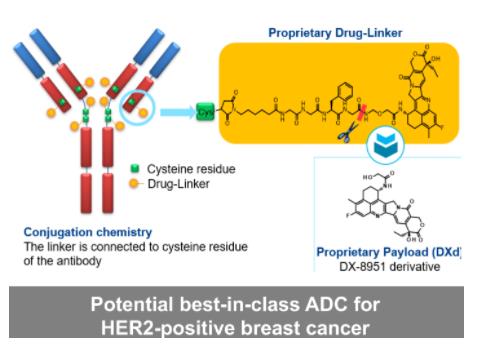
Enhertu是一款靶向HER2的ADC,采用第一三共专有的DXd ADC技术设计。由HER2单抗通过稳定的四肽可裂解连接子连接于拓扑异构酶I抑制剂有效载荷(依沙替康衍生物)上。该产品是第一三共肿瘤产品组合中领先ADC,也是阿斯利康ADC科学平台中最先进的项目。2021年,Enhertu全球销售额是4.26亿美元(不包括日本市场)。
ESTINY-Breast04研究是一项全球、随机、开放标签、注册性III期临床试验,旨在评估Enhertu (5.4 mg/kg)与化疗(卡培他滨、艾立布林、吉西他滨、紫杉醇或白蛋白结合型紫杉醇)相比在HR阳性(n=480)或HR阴性(n=60),既往接受过一线或二线化疗的HER2低表达不可切除和/或转移性乳腺癌患者的疗效和安全性。患者以2:1的比例随机分配,接受Enhertu或化疗。
研究的主要终点是HR阳性患者的无进展生存期(PFS)。关键次要终点包括所有随机患者基于BICR的PFS(无论HR状态如何)、HR阳性患者的OS和所有随机患者的OS(无论HR状态如何)。其他次要终点包括基于BICR和研究者评估的PFS,基于BICR和安全性的反应持续时间。
结果显示,该研究达到了其主要终点,与标准治疗化疗相比,Enhertu在经治的HR阳性HER2低表达转移性乳腺癌患者中表现出优越的PFS。该试验也达到了 HER2低表达转移性乳腺癌患者PFS的关键次要终点,无论HR状态如何(HR阳性或HR阴性)。该试验也达到了HR阳性患者在中期分析中的OS关键次要终点,无论患者HR状态如何。
阿斯利康肿瘤研发执行副总裁 Susan Galbraith 说:“今天来自 DESTINY-Breast04的历史性消息可能会重塑乳腺癌的分类和治疗方式。靶向HER2的治疗从未在HER2低转移性乳腺癌患者中显示出益处。Enhertu的这些结果是向前迈出的一大步,可能会扩大我们针对HER2表达的全谱的能力。”
英文原文链接:http://www.pharmabiz.com/ewsDetails.aspx?aid=145985&sid=2

 新浪医药
新浪医药
 2018.07.12
2018.07.12
 34376
34376

 医药地理
医药地理
 2018.10.22
2018.10.22
 18834
18834

 医谷
医谷
 2019.03.18
2019.03.18
 18793
18793