 研发追踪
研发追踪
 医麦客News
医麦客News
 2022.12.19
2022.12.19
 2109
2109
2022年12月16日/医麦客新闻 eMedClub News/--近日,蓝鸟生物和诺华在2022ASH大会上公布了其用于治疗镰状细胞贫血病基因疗法的最新进展。
蓝鸟生物:Lovo-cel
Lovo-cel是一款基于慢病毒的用于治疗镰状细胞贫血病(SCD)的自体干细胞疗法,通过慢病毒载体将具备功能的人βA-T87Q-珠蛋白基因拷贝至取自患者体内的造血干细胞中,再将这些干细胞回输到患者体内,使其自主生成β-珠蛋白,从而消除或大幅降低继续输血需求。值得一提的是,2021年2月,FDA暂停了lovo-cel的临床试验,并在同年解除限制。
本次ASH年会蓝鸟生物公布了正在进行的I/II期HGB-206试验C组的最新数据。HGB-206研究是目前业内规模最大,随访时间最长,最成熟的SCD基因疗法临床试验之一。截至2022年8月,蓝鸟Lovo-cel的三项临床研究中,已有50名患者接受了治疗,患者随访时间长达7年,(中位数:37.7个月)。
➤研究结果
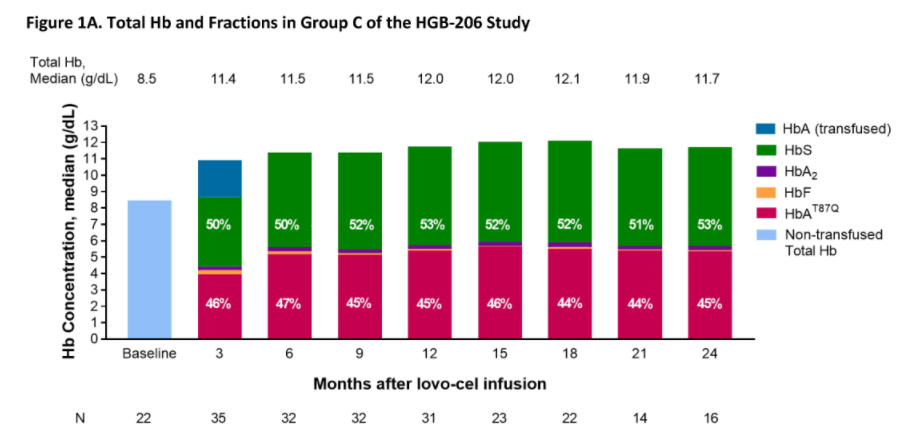
数据截至2021年7月,C组35例患者接受了lovo-cel输注,中位随访时间为20.9个月(8.5-28.5)。在29名可评估的患者中,截至最后一次随访,在2年的母研究中,28名患者在输注lovo-cel后严重血管闭塞发作(VOEs)完全解决,而在入组前2年,每年3.5例(1.0-13.5例);在长期随访研究中未见严重VOE的报告。关键溶血指标接近正常水平。
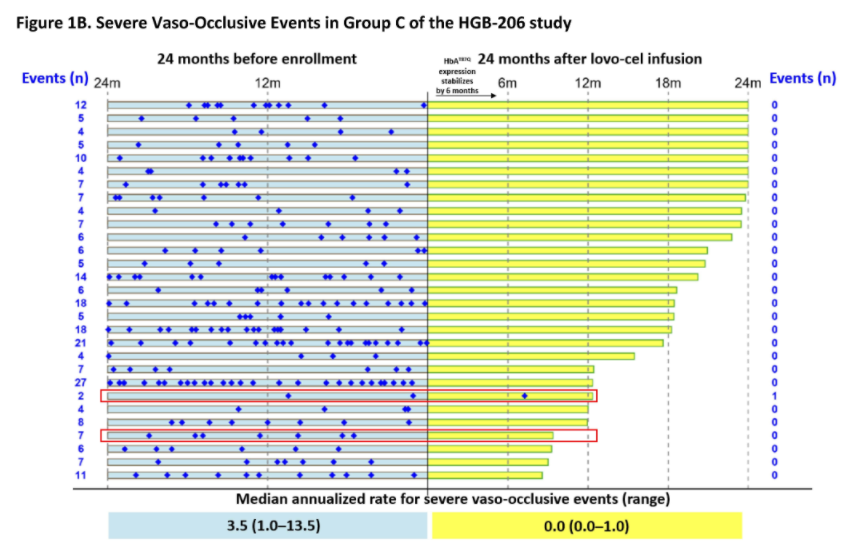
总的来看,该种治疗技术可使大多数红细胞持续产生β-珠蛋白,从而减少溶血,并解决严重的血管阻塞事件。据业内人士称,蓝鸟生物仍有望在2023年第一季度提交lovo-cel 的生物制品许可申请(BLA)。
Intellia/诺华:OTQ923
OTQ923是一种基于CRISPR/Cas9基因组编辑的体外自体干细胞(HSCs)疗法,用于治疗镰状细胞病(SCD)。本次ASH大会上公布的是OTQ923用于治疗镰状细胞病(SCD)的I/II期试验的最新数据。
截至2022年7月8日,2名参与者接受了OTQ923治疗,随访分别为9个月和3个月。
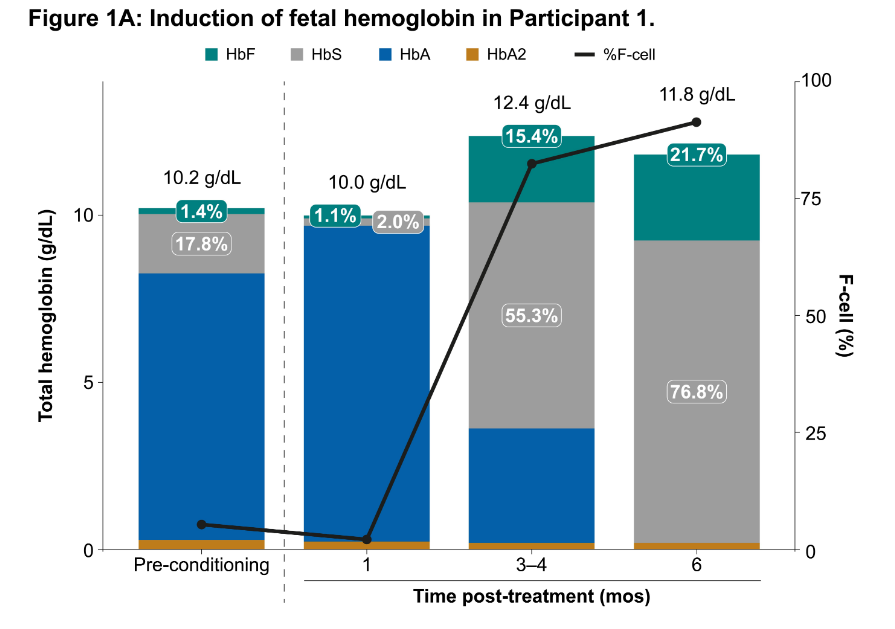
研究结果显示,参与者1的HbF水平在输注6个月后上升,并在数据截止时保持稳定,即在输注9个月时的HbF水平为22.1%。参与者2在输注3个月后HbF水平达到了15.9%。此外,直到输注完成后的第6个月,受试者1的外周血中编辑等位基因的比例一直维持在60%以上。

总的来说,初步数据显示,在接受治疗后,两名患者均有获益,两者的HbF水平均有临床意义的增加,并且该疗法安全性可控,有望成为严重SCD患者一种潜在的治疗选择。
结语
事实上,蓝鸟的基因疗法研发是颇为曲折的,慢病毒技术路线也曾经遭到过FDA和业内专家的质疑,并且蓝鸟已上市的基因疗法并没有为其创造太大的利润。但是,蓝鸟仍然在前进,近期蓝鸟卖掉了优先审查券补贴家用。做创新药本就九死一生,龙头企业也不例外,尤其是在基因治疗这一新兴赛道研发风险更为放大。因此,无论成功或失败,先行者值得敬佩,其研发经验能够给后来者以借鉴。此外,蓝鸟一直也在对基因疗法和商业模式进行优化,有望让基因疗法惠及更多患者。

 新浪医药
新浪医药
 2018.07.12
2018.07.12
 34377
34377

 医药地理
医药地理
 2018.10.22
2018.10.22
 18834
18834

 医谷
医谷
 2019.03.18
2019.03.18
 18794
18794