 研发追踪
研发追踪
 Insight数据库
Insight数据库
 2023.03.06
2023.03.06
 1955
1955
2023 年 3 月 1 日,默沙东宣布,PD-1 单抗 Keytruda 用于早期 NSCLC 围手术期治疗的 III 期临床试验 KEYNOTE-671 研究已达到双重主要终点之一无事件生存期(EFS),病理完全缓解(pCR)和主要病理学缓解(mPR)这两个次要终点也表现出了统计学意义上的改善。后续将继续评估另一主要终点 OS,并在医学会议上发布详细数据。
基于此,FDA 已经接受默沙东递交的新适应症上市申请(sBLA),并将 PDUFA 决定日期设定在 2023 年 10 月 16 日。具体适应症为:K 药联用铂类化疗术前新辅助治疗 II 期、IIIA 或 IIIB 期 NSCLC 患者,随后在术后作为单药辅助治疗。
继昨日的前列腺癌失利之后,K 药继续稳扎稳打,又掰回一局,在 NSCLC 治疗的前线推进中再下一城。

截图来自:默沙东官网
KEYNOTE-671 是一项随机、双盲全球多中心 3 期研究,首次启动于 2017 年 11 月(ClinicalTrials.gov,NCT03425643),共入组 786 例患者,1:1 随机分配到 K 药组和安慰剂组。中国内地也是其试验地点之一,在 CDE 登记于 2019 年 9 月,同年 12 月完成首例入组,共入组 118 人。
默沙东 K 药的肺癌系列研究布局极广,在 ClinicalTrials.gov 上连同各种联合治疗方案,已经登记了超过 400 项,且有 5 项肺癌适应症已经获批,涵盖二线、一线和辅助治疗。KEYNOTE-671 的成功和 sBLA 申报,将 K 药的适应症再推进到了新辅助环境中。
众所周知,肺癌是全球发病率和死亡率均居前列的致命癌种,2020 年 WHO 数据显示,全球有 220 万新发肺癌患者和 180 万例肺癌导致的死亡,而其中非小细胞肺癌占据了 81% 的比例。早期筛查无疑是延长肺癌患者生存时间的关键手段之一,对于早期肺癌患者的治疗,也仍存在着未满足的医疗需求。
目前,全球药企都在积极布局 NSCLC 早期新辅助/辅助治疗。据 Insight 数据库显示,已有 56 项相应临床试验登记,其中包括 11 项 III 期临床,从结果释放和上市申报上 K 药和 O 药无疑走在前头,国内四款 PD-1 单抗也有相应布局。
全球 PD-1 单抗辅助/新辅助 NSCLC III 期临川试验登记
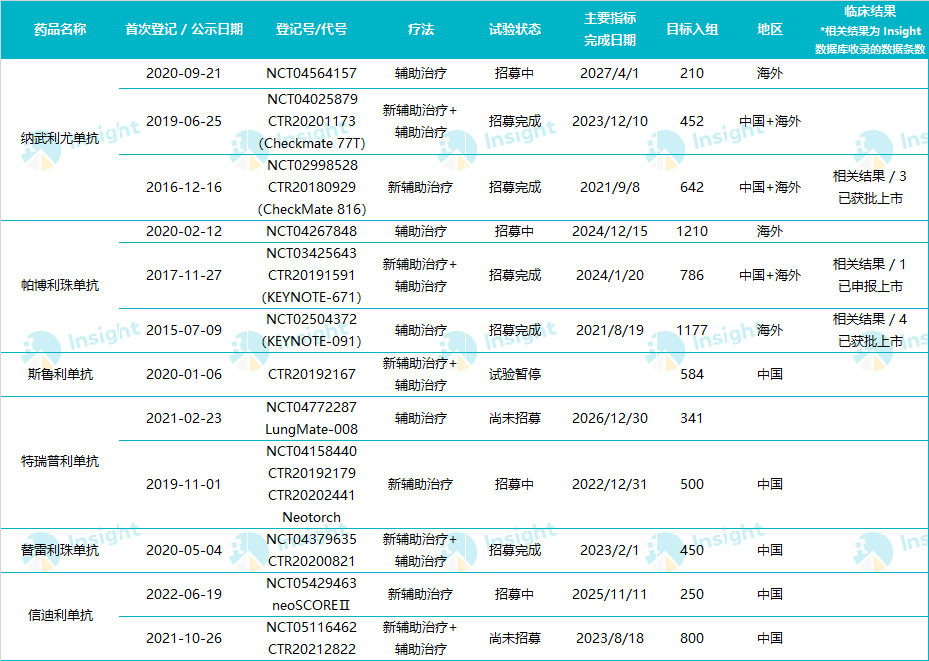
数据来自:Insight 数据库

 新浪医药
新浪医药
 2018.07.12
2018.07.12
 34519
34519

 医药地理
医药地理
 2018.10.22
2018.10.22
 18890
18890

 医谷
医谷
 2019.03.18
2019.03.18
 18885
18885