 研发追踪
研发追踪
 Insight数据库
Insight数据库
 2023.05.22
2023.05.22
 1882
1882
5 月 17 日,阿斯利康宣布,III 期临床试验 FLAURA2 获得了高水平阳性结果,奥希替尼(Tagrisso,泰瑞沙®)联合化疗相较于奥希替尼单药一线治疗局部晚期(IIIB-IIIC 期)或转移性(IV 期)EGFR 突变 NSCLC 中表现出具有统计学显著性和临床意义的 PFS 改善。
目前,OS 数据尚未成熟,将在后续分析中继续评估;安全性方面则与既往各药物特征一致。阿斯利康将在后续医学大会上公布 FLAURA2 数据。
这项临床试验的成功,意味着 EGFRm NSCLC 患者有望迎来更优治疗方案,延长其一线疗法获益时间。

截图来自:阿斯利康官网
FLAURA2(登记号:NCT04035486)是一项随机、开放标签、全球多中心 III 期临床试验,纳入 586 名局部晚期(IIIB-IIIC 期)或转移性(IV 期)EGFRm NSCLC 患者进行一线治疗。患者接受每日一次奥希替尼 80 mg 联合每三周一次化疗(培美曲塞 [500 mg/m²] + 顺铂 [75 mg/m²] 或卡铂[AUC5]),持续四个周期;随后每三周接受一次奥希替尼 + 培美曲塞维持治疗。
这项试验登记于 2019 年 6 月,在美国、欧洲、亚洲等 20 多个国家的 150 多个中心招募患者,其中也包括了中国地区的 112 例患者。本次积极结果是对 PFS 主要终点的最终分析。试验仍在进行中,将继续评估 OS 的次要终点。
FLAURA2 试验历程

截图来自:Insight 数据库网页版(http://db.dxy.cn/v5/home/)
奥希替尼作为首款获批上市、临床证据最充分的三代 EGFR 抑制剂,其单药疗法已经在中美日欧在内的 100 多个国家或地区获批上市,获批适应症包括晚期 EGFRm NSCLC 二线、一线治疗以及早期 EGFRm NSCLC(IB/II/IIIA 期)辅助治疗。
除了在晚期疾病状态中评估奥希替尼与化疗的联合疗法(FLAURA2 研究)之外,阿斯利康还瞄准早期肺癌开展了多项 III 期临床,包括对于新辅助可切除环境(NeoADAURA 研究)、IA2-IA3 期辅助可切除环境(ADAURA2)和 III 期局部晚期不可切除环境(LAURA)。
同时,针对耐药问题,阿斯利康也在进行持续探索:联用口服 MET 抑制剂赛沃替尼开展 II 期临床 SAVANNAH 和 III 期临床 SAFFRON,联用多种其他药物的 II 期临床 ORCHARD。不光奥希替尼联合疗法,阿斯利康还基于自家平台开发了 EGFR/c-MET 双靶点 ADC 新药 AZD9592,同样旨在解决耐药问题。
在整体 NSCLC 布局方面,阿斯利康期望到 2030 年其商业化疗法能够覆盖超 50% 的非小细胞肺癌患者,从当前临床布局来看:
奥希替尼有望作为约 16% 的 EGFR 突变人群的基石疗法,耐药群体则有 AZD9592;
度伐利尤单抗在约 70% 的 IO 敏感不可切除疾病群体中持续建设领导地位,后继双抗管线如 PD-1/TIGIT 双抗 rilvegostomig、PD-1/CTLA-4 双抗 volrustomig、PD-1/TIM3 双抗 sabestomig 则有望成为下一代 PD-(L)1 为患者提供改善;
其他驱动基因突变约 12% 的患者,部分有度伐利尤单抗和 Dato-DXd 覆盖;而 2% 的 HER2 突变/过表达群体中则以 Enhertu 为首的 ADC 管线替代系统化疗。同时,包括细胞疗法在内的新平台新管线也在持续推进。
阿斯利康肺癌领域布局
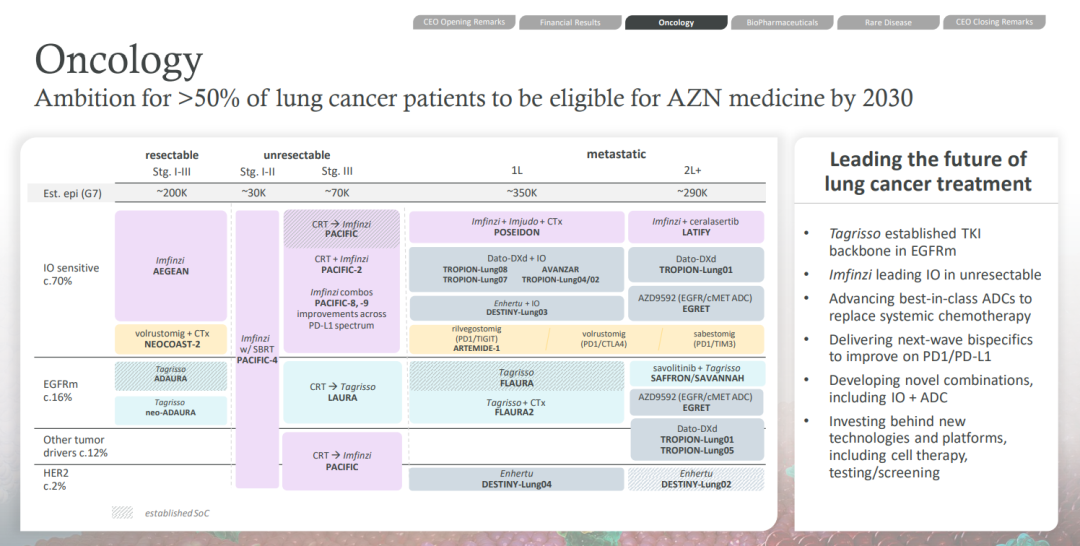
*Est. epi (G7) 即在欧美日 7 国的流行病学 截图来自:阿斯利康 2023Q1 季报

 新浪医药
新浪医药
 2018.07.12
2018.07.12
 34376
34376

 医药地理
医药地理
 2018.10.22
2018.10.22
 18833
18833

 医谷
医谷
 2019.03.18
2019.03.18
 18792
18792