 研发追踪
研发追踪
 2015-04-08
2015-04-08
 5369
5369
来源:浮米网 2015-04-08
Clovis Oncology的rucaparib在美国获得“突破性治疗”资格,作为单药治疗BRCA突变的晚期卵巢癌,是首个获得该资格的聚腺苷二磷酸核糖聚合酶(PARP)抑制剂。消息一出,Clovis Oncology的股价上涨了不少。
PARP是一类DNA损伤检测酶,在DNA损伤修复与细胞凋亡中发挥着关键作用。多项研究表明PARP是治疗肿瘤的良好靶点。此次,rucaparib被批准作为3线治疗药物,用于一线二线药物治疗失败的BRCA突变的晚期卵巢癌。
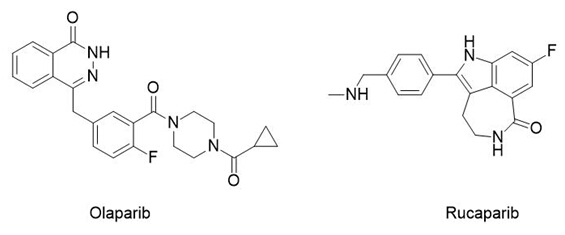
到目前为止,有多个PARP抑制剂进入临床,包括是阿斯利康的olaparib、艾伯维的veliparib(ABT-888)、BioMarin的BMN-673、Clovis Oncology的rucaparib、和Tesaro的niraparib、National Cancer Institute (NCI)的Talazoparib (BMN-673),Teva的CEP-9722、BeiGene的BGB-290。其中必须提一下阿斯利康的Olaparib(商品名:Lynparza),它是第一个在欧盟(EMA)获批上市的PARP抑制剂。阿斯利康也曾向FDA申请“突破性治疗”资格,但没有成功。

 研发追踪
研发追踪
 药时代
药时代  2026-02-13
2026-02-13
 337
337

 研发追踪
研发追踪
 医药魔方
医药魔方  2026-02-13
2026-02-13
 326
326

 研发追踪
研发追踪
 瞪羚社
瞪羚社  2026-02-13
2026-02-13
 315
315