 研发追踪
研发追踪
 药时代
药时代  2026-02-13
2026-02-13
 3500
3500
2026年2月10日,Evommune公布了其核心候选药物EVO301在中重度特应性皮炎患者(AD)中开展的2a期临床试验顶线结果。研究数据显示,EVO301成功达到主要终点,疗效显著优于安慰剂,且有望向当前自免主流药物:赛诺菲的度普利尤单抗(Dupixent)与礼来的Ebglyss(IL-13)发起挑战。

来源:雪球网
消息公布后,Evommune股价在盘前交易中应声大涨70%,迅速成为生物科技领域备受瞩目的焦点。
当多数疗法仍围绕IL-4/IL-13等成熟通路布局时,EVO301独辟蹊径,精准靶向免疫炎症网络上游的IL-18。这一战略选择,不仅使其成为当前研发管线中极具差异化的稀缺资产,也为投资者开辟了更具深度的价值想象空间。
01
早期数据亮点:疗效信号明确
首先,让我们聚焦这次临床试验本身。本研究共入组70例成年中重度特应性皮炎患者,患者仅在第1天和第28天接受了5mg/kg的药物注射,观察期为12周。试验主要评估其在中重度特应性皮炎患者中的疗效与安全性,核心终点为湿疹面积和严重程度指数(EASI)评分的改善情况。
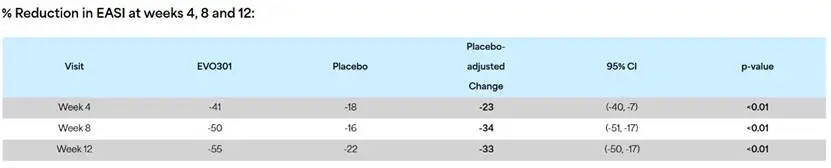
在第12周时,EVO301治疗组的湿疹面积和严重程度指数(EASI)较基线平均下降了55%,而安慰剂组仅下降了22%,两组之间的差异具有高度统计学意义(p<0.01)。这种显著的疗效在第4周和第8周时就已经显现,这表明药物起效迅速,且全程保持疗效。
来源:企业官网
经安慰剂校正后,EVO301组患者第12周的EASI评分降幅达33%,与自免“标杆”度普利尤单抗在Ⅲ期研究中的疗效数据(35%-36%)相当。
在第12周,23%的EVO301组患者达到研究者整体评估(IGA)0/1分(皮损完全清除或基本清除)且较基线改善≥2分,安慰剂组无人达到该终点。这一结果也与度普利尤单抗、礼来Ebglyss水平相近,显示出极强的市场竞争力。
在安全性方面,EVO301表现出了良好的耐受性。试验期间未报告与药物相关的严重不良事件,也没有患者因不良事件而停止治疗,且活性组与安慰剂组间事件无显著差异。
02
为何EVO301如此受到资本追捧?
在AD这片红海,III期捷报已难激起太大波澜。Apogee的抗IL-13抗体APG777、安进的OX40L单抗Rocatinlimab、赛诺菲的OX40L单抗Aplitelimab等药物均在AD的III期研究中传出积极消息,但市场反响常相对温和。在此背景下,EVO301仅凭一项II期数据便引起资本狂欢,才更显耐人寻味。这并非偶然,而是投资逻辑与科学价值的深度共振。
资本市场对生物科技资产的定价,往往包含了对未来不确定性的溢价。II期临床成功的药物,其疗效与安全性的全貌尚未完全展现,保留了巨大的想象与叙事空间。积极的早期数据犹如一个强有力的“概念验证”,点燃了市场对其解决更大临床问题、开拓广阔市场的预期。相比之下,进入III期阶段的药物,其成功概率已部分被市场预判,积极数据的公布有时仅是“预期兑现”,甚至可能因利好出尽而回调。EVO301的II期成功,恰好处于“概念已验证,空间仍巨大”的黄金节点。
资本的热忱最终需植根于产品解决真实世界临床问题的潜力。EVO301获得关注度,源于它精准瞄准了当前AD治疗未满足的需求。
首先,上游调控的差异化机制,具备多重免疫调节潜力。EVO301是一种长效融合蛋白,由IL-18结合蛋白和抗血清白蛋白Fab相关结构域组成,理论上比传统抗体能更有效地渗透进发炎组织中和异常上调的IL-18活性。
IL-18是位于炎症“上游”的关键细胞因子,能同时调控Th1、Th2、Th17/22及先天免疫多条通路,具备更广谱的免疫调节潜力。II期临床的生物标志物分析证实,EVO301治疗后,患者体内不仅Th2通路标志物(如CCL-17、CCL-22)下降,非Th2通路标志物(如IL-22)也同步降低,从机制上验证了其“多通路抑制”的能力,使其与现有疗法具有天然的互补性。
其次,直击未满足的临床需求:难治性患者。正是得益于上述作用机制,EVO301被视为攻克“难治性”AD的利器。对于那些对现有生物制剂(如Dupixent)、JAK抑制剂等应答不足或不耐受的患者群体,EVO301提供了机制上互补的新选择,且存在联合治疗的巨大想象空间,有望切入了一个庞大且亟待满足的临床市场。
再者,给药方式长效便捷。目前EVO301已支持每季度一次的皮下注射,相较于目前多数需要每两周或每月给药的生物制剂,在患者依从性和生活便利性上具备明显优势。研究团队指出,未来通过优化给药方案(如调整剂量或频率),疗效仍有提升空间。
03
IL-18靶点已展开竞速赛
EVO301的成功,将业界目光再次引向IL-18这一潜力靶点。全球范围内,该赛道的竞争图景已然展开:
瑞士公司AB2 Bio开发的新型重组人白介素18结合蛋白Tadekinig alfa进展较快,已于2021年进入针对原发性单基因HLH患者的关键Ⅲ期试验。2025年,公司宣布日本Shinyaku以最高可达1.86亿美元的总金额获得了该药物在美国的许可权。AB2 Bio将继续筹备在美国提交其生物制品许可申请,以推动该适应症的上市批准。

来源:AB2公告
此外,诺华开发的IL-1β/IL-18双抗MAS-825也已进入Ⅲ期研究阶段。该分子由IL-1β抗体与IL-18单抗CMK389融合而成。
在AD领域,Apollo Therapeutics/Avalo Therapeutics开发的IL-18单抗AVTX‑007(camoteskimab)与EVO301将形成竞争。2025年9月,该药在AD的2a期试验中达到主要终点:患者平均EASI评分降低约80%,约65%的患者EASI评分降低≥75%,约60%达到研究者整体评估(IGA)0/1应答。
研发过程中亦不乏挫折。GSK开发的IL-18抗体GSK1070806曾针对特应性皮炎、克罗恩病、肾移植后移植物功能延迟及糖尿病等多个适应症开展研究。2025年4月底,基于数据监查委员会章程及第二次期中分析结果,GSK主动终止了该药用于特应性皮炎的两项II期研究,原因是试验已达到无效性分析中预设的疗效标准。
小结:
EVO301的II期成功,是IL-18通路在自免疾病治疗价值的一次有力验证。它为AD患者,尤其是难治性人群,带来了新的希望。
然而,其最终能否真正撼动度普利尤单抗构筑的自免壁垒,答案不在今日的涨幅里,而在未来的III期数据、监管决策与商业化落地中。
悬念已经埋下。IL-18的故事,或许才刚刚开始。

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-05-18
2026-05-18
 415
415

 研发追踪
研发追踪
 医药魔方Info
医药魔方Info  2026-05-18
2026-05-18
 477
477

 研发追踪
研发追踪
 药研网
药研网  2026-05-18
2026-05-18
 391
391
 热门资讯
热门资讯