 产业资讯
产业资讯
 2014-07-24
2014-07-24
 9208
9208
来源:丁香园 2014-7-24
上市篇
与过去两年同期相比,上半年化药上市批准量有所减少,中药和生物制品相对稳定:
根据丁香园INSIGHT-China Pharma Data数据库统计,今年上半年,CFDA共批准药品上市申请238件(以受理号计,不包含复审,下同)。从总体上来看,批准数量与过去两年同期相比有所减少,但浮动不大。其中减少的部分集中在化药,而中药和生物制品是维持在相对稳定的状态。具体情况,如下图所示:
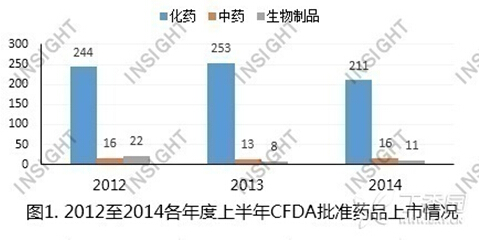
以下,分别来分析今年上半年化药、中药、生物制品的批准上市情况。
一、化药
新药上市批准量略有增加,其他类型均有所减少:
根据丁香园INSIGHT-China Pharma Data统计,上半年,CFDA共批准化药上市申请211件,与过去两年同期相比,总体数量有所减少,但是批准的化药新药数量略有增加。具体情况如下图所示:
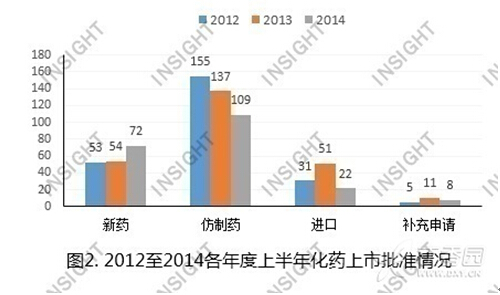
1. 新药上市批准:
(1)1.1类新药
江苏豪森首个1.1类新药上市品种吗啉硝唑引关注:
根据数据显示,今年上半年,共有两个化药1.1类新药品种获批生产,与去年同期持平。分别是江苏豪森的吗啉硝唑(原料药和注射剂),湖南方盛和湖南华纳的阿德福韦酯(原料药),苏州二叶的阿德福韦酯片。具体数据,如下所示:
表1. 2014上半年获批生产的化药1.1类新药:
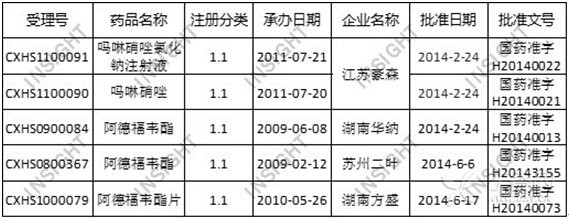
其中,阿德福韦酯在国内已经有多家生产企业,这个1.1类其实已经有些鸡肋。而江苏豪森的吗啉硝唑倒是很值得期待。吗啉硝唑是由江苏豪森自主研发的、我国首个拥有自主知识产权的新一代硝基咪唑类抗菌药。据豪森发布的信息显示,相比市面上的同类产品,具有抗菌活性强、耐受性好、安全性高等特点。这也是江苏豪森迄今为止获批生产的首个1.1类新药品种。
吗啉硝唑的研发历时十余年,江苏豪森于2002年就开始对吗啉硝唑进行立项方面的研究,2005年4月申报临床,同年8月份就获得临床批件,速度之快也令人惊叹。其后,一直处于临床试验阶段。吗啉硝唑按照特殊审批品种进行审评,同时也是国家“重大新药创制专项”项目。2011年7月份申报上市,今年2月底获得上市批准,5月份已正式投产上市,商品名为迈灵达。
上半年,豪森有3个品种获得上市批准,无论是创新药还是仿制药都有所斩获,可谓收获颇丰。具体数据,如下所示:
表2. 2014上半年江苏豪森获批生产的品种:
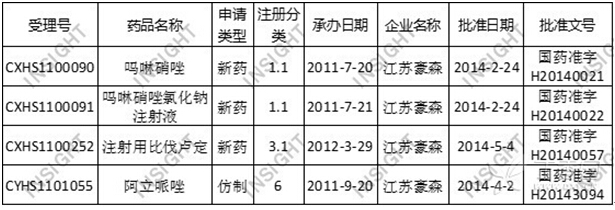
(2)3.1类新药
武汉启瑞的索法酮为国内首次获批上市:
根据丁香园INSIGHT-China Pharma Data数据库统计,上半年,CFDA共批准化药3.1类新药上市申请41件,涉及21个品种(包含原料药)。其中,仅武汉启瑞的索法酮(原料药和干混悬剂)为国内首次上市。索法酮主要用于急性胃炎和慢性胃炎急性发作的治疗,这也是武汉启瑞到目前为止获批生产的唯一一个独家首仿品种,索法酮干混悬剂商品名为瑞琅。
2. 仿制药上市批准
仿制药批准量逐年下降,成都圣诺的恩夫韦肽为国内首仿:
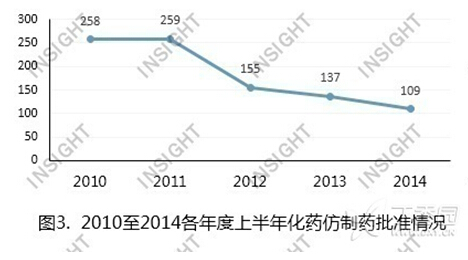
上半年,CFDA共批准化药仿制药上市申请109件。与过去两年同期相比,有所减少。根据数据显示,从2010年至今,化药仿制药批准量在逐年下降。国家食品药品监督管理总局在通过一系列政策和措施鼓励支持药物创新的同时,也对仿制药的质量及仿制水平提出更高要求,在努力改善仿制药重复申报以及资源浪费等现象。
另外,在上半年批准上市的6类仿制药中,成都圣诺生物制药有限公司的艾滋病用药注射用恩夫韦肽为国内首仿。恩夫韦肽是全球首个HIV融合抑制剂,用于治疗成人及6岁以上儿童慢性人类免疫缺陷病毒(HIV)感染,是HIV治疗领域的重要药物,最早由罗氏公司于2013年3月份在美国上市,其后在全球多个国家已上市。罗氏于2005年12月份取得进口批准,恩夫韦肽开始进入中国市场。成都圣诺此次获得恩夫韦肽(原料药3.1类,制剂6类)的上市批准为国内企业首家。
3. 进口批准
有3个进口品种(钆特醇注射液、贝米肝素钠注射液、盐酸西那卡塞片)为国内首次上市:
上半年,CFDA共批准药品进口申请22件,涉及11个品种。与过去两年同期相比,有所减少。其中,博莱科(Bracco)公司的磁共振成像造影剂钆特醇注射液、Laboratorios Farmaceuticos ROVI,S.A.公司的抗血栓药物贝米肝素钠注射液、协和发酵麒麟株式会社的盐酸西那卡塞片为国内首次获批上市的产品。
二、中药
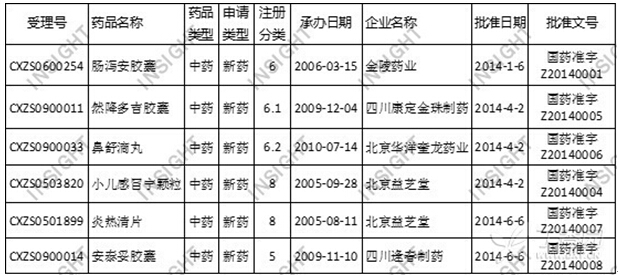
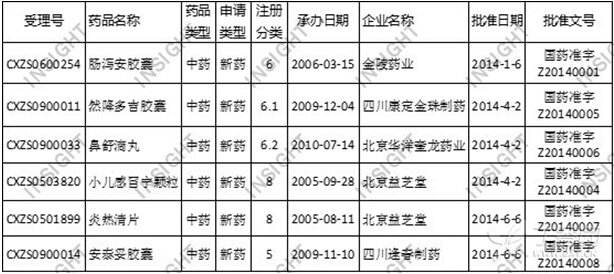
根据数据统计,上半年CFDA共批准中药上市申请16件,与去年同期(13件)相比,大体持平。其中6个为新药,10个为补充申请。于上半年获批上市的中药新药数据,如下所示:
表3. 2014上半年获批上市的中药新药(数据来自丁香园 INSIGHT 数据库):
三、生物制品
上半年CFDA共批准生物制品上市申请11件,但无进口:
根据数据统计,上半年,CFDA共批准生物制品上市申请11件,其中补充申请5件,新药申请6件。与去年同期相比,相对稳定。但遗憾的是,今年上半年没有生物制品获得进口批准。批准上市的生物制品新药数据,如下所示:
临床篇
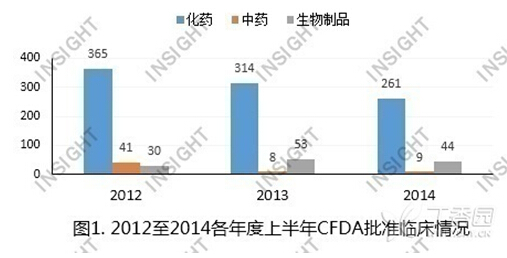
与过去两年同期相比,临床批准数量总体有所减少,主要集中在化药:
上半年CFDA共批准药物临床申请314件(以受理号计,不包含复审,下同)。从总体上来看,批准数量与过去两年同期相比有所减少,而减少的部分主要集中在化药。具体情况,如下图所示:
以下,分别来分析今年上半年化药、中药、生物制品的批准临床情况。
一、化药
批准临床数量与过去两年同期相比有所减少:
上半年,CFDA共批准化药临床261件,其中新药临床批准数量与去年同期相比略有增加,而其他申请类型的批准数量与去年同期相比均有所减少,如下图所示:
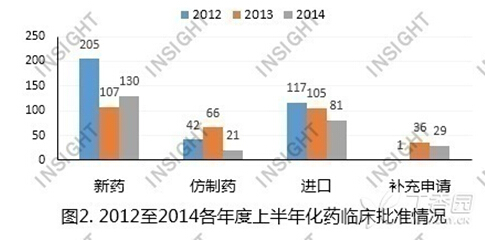
以下,让我们主要看一下今年上半年化药新药和进口的临床批准情况。
1. 新药临床批准:
(1)1.1类新药:
上半年共有10个化药1.1类新药品种获批临床,恒瑞占两个:
根据丁香园INSIGHT-China Pharma Data 数据库统计,今年上半年共有10个化药1.1类新药品种获得临床批件,与去年同期(15个)相比,有所减少。这10个品种里面,江苏恒瑞占据两个,领先于其他企业,分别是抗肿瘤药物环咪德吉(原料药和片剂)和糖尿病用药呋格列泛(原料药和片剂)。上半年获批临床的化药1.1类新药数据,如下所示:
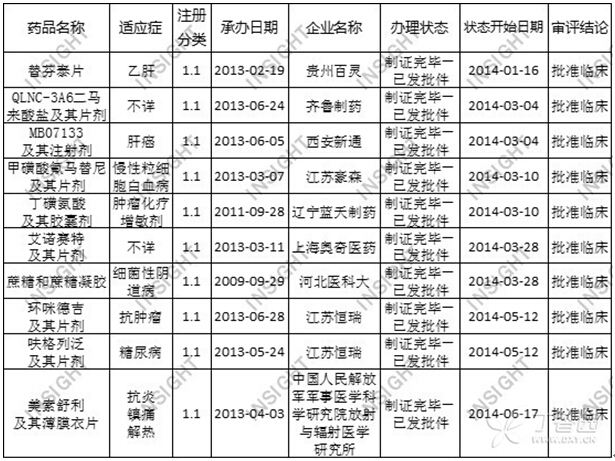
表1. 2014年上半年获批临床的化药1.1类新药:
值得注意的是,其中有3个品种原为上市申请,但最后并未被批准上市,而是发送了临床批件,还需继续进行临床试验。分别是江苏豪森的甲磺酸氟马替尼,辽宁蓝天制药有限公司的丁磺氨酸,河北医科大学的蔗糖凝胶。
另外,从以上数据也可以看出,这些化药1.1类新药品种从进入药审中心到获得临床批件,大多历时一年左右。
(2)3.1类新药:
上半年有3个化药3.1类新药品种首次获得国内临床批准:
上半年,CFDA共批准化药3.1类新药临床申请74件,与去年同期相比有所增加。由于品种较多,我们根据丁香园INSIGHT-China Pharma Data 数据库的品种筛选系统,主要筛选出目前尚未在国内上市、且是国内前两家获批临床的企业和对应品种。具体数据如下所示:
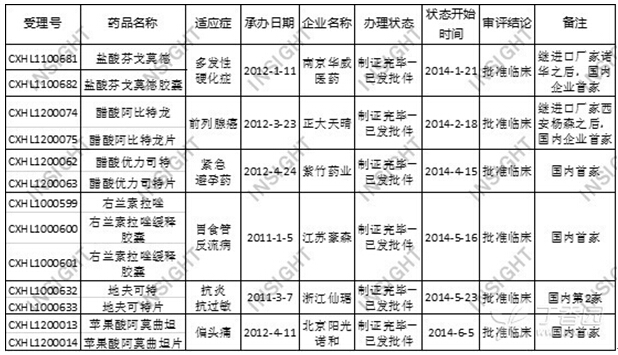
表2. 2014上半年获批临床的化药3.1类新药及对应企业(国内前两家):
2. 进口临床批准:
抗肿瘤药物依然是热点:
2014上半年,CFDA共批准化药进口临床申请81件(以受理号计),与去年同期(105件)相比有所减少。我们根据丁香园INSIGHT数据库的品种筛选系统,筛选出于今年上半年在国内首次获得进口临床批准的11个品种。其中,拜耳有3个品种,诺华有2个品种。另外,这11个品种里面,抗肿瘤药物多达5个,依然是研发热点。具体数据,如下所示:
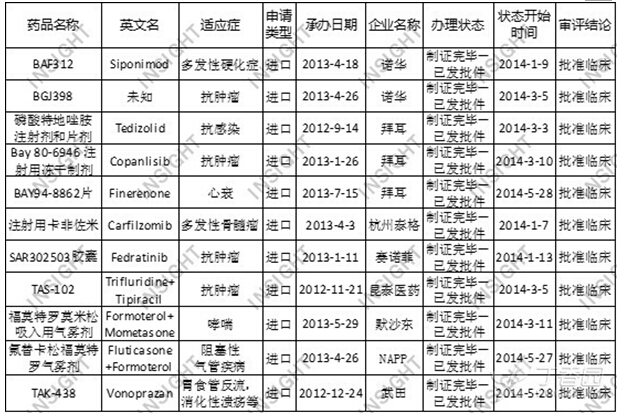
表3. 2014上半年首次获批临床的进口品种:
其中,根据数据显示,只有Onyx 制药公司的卡非佐米(商品名:Kyprolis)于2012年7月获得FDA批准、在美国已上市,其余品种在全球范围内均尚未上市。从这也可以看出,大型制药企业在新药研发时,一般会在国际上同时布局,在多个国家和地区共同展开临床研究。
二、中药
中药临床批准情况相对稳定:
上半年,CFDA共批准中药临床申请9件(以受理号计),与去年同期(8件)相比,近乎持平。其中8个为新药,1个补充申请。具体数据,如下所示:

表4. 2014上半年获批临床的中药:
三、生物制品
上半年共有4个生物制品1类新药品种获批临床,抗肿瘤单抗药物研发热:
根据丁香园INSIGHT-China Pharma Data 数据库统计,上半年,CFDA共批准生物制品临床申请44件(以受理号计),与去年同期(53件)相比,有所减少。其中1类新药有4个品种,而其中有3个是抗肿瘤单抗药物。具体数据,如下所示:
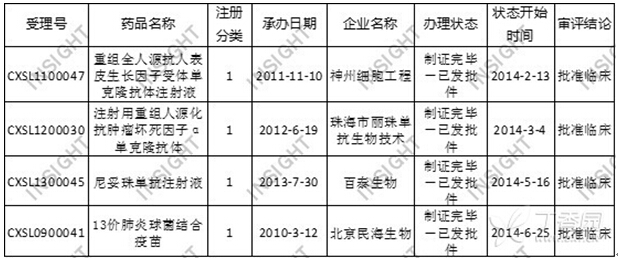
表5. 2014上半年获批临床的生物制品1类新药
:
近些年,医药生物技术发展迅速,而其中单抗药物更是热门。据GEN公司发布的2013年全球最畅销药物排行榜中,前十强中有七个是生物制品,更引人瞩目的是前三名都是单抗药物(阿达木单抗、英夫利昔单抗、利妥昔单抗)。
百泰生物药业有限公司的尼妥珠单抗注射液(商品名:泰欣生),是我国首个人源化抗肿瘤单抗,世界上第三个被批准用于治疗实体瘤的单抗药物,主要用于治疗头颈部、食道、胃、肺、乳腺、结肠、直肠等部位的上皮源性肿瘤。其实,泰欣生已于2008年1月获得上市批准,同年6月份正式上市。上市之后,百泰在继续开展新的适应症的临床研究。
 产业资讯
产业资讯
 国际肿瘤资讯
国际肿瘤资讯  2026-04-02
2026-04-02
 31
31
 产业资讯
产业资讯
 识林
识林  2026-04-02
2026-04-02
 33
33

 产业资讯
产业资讯
 医药地理
医药地理  2026-04-02
2026-04-02
 36
36