 研发追踪
研发追踪
 药明康德
药明康德  2022-01-10
2022-01-10
 3501
3501
日前,Genprex公司宣布,美国FDA已授予基因疗法Reqorsa快速通道资格(FTD),与默沙东(MSD)的重磅PD-1抑制剂Keytruda(帕博利珠单抗,pembrolizumab)联用,治疗经组织学证实无法切除的III期或IV期非小细胞肺癌(NSCLC)患者。这些患者在接受Keytruda单药治疗后发生疾病进展。在2022年第一季度,Genprex预计将启动一项开放标签、多中心的1/2期临床试验,以评估这一治疗组合在此患者群体中的疗效与安全性。

Reqorsa由包裹在带有正电荷脂质分子纳米颗粒中的抑癌基因TUSC2组成,而肿瘤细胞一般带有负电荷。Reqorsa经静脉注射,能特异性靶向肿瘤细胞。Reqorsa具有多模式的作用机制,可中断引起肿瘤细胞复制和增殖的细胞信号通路,重新建立肿瘤细胞程序性死亡通路,并调节针对肿瘤细胞的免疫反应。Reqorsa也被证明可以阻断产生耐药性的机制。Genprex公司认为Reqorsa将是首个用于治疗人类癌症的全身性基因疗法。
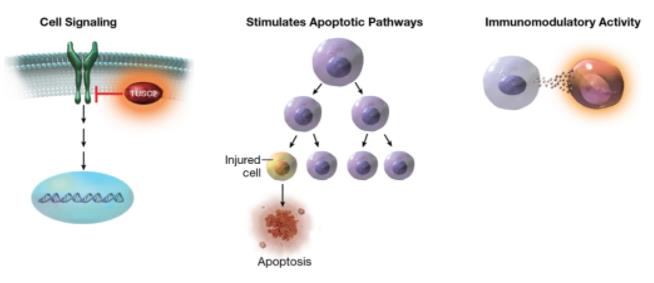
图片来源:Genprex公司官网
之前公布的临床前数据显示,Reqorsa和Keytruda具有协同作用。具体而言,在具有人源化免疫系统的转移性肺癌小鼠中,相比Keytruda单药治疗,Reqorsa+Keytruda的治疗组合更有效地提高了它们的存活率。并且,小鼠模型也证明了Reqorsa对免疫系统的多重影响,如增加自然杀伤细胞的产生和降低肿瘤细胞上的PD-L1表达,这被认为很可能有助于与Keytruda的协同作用。
此外,针对经组织学证实无法切除的III期或IV期NSCLC患者,Reqorsa与阿斯利康(AstraZeneca)第三代不可逆表皮生长因子受体(EGFR)酪氨酸激酶抑制剂泰瑞沙(Tagrisso)联用的治疗组合,此前已获得FDA授予FTD。这些患者携带EGFR突变且在泰瑞沙单药治疗后发生疾病进展。
Genprex总裁兼首席执行官Rodney Varner先生表示:“我们很高兴FDA授予Reqorsa第二个快速通道资格,用于治疗晚期NSCLC患者,这次将与检查点抑制剂Keytruda联用。这一快速通道资格是我们努力加速Reqorsa临床开发,和再次验证Reqorsa解决晚期NSCLC患者未满足医疗需求潜力的重要一步。”

 研发追踪
研发追踪
 药时代
药时代  2026-02-13
2026-02-13
 103
103

 研发追踪
研发追踪
 医药魔方
医药魔方  2026-02-13
2026-02-13
 96
96

 研发追踪
研发追踪
 瞪羚社
瞪羚社  2026-02-13
2026-02-13
 89
89