 产业资讯
产业资讯
 药融圈
药融圈  2022-01-14
2022-01-14
 4284
4284
2021年8月,艾博生物获得超过45亿元的C轮融资,刷新了中国生物医药企业IPO前单笔融资的纪录;到了11月,又获得了3亿美元的C+轮融资。2021年还未结束,艾博生物就获得了近70亿人民币的投资。
资本为核酸药物研发的热情着实添了一把火,为小核酸药物开发打开了一个新的百亿赛道。
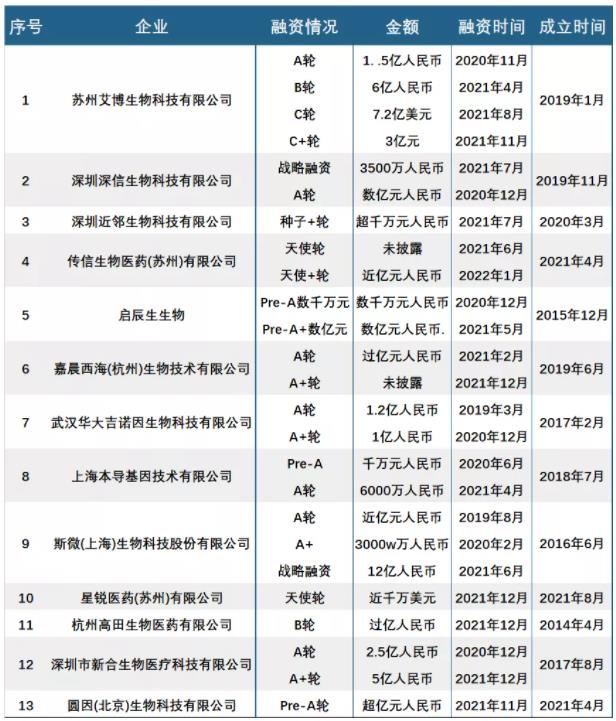
图1:2019年至今国内研发mRNA药物公司融资一览
(数据来源:公开资料整理)
小核酸开发难点多多,怎么办?
1.核酸分子不稳定,易降解
mRNA 自身稳定性差、易被体内的核酸酶降解,序列优化、碱基修饰以及加帽/尾对降解的保护有限。因此,mRNA药物需要有合适的递送载体将其递送至体内,才能有更好的免疫效果,开发高效无毒的递送系统是 mRNA 疫苗成功的关键。
2.核酸药物的潜在副作用
例如体外合成的mRNA具有较高的免疫原性,可能会诱发大量炎症反应。
3.药物递送系统是mRNA药物的关键
mRNA药物递送面临3个难点:胞外屏障、内体逃逸和胞内免疫。由于mRNA较大(104-106 Da),带负电荷,不能通过细胞膜的阴离子脂质双分子层。在体内,它被先天免疫系统的细胞吞噬并被核酸酶降解。此外,靶组织中存在细胞外切酶、细胞摄取效率低下或释放不成功都会限制mRNA的传递。
4.mRNA技术的发展目前仍处于早期
RNA作为一类全新药物形态的设想始于1990s,最初的十余年里,mRNA被认为过于不稳定且高纯度体外合成成本高昂, 大企业大多浅尝辄止。现在其分子量大,蛋白翻译机器对于去免疫原性和增加稳定性所必须的化学修饰容忍度低等原因,也让 mRNA 药物的发展滞后于小核酸药物 ASO 和 siRNA。
5.mRNA生产工艺流程复杂,存在较多“Know-how”环节
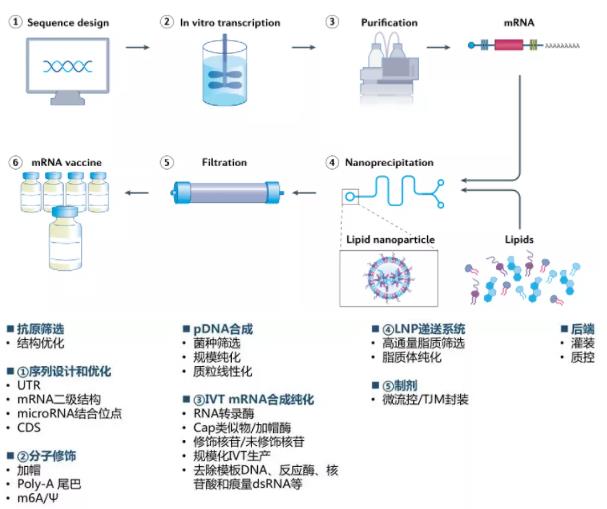
图2:mRNA生产工艺流程(来源:mRNA vaccines for infectious diseases: principles, delivery and clinical translation)
6.核酸药物的药代动力学研究亟待提高
虽然获批或在研的核酸药物或核酸疗法已经获得了阶段性成果,但具有相对完整药代动力学(ADME)数据的核酸药物相对较少。裸mRNA疗法的半衰期短,由于大量细胞外RNA酶迅速降解,体外转录的mRNA(IVT mRNA)及其蛋白产物的半衰期是影响药代动力学(PK)和药效学(PD)的关键因素。
7.生物分析较为复杂
核酸药物一般通过化学合成,分子量介于小分子化学药物与大分子生物制剂之间。但由于核酸药物是带电化合物,在生物环境中极不稳定,其理化性质与生物制剂更为相似,因此核酸药物的临床试验及生物分析比生物制剂更为复杂。

 产业资讯
产业资讯
 UmabsDB
UmabsDB  2025-06-23
2025-06-23
 47
47

 产业资讯
产业资讯
 支点财经
支点财经  2025-06-23
2025-06-23
 48
48

 产业资讯
产业资讯
 药视声
药视声  2025-06-23
2025-06-23
 50
50